Nový staging karcinomu endometria – FIGO 2023
New staging of endometrial carcinoma – FIGO 2023
Aim: To review the changes in the new version of the FIGO 2023 staging system for endometrial cancer. Methods and results: The new FIGO 2023 endometrial cancer staging system provides key updates for the diagnosis and treatment of endometrial cancer. An important step in diagnosis is molecular classification, which allows more accurate risk stratification for recurrence and the identification of targeted therapies. The new staging system, based on the recommendations of the international societies ESGO, ESTRO and ESP, incorporates not only the description of the pathological and anatomical extent of the disease, but also the histopathological characteristics of the tumour, including the histological type and the presence of lymphovascular space invasion. In addition, the staging system uses molecular testing to classify endometrial cancers into four prognostic groups: POLEmut, MMRd, NSMP and p53abn. Each group has its own specific characteristics and prognosis. The most significant changes have occurred in stages I and II, in which the sub-staging better reflects the biological behaviour of the tumour. This update increases the accuracy of prognosis and improves individualized treatment options for patients with endometrial cancer. Conclusion: The updated FIGO staging of endometrial cancer for 2023 incorporates different histologic types, tumour features, and molecular classifications to better reflect the current improved understanding of the complex nature of several endometrial cancer types and their underlying bio logic behaviour. The aim of the new endometrial cancer staging system is to better define stages with similar prognosis, allowing for more precise indication of individualised adjuvant radiation or systemic treatment, including the use of immunotherapy.
Keywords:
endometrial cancer – staging – FIGO – molecular classification – update
Authors:
M. Hruda 1
; B. Sehnal 1
; M. J. Halaška 1
; J. Drozenová 2
; Helena Robová 1
; Tomáš Pichlík 1
; L. Rob 1
Authors‘ workplace:
Onkogynekologické centrum, Gynekologicko-porodnická klinika 3. LF UK a FNKV, Praha
1; Ústav patologie, 3. LF UK a FNKV, Praha
2
Published in:
Ceska Gynekol 2024; 89(2): 120-127
Category:
doi:
https://doi.org/10.48095/cccg2024120
Overview
Cíl: Přehled změn v nové verzi stagingové klasifikace FIGO 2023 pro karcinomy endometria. Metodika a výsledky: Nový stagingový systém karcinomu endometria FIGO 2023 přináší klíčové aktualizace pro diagnostiku a léčbu karcinomů endometria. Důležitým krokem v diagnostice je molekulární klasifikace, která umožňuje přesněji stratifikovat riziko recidivy a určit cílené léčebné postupy. Nový stagingový systém vycházející z doporučení mezinárodních společností ESGO, ESTRO a ESP zapracoval kromě popisu patologicko-anatomického rozsahu onemocnění také histopatologické charakteristiky nádoru, mezi které patří histologický typ nádoru a přítomnost lymfangioinvaze. Navíc stagingový systém používá molekulární testování, podle něhož lze rozdělit karcinomy endometria do čtyř prognostických skupin: POLEmut, MMRd, NSMP a p53abn. Každá skupina má své specifické charakteristiky a prognózu. Nejvýznamnější změny nastaly ve stadiích I a II, ve kterých rozdělení na podstadia lépe reflektuje biologické chování nádoru. Tato aktualizace zvyšuje přesnost prognózy a zlepšuje možnosti individualizované léčby pro pacientky s karcinomem endometria. Závěr: Aktualizovaný FIGO staging karcinomu endometria pro rok 2023 zahrnuje různé histologické typy, nádorové rysy a molekulární klasifikaci, aby lépe odrážel současné lepší pochopení komplexní povahy několika typů karcinomu endometria a jejich základního biologického chování. Cílem nového stagingového systému karcinomu endometria je lépe definovat stadia s podobnou prognózou, což umožní přesnější indikaci individualizované adjuvantní radiační nebo systémové léčby včetně využití imunoterapie.
Klíčová slova:
karcinom endometria – staging – FIGO – molekulární klasifikace – aktualizace
Úvod
Karcinomy endometria jsou celosvětově šestou nejčastější malignitou u žen s kontinuálním vzestupem incidence [1]. Incidence se zvyšuje v souvislosti se stárnutím populace a rostoucí mírou obezity. V Evropě se za rok 2018 odhadnul počet nových případů karcinomu endometria na 121 578 a 29 638 pacientek na tuto diagnózu zemřelo [1]. Studie EURO-CARE-5 publikovaná v roce 2015 uvádí 5leté přežití u 76 % evropských žen v rozmezí od 72,9 % ve východní Evropě po 83,2 % v severní Evropě [2]. Česká republika patří v EU k zemím s nejvyšší incidencí. V roce 2019 bylo dosaženo vrcholu incidence 37,1/100 000 žen, což znamená více než 2 000 nových případů. Od roku 2019 však v ČR pozorujeme příznivý trend snižování incidence. Poslední data z roku 2021 ukazují pokles o 200 případů, což odpovídá incidenci 33,9 nových případů na 100 000 žen [3]. Celoživotní riziko v nezatížené populaci se pohybuje kolem 3 %, u geneticky zatížené populace pak kolem 40–60 % v případě Lynchova syndromu [4]. Vzhledem k časné symptomatologii je téměř 75 % pacientek diagnostikováno v časných stadiích, v naprosté většině případů je základní terapeutickou modalitou chirurgická léčba a jen část pacientek je poté indikována k adjuvantní terapii [3,5].
Stratifikace rizika podle molekulární klasifikace
Možnost molekulárního testování karcinomů endometria umožňuje významně zpřesnit prognózu konkrétní pacientky ve smyslu rizika recidivy [6–9]. Jedná se o zásadní posun v diagnostice a léčbě karcinomů endometria za posledních 10 let [7]. Pro potřeby běžné klinické praxe se na doporučení TCGA (the Cancer Genome Atlas) využívá relativně jednoduchá testace pomocí tří imunohistochemických markerů (p53, MSH6 a PMS2) a jednoho molekulárního testu (analýza patogenních POLE mutací) [6,9–12]. Pro správné vyhodnocení výsledků je zapotřebí provedení všech těchto vyšetření, provedení pouze jednoho testu je nedostatečné. Tento postup, jehož validita byla ověřena studií PORTEC 3 [8], umožňuje klasifikovat karcinom endometria do čtyř prognostických skupin: POLEmut, MMRd, NSMP a p53abn [4,7,13,14]:
- POLEmut (inaktivace DNA polymerázy e POLE) – typický je velký počet somatických mutací (tzv. ultramutované endometriální karcinomy). Přestože se většinou jedná o morfologicky vysoce maligní nádory (grade 3), mají vynikající prognózu s dlouhodobým přežitím dosahujícím bez adjuvantní terapie 98–100 % [4,12]. Naopak radioterapie a chemoterapie nemá na tyto nádory prakticky žádný léčebný efekt, ale tyto nádory dobře reagují na imunoterapii [4]. Zastoupení této skupiny v karcinomech endometria v naší populaci lze zatím pouze odhadovat na 6–12 % [6,8,11,15].
- MMRd (mismatch repair deficient) – zahrnuje karcinomy s mikrosatelitní nestabilitou (MSI) s vysokým počtem mutací (tzv. hypermutované endometriální karcinomy). Jejich prognóza se udává jako intermediální, i když jsou často vysoce maligní (grade 3, přítomnost lymfovaskulární invaze – LVSI) [4,12]. Stanovení prognózy zpřesní stanovení stadia nemoci, grade nádoru, závažnosti LVSI, exprese estrogenových a progesteronových receptorů. Část těchto nádorů, které jsou velmi citlivé na imunoterapii, je diagnostikována u pacientek s Lynchovým syndromem. Velikost této skupiny se odhaduje na 30–35 % [6,8,11,15].
- NSMP (non-specific molecular profile) – tyto endometriální karcinomy s nespecifickým molekulárním profilem vykazují nízký počet somatických početních alterací s nízkým počtem mutací chromozomů (copy number low, somatic copy-number alteration low – SCNA-low). Prognóza je intermediální až dobrá a odvíjí se od stadia onemocnění a dalších histopatologických charakteristik (grade, LVSI, exprese estrogenových a progesteronových receptorů) [16]. Tato skupina je největší (30–60 %), geneticky velmi heterogenní a výhledově bude nejspíše dále rozčleněna [6,8,11,15].
- (abnormalita genu TP53) – je přítomno vysoké množství početních změn chromozomů (copy number high, somatic copy-number alteration high/serous like – SCNA-high). Skupina zahrnuje serózní karcinomy, karcinosarkomy, asi 50 % světlobuněčných karcinomů a některé vysoce maligní endometrioidní karcinomy. Prognóza je velmi nepříznivá [8]. V naší populaci tvoří 12–25 % [6,8,11,15].
- p53abn
Přibližně 5 % všech endometriálních karcinomů vykazuje více než jednu molekulární charakteristiku (např. POLEmut a p53abn nebo MMRd a p53abn). Imunohistochemická pozitivita abnormálního p53 není 100% průkazem mutace TP53. Je tedy nutné provést kompletní molekulární testování k vyloučení případů, u nichž je aberantní exprese p53 sekundárním projevem ultramutovaného stavu při POLE mutaci či v rámci mikrosatelitní nestability u MMRd. Prognóza těchto nádorů se pak odvíjí od POLE mutace nebo MMRd (mikrosatelitní nestability) a podle toho je i přiděleno příslušné stadium [14]. Pro nádory se společnou molekulární charakteristikou POLEmut a MMRd jsou údaje omezené a v těchto případech by měl být zvážen screening na Lynchův syndrom [9].
Nový staging karcinomů endometria FIGO 2023
Poslední změna stagingového systému FIGO (Fédération Internationale de Gynécologie et d’Obstétrique – the International Federation of Gynecology and Obstetrics) karcinomu endometria byla přijata v roce 2008, o 2 roky později byly obdobné změny implementovány i do TNM systému [17,18]. Význam nových poznatků o molekulárních charakteristikách různých typů karcinomů endometria je tak zásadní, že důsledky se promítly i do definic mezinárodních doporučených postupů a nově také do stagingového systému FIGO pro karcinom endometria. V roce 2021 byla publikována společná doporučení (ESGO-ESTRO-ESP) pro diagnostiku, léčbu a sledování pacientek s karcinomem endometria tří evropských odborných společností [13]:
- Evropská společnost pro gynekologickou onkologii (ESGO – European Society of Gynaecological Oncology);
- Evropská společnost pro radioterapii a onkologii (ESTRO – European Society for Radiotherapy and Oncology);
- Evropská patologická společnost (ESP – European Society of Pathology).
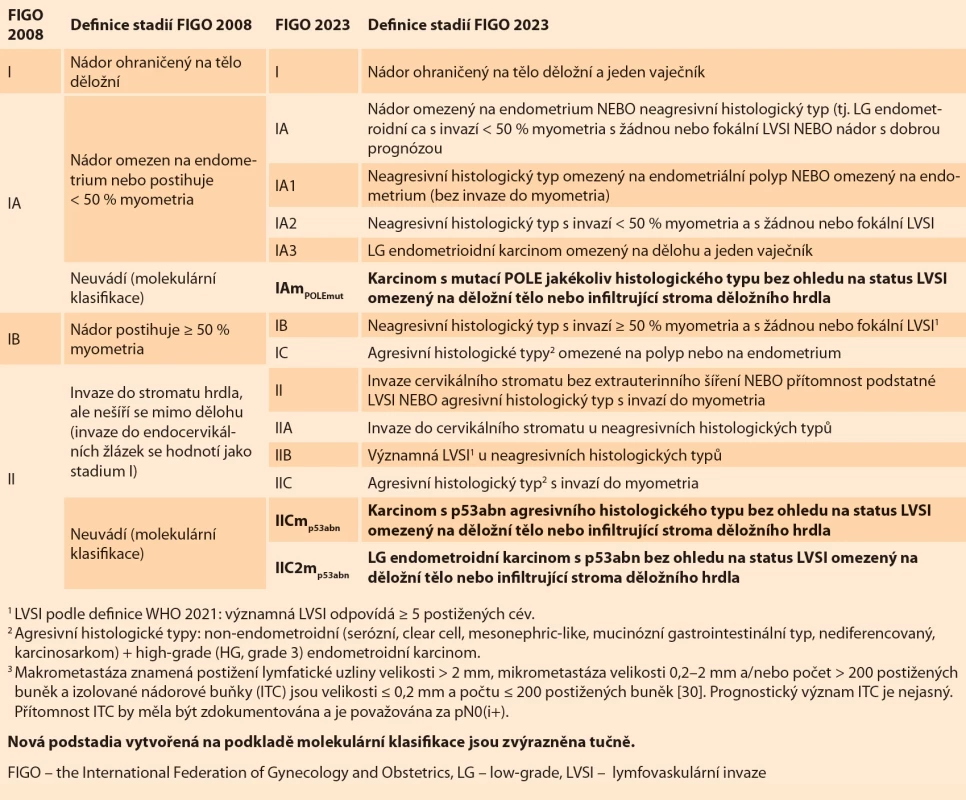
Již po 2 letech dochází také k aktualizaci stagingového systému. Nové poznatky zapracoval do stagingového systému multidisciplinární mezinárodní tým za předsednictví profesorů Nicole Concin (ESGO), Carien L Creutzberg (ESTRO) a Xavier Matias-Guiu (ESP) [7]. Stagingové systémy FIGO 2008 a FIGO 2023 prezentuje tab. 1. Stagingový systém pro karcinosarkom zůstává identický se stagingovým systémem pro karcinom endometria.
Stadium I
K významným změnám v rámci změn stagingového systému FIGO 2023 došlo již ve stadiu I. Do stadia IA, které ve stagingovém systému FIGO 2008 bylo vyhrazeno pouze pro nádory omezené na endometrium nebo s invazí do méně než poloviny myometria kteréhokoli histologického typu a přítomnost LVSI nehrála roli, se nyní řadí pouze nádory neagresivního histologického typu (LG – low-grade endometroidní karcinom, tzn. grade 1 a 2), které navíc mohou postihovat i jeden vaječník. Stadium IA se dělí na tři podstadia:
- IA1 – neagresivní histologický typ omezený na endometriální polyp nebo na endometrium;
- IA2 – neagresivní histologický typ postihující méně než polovinu myometria s žádnou nebo fokální LVSI (podle kritérií Světové zdravotnické organi - zace – WHO);
- IA3 – LG endometrioidní karcinomy s maximální invazí do poloviny šíře myometria se současným postižením jednoho vaječníku s dalšími podmínkami (nepřítomnost masivní LVSI, nepřítomnost dalších metastáz, bez invaze či ruptury kapsuly vaječníku).
Nádory zařazené do stadia IB jsou neagresivní histologické typy (tj. LG endometroidní karcinomy) s invazí přes polovinu myometria bez masivní LVSI (tzn. není žádná nebo je přítomna pouze fokální LVSI). Stadium IC je vyhrazeno pouze pro agresivní histologické typy nádorů bez prorůstání do myometria (tzn. omezené na polyp nebo na endometrium).

Stadium II
Revidovaný stagingový systém FIGO 2023 provádí ve stadiu II zásadní změny. Počet žen s nádory ve stadiu II podle nového stagingového systému výrazně stoupne. Stadium IIA zahrnuje nádory s neagresivním histotypem, které infiltrují stroma děložního hrdla. Stadium IIB nyní představují případy s neagresivním histotypem, ale s přítomností masivní LVSI bez ohledu na lokální šíření nádoru. Stadium IIC je vyhrazeno pouze pro agresivní histologické typy nádorů s prorůstáním do myometria jakékoli hloubky (agresivní histologické typy nádorů bez prorůstání do myometria spadají pod stadium IC).
Stadium III
Základní definice stadia III zůstala zachována: lokální a/nebo regionální šíření nádoru jakéhokoli histologického typu. Stadium IIIA nově rozlišuje mezi postižením (infiltrací) adnex (IIIA1) a děložní serózy (IIIA2), což lépe odráží chování nádoru, zejména u agresivních histotypů karcinomů. Stadium IIIB1 odpovídá předchozímu stadiu IIIB a je charakterizováno postižením pochvy nebo parametrií. Postižení pánevní pobřišnice je nyní klasifikováno jako IIIB2 (předchozí stadium IV), protože tyto případy jsou na rozdíl od stadia IV většinou indikovány k operační léčbě. Stadium IIIC s identickou definicí pro staging FIGO 2008 i FIGO 2023 (metastáza do pánevních a/nebo paraaortálních lymfatických uzlin) nově rozlišuje mikrometastázy (IIIC1i, IIIC2i) a makrometastázy (IIIC1ii, IIIC2ii) do lymfatických uzlin. Průkaz izolované nádorové buňky (ITC) se nepovažuje za metastázu (pN0 (i+)). Změna vyjadřuje lepší prognózu u pacientek s mikrometastázami do lymfatických uzlin [7,13,19]. Toto rozčlenění odráží také rostoucí využití techniky sentinelové uzliny s histologickým ultrastagingem, které se úspěšně prosazuje i v ČR [20]. Při postižení lymfatických uzlin zůstává hranice mezi stadiem III a IV identická, přítomnost metastáz v paraaortálních (suprapelvických) lymfatických uzlinách znamená postižení uzlin do úrovně odstupu renálních cév.
Stadium IV
Základní definice stadia IV se nemění (postižení sliznice močového měchýře a/nebo střeva nebo vzdálené metastázy), bylo ale přidáno další podstadium pro pacientky s peritoneálními metastázami nad úrovní pánve (stadium IVB). Peritoneální karcinomatóza je relativně vzácná (přibližně u 2 % ze všech pacientek s karcinomy endometria) a tyto pacientky je třeba odlišit od pacientek se vzdálenými metastázami [7,21]. Pacientky s peritoneálním postižením v oblasti pánve spadají do stadia IIIB2. Stadium IVC je vyhrazeno pro pacientky se vzdálenými metastázami (tzn. do lymfatických uzlin nad úrovní odstupu renálních cév nebo do jakýchkoli extraabdominálních lymfatických uzlin, do plic, jater, mozku nebo kostí).
Staging FIGO s molekulární klasifikací
Standardně se doporučuje provést u všech případů karcinomu endometria kompletní molekulární klasifikaci (POLEmut, MMRd, NSMP, p53abn) pro prognostickou stratifikaci rizikových skupin a stanovení potenciálních faktorů ovlivňujících rozhodnutí o adjuvantní a systémové léčbě.
U časného stadia karcinomu endometria mění přítomnost patogenních mutací POLE nebo abnormalit p53 stadium FIGO (tab. 1). U nádorů kategorizovaných do stadia I a II (omezený na děložní tělo nebo infiltrující stroma děložního hrdla) na základě chirurgicko-patologického nálezu se nyní karcinom endometria s mutací POLE bez ohledu na přítomnost LVSI nebo histologický typ klasifikuje jako stadium IAmPOLEmut, zatímco identické případy karcinomu endometria s průkazem p53abn se klasifikují jako stadium IICmp53abn. Ve vzácných případech, kdy LG endometroidní karcinom stadia I nebo II obsahuje mutaci p53, se stadium nádoru zvyšuje na IIC2mp53abn. Průkaz MMRd nebo NSMP nemění FIGO stadium, ale výsledek molekulární klasifikace by měl být zaznamenán jako stadium ImMMRd, ImNSMP, IImMMRd nebo IimNSMP.
Stadia III a IV se při známém výsledku molekulární klasifikace nemění, ačkoli znalost molekulární klasifikace přináší více prognostických informací a směrů léčby. Pokud molekulární klasifikace odhalí některý marker, měla by být tato skutečnost pro účely sběru a vyhodnocování dat do stadia zaznamenána (např. IIIB2mMMRd, IVCmp53abn, IIIA2mPOLEmut a podobně). Pokud bylo molekulární testování provedeno s negativním výsledkem, označení stadia se doplní ze stejného důvodu pouze písmenem „ m“ (např. IA3m nebo IVAm).
Diskuze
Cílem nového stagingového systému FIGO se začleněním histopatologických, imunohistochemických a molekulárních charakteristik bylo zpřesnění prognózy pro konkrétní stadium u pacientek se stejnými histologickými typy, ale s odlišnou biologickou povahou tumoru. Nový stagingový systém lépe definuje prognostické skupiny a usnadňuje management vhodné adjuvantní radiační a systémové terapie [7,13]. Současné úpravy by měly odstranit významné rozdíly v prognóze a délce přežití v jednotlivých stadiích podle stagingu z roku 2008.
Molekulární klasifikace karcinomů endometria rozdělí nádory prognosticky do skupin s nízkým, středním a vysokým rizikem. Pro doporučení adjuvantní léčby má molekulární klasifikace zvláště význam u high grade (HG) endometroidních a non-endometriodních karcinomů (serózní, clear cell, nediferencovaný, karcinosarkom, mesonephric-like, mucinózní gastrointestinální typ). HG endometroidní karcinom (grade 3) je klinicky, molekulárně a prognosticky heterogenní onemocnění, a proto tento typ nádoru nejvíce profituje z molekulární klasifikace pro stanovení prognózy a managementu léčby [22]. Bez molekulární klasifikace nelze HG endometroidní karcinom endometria stratifikovat do správné rizikové skupiny.
Molekulární testování je v této skupině schopné definovat pacientky s vynikající prognózou (POLEmut) od skupiny se špatnou prognózou (p53abn). Karcinomy endometria s MMRd nebo nespecifickým molekulárním profilem (NSMP) mají středně závažnou prognózu. Navíc průkaz MMRd představuje u pokročilých nádorů prediktor imunoterapie check-point inhibitory. Testování MMR je důležité také s ohledem na roli ve screeningu Lynchova syndromu [14]. Pokud není molekulární klasifikace známa, jsou HG endometroidní karcinomy zařazeny do stejného stadia vysoce rizikových nádorů a pacientky jsou indikovány k následné terapii. Naopak pacientky s karcinomy spadající do skupiny POLEmut mají nezanedbatelný prospěch z redukce pooperační adjuvantní terapie ve smyslu eliminace nežádoucích účinků radioterapie při zachování stejné prognózy [7,8,12,13]. Naproti tomu p53abn má výrazně horší prognózu a extenzivní adjuvantní terapie může být přínosem. Pokud není molekulární testace k dispozici, mělo by být stadium přiřazeno podle tradičních histopatologických kritérií (histopatologický typ, grade, hloubka myometrální invaze, přítomnost LVSI), která zůstávají důležitými prognostickými parametry [7,13]. Při průkazu MMRd nebo NSMP se stadium nemění. Důvody pro definice nových podstadií ve stadiu I vycházejí ze současných poznatků. Karcinomy endometria omezené na endometriální polypy nebo endometrium jsou spojeny s dobrou prognózou včetně agresivních histologických typů [7,23]. Na druhou stranu se u významné části (≥ 40 %) agresivních (zejména serózních) karcinomů, kde se předpokládá, že jsou ve stadiu IC (omezeny na polyp nebo endometrium), při důkladném stagingu zjistí okultní postižení lymfatických uzlin nebo peritonea, a proto se ve skutečnosti jedná o onemocnění ve stadiu III [7,24].
Vyjádření exprese LVSI hraje v prognóze nádoru významnou roli, a proto bylo do stagingu implementováno. Nepřítomnost nebo výskyt pouze fokální LVSI jsou u dobře diferencovaného endometroidního karcinomu omezeného na dělohu spojeny s velmi dobrou prognózou na rozdíl od přítomnosti masivní LVSI [7,25,26]. Kritéria pro LVSI se řídí pravidly WHO [22]. Exprese LVSI by tedy měla spadat do jedné z následujících tří kategorií:
- negativní LVSI (bez postižení cév);
- fokální LVSI (postižení < 5 cév);
- masivní LVSI (postižení ≥ 5 cév).
Dobře diferencované neagresivní endometroidní karcinomy mají dobrou prognózu i v případě postižení jednoho ovaria [7,27] nebo v případě hluboké invaze do myometria, pokud není přítomna masivní LVSI [7,25,26,28]. U pacientek s postižením endometria i ovaria byl v minulosti kladen velký důraz na rozlišení mezi metastázami a dvěma synchronními primárními karcinomy endometria a ovaria. V případě vysoce rizikových karcinomů endometria je postižení vaječníků téměř vždy kategorizováno jako metastatické [7]. Nicméně u low-risk (LR) endometroidních karcinomů je situace složitá. Recentní molekulární studie prokázaly, že původ endometriálního a ovariálního karcinomu je u těchto tumorů v naprosté většině případů ze stejné klonální buněčné linie, což naznačuje, že se primární tumor z endometria sekundárně šíří na ovaria [7,29]. Podle WHO klasifikace z roku 2020 [30] a také podle doporučení ESGO-ESTRO-ESP se doporučuje konzervativní postup bez adjuvantní terapie pro pacientky se synchronním LR karcinomem endometria a ovaria, neboť prognóza je u těchto případů velmi dobrá [7,13,31]. Nový revidovaný FIGO staging karcinomu endometria respektuje tento postoj a zavádí kategorii stadia IA3 u LG endometroidních karcinomů, pokud jsou splněna následující kritéria:
- není přítomna hluboká myometriální invaze < 50 %;
- není přítomna masivní LVSI;
- nejsou přítomny jiné metastázy;
- nádor je omezený pouze na jeden vaječník a není přítomna invaze/porušení pouzdra (ekvivalent pT1a).
Případy, které nesplňují tato kritéria, by měly být klasifikovány jako stadium IIIA1 (metastáza karcinomu endometria do vaječníků).
Nádorové postižení vejcovodu se automaticky řadí do stadia IIIA1. Postižení mukózy vejcovodu u karcinomu endometria má nejasný prognostický význam, neexistují žádné silné vědecké důkazy. Mělo by se vždy odlišit postižení vejcovodů u serózního karcinomu od paralelní přítomnosti primárního serózního intraepiteliálního karcinomu vejcovodu (STIC). Patologové by měli být pečliví při rozlišování metastázy serózního karcinomu v tubě od duplicitního nezávislého STIC. V těchto případech je vhodné vyšetřit tuby histologicky podle protokolu SEE-FIM [7] a také imunohistochemicky. Přítomnost intraluminálních volných fragmentů tumoru v tubě je kontroverzní a není rozhodující pro stanovení stadia. Totéž platí pro pozitivní cytologii z laváže [7].
Mezinárodní retrospektivní studie ze tří akreditovaných onkogynekologických center v Rakousku a Itálii retrospektivně srovnávala 519 pacientek s karcinomem endometria podle stagingových systémů FIGO 2008 a 2023 [32]. Obě skupiny byly porovnávány ve smyslu prognostické přesnosti na základě 5letého období bez progrese nemoci (PFS – progression-free survival) a celkového přežití (OS – overall survival). Ke změně (pod) stadia došlo u 143 (27,6 %) pacientek, z toho celkem 123 (23,7 %) pacientkám bylo přiřazeno vyšší stadium a ostatním 20 (3,9 %) nižší stadium. Kohorta ve stadiu I podle FIGO 2023 vykazovala výrazně vyšší 5letý PFS ve srovnání s FIGO 2008 (93,0 vs. 87,4 %). U onemocnění stadia II byla 5letá míra PFS podobná v obou skupinách (70,2 vs. 71,2 %). Dvě nová molekulárně definovaná podstadia IAmPOLEmut a IICmp53abn podle 2023 FIGO vykazovaly zcela odlišné onkologické výsledky. Všechny aplikované statistické testy potvrdily přesnější predikci PFS a OS pomocí stagingového systému FIGO 2023 ve srovnání s FIGO 2009 [32].
Velký význam některých imunohistochemických markerů pro prognózu pacientek s karcinomem endometria potvrdila i prospektivní studie z brněnského onkogynekologického centra [33]. Autoři v rámci předoperační stratifikace pacientek s nízkým nebo vysokým rizikem hodnotili mimo standardní kritéria (věk, stadium, histologický typ, grade, lymfovaskulární invaze) také význam přítomnosti některých imunohistochemických biomarkerů (L1CAM, ER, PR a p53). Celkem bylo zařazeno 132 pacientek. Když byly do diagnostického modelu zahrnuty imunohistochemické markery, významně se zlepšila senzitivita pro stanovení skupiny s vysokým rizikem (48,4 vs. 75,8 %; p < 0,001) se statisticky nevýznamným poklesem specificity na 80 % (p = 0,238). Pozitivní prediktivní hodnota (PPV) byla pro obě metody podobná, zatímco negativní prediktivní hodnota (NPV, tj. pravděpodobnost extrémně nízkého rizika v negativních testovacích případech) se statisticky signifikantně zlepšila (66,0 vs. 78,9 %; p < 0,001) [33].
Existují obavy, že molekulární testování, které přináší zásadní změny do diagnosticko-léčebného algoritmu, kvůli své komplexnosti oddálí zahájení léčebného procesu. Výsledky observační studie z onkogynekologického centra FN Brno tyto obavy nepotvrdily. Do své analýzy zařadili od května 2021 do května 2022 celkem 85 pacientek s nově diagnostikovaným karcinomem endometria. V rámci standardního histopatologického vyšetření byl u všech pacientek imunohistochemicky stanoven status proteinů p53 a MMR. U tumorů nesplňujících klinická kritéria pro nízké riziko a vždy při průkazu MMRd nebo p53abn bylo provedeno také molekulárně genetické testování genu POLE. Všem pacientkám s MMRd tumory a/nebo pozitivní rodinnou anamnézou byla doporučena genetická konzultace. Z 18 geneticky testovaných pacientek byla u 4 (22 %) prokázána hereditární forma onemocnění. Medián doby od operace po projednání na multioborovém onkogynekologickém týmu byl 21 (8–36) dní. Celkem 76 (90 %) pacientek absolvovalo komplexní doporučenou léčbu. Závěrem autoři konstatují, že molekulární testování je u všech pacientek s karcinomem endometria v běžné praxi proveditelné a neprodlužuje dobu nutnou pro rozhodnutí o adjuvantní terapii [34].
Optimální by bylo testování všech karcinomů endometria. V současné době však molekulární testování nemá stejný klinický význam pro všechny rizikové skupiny. Každý případ je nutné posuzovat individuálně. Podle společného doporučení českých odborných společností se molekulární vyšetření provádí vždy na žádost klinika z komplexního onkologického centra (KOC) či onkogynekologického centra a doporučuje se testovat až po vyšetření definitivního resekátu, nikoli hned v rámci odběru biopsie (materiál z diagnostického odběru však může být také použit) [14]. Předpokládá se využití molekulárního testování pro stanovení rizika nemoci v případě fertilitu zachovávajících postupů, které je možno zvážit u mladých žen s karcinomem endometria splňujících předepsaná kritéria [35].
Závěr
Nový stagingový systém FIGO 2023 je strukturován tak, aby zahrnul jak standardní histopatologické parametry, tak i molekulární prognostické faktory ovlivňující chování zhoubných nádorů endometria. Účelem stagingového systému je poskytnout klasifikaci šíření tumoru, aby jednotlivým stadiím odpovídaly určité modality terapie s konkrétní prognózou onemocnění. Operační léčba je v ČR centralizována v onkogynekologických centrech. Tato centra by měla disponovat možnostmi adekvátního histopatologického zpracování operačních preparátů vč. molekulárního testování a vyšetření sentinelových uzlin ultrastagingem. Chirurgická léčba s detekcí sentinelové uzliny je v současnosti standardem u všech rizikových skupin. Lze předpokládat, že aktuální stagingový FIGO 2023 systém bude na základě výsledků prospektivně prováděných studií dále revidován. Doufejme, že kromě dalšího zpřesnění prognózy jednotlivých stadií dojde i k jeho zjednodušení pro klinickou praxi.
Sources
1. Sung H, Ferlay J, Siegel RL et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2021; 71 (3): 209–249. doi: 10.3322/caac.21660.
2. Sant M, Chirlaque Lopez MD, Agresti R et al. Survival of women with cancers of breast and genital organs in Europe 1999–2007: results of the EUROCARE-5 study. Eur J Cancer 2015; 51 (15): 191–205. doi: 10.1016/j.ejca.2015.07. 022.
3. Dušek L, Mužík J, Kubásek M et al. Epidemiologie zhoubných nádorů v České republice. Masarykova univerzita. 2007 [online]. Dostupné z: http: //www.svod.cz.
4. Presl J, Vaněček T, Michal M et al. Molekulární klasifikace endometriálních karcinomů převedená do praxe. Ceska Gynekol 2021; 86 (4): 258–262. doi: 10.48095/cccg2021258.
5. Vinklerová P, Felsinger M, Frydová S et al. Je nález hyperplazie či polypu děložní dutiny automatickou indikací k biopsii? Ceska Gynekol 2020; 85 (2): 84–93.
6. Kandoth C, Schultz N, Cherniack AD et al. Cancer Genome Atlas Research Network. Integrated genomic characterization of endometrial carcinoma. Nature 2013; 497 (7447): 67–73. doi: 10.1038/nature12113.
7. Berek JS, Matias‐Guiu X, Creutzberg C et al. FIGO staging of endometrial cancer: 2023. Int J Gynecol Obstet 2023; 162 (2): 383–394. doi: 10.1002/ijgo.14923.
8. León-Castillo A, de Boer SM, Powell ME et al. Molecular classification of the PORTEC-3 trial for high-risk endometrial cancer: impact on prognosis and benefit from adjuvant therapy. J Clin Oncol 2020; 38 (29): 3388–3397. doi: 10.1200/JCO.20.00549.
9. Piulats JM, Guerra E, Gil-Martín M et al. Molecular approaches for classifying endometrial carcinoma. Gynecol Oncol 2017; 145 (1): 200–207. doi: 10.1016/j.ygyno.2016.12.015.
10. Talhouk A, McConechy MK, Leung S et al. A clinically applicable molecular-based classification for endometrial cancers. Br J Cancer 2015; 113 (2): 299–310. doi: 10.1038/bjc.2015.190.
11. Talhouk A, McConechy MK, Leung S et al. Confirmation of ProMisE: a simple, genomics-based clinical classifier for endometrial cancer. Cancer 2017; 123 (5): 802–813. doi: 10.1002/cncr. 30496.
12. Stelloo E, Nout RA, Osse EM et al. Improved risk assessment by integrating molecular and clinicopathological factors in early-stage endometrial cancer-combined analysis of the PORTEC cohorts. Clin Cancer Res 2016; 22 (16): 4215–4224. doi: 10.1158/1078-0432.CCR-15-2878.
13. Concin N, Matias-Guiu X, Vergote I et al. ESGO/ESTRO/ESP guidelines for the management of patients with endometrial carcinoma. Int J Gynecol Cancer 2021; 31 (1): 12–39. doi: 10.1136/ijgc-2020-002230.
14. Dundr P, Cibula D, Doležel M et al. Molekulární testování u karcinomu endometria – společné doporučení ČOS, onkogynekologické sekce ČGPS, SROBF a SČP ČLS JEP. Ceska Gynekol 2021; 86 (4): 264–272. doi: 10.48095/cccg2021264.
15. Kommoss S, McConechy MK, Kommoss F et al. Final validation of the ProMisE molecular classifier for endometrial carcinoma in a large population-based case series. Ann Oncol 2018; 29 (5): 1180–1188. doi: 10.1093/annonc/mdy058.
16. Horeweg N, de Bruyn M, Nout RA et al. Prognostic integrated image-based immune and molecular profiling in early-stage endometrial cancer. Cancer Immunol Res 2020; 8 (12): 1508–1519. doi: 10.1158/2326-6066.CIR-20-0149.
17. Creasman W. Revised FIGO staging for carcinoma of the endometrium. Int J Gynaecol Obstet 2009; 105 (2): 109. doi: 10.1016/j.ijgo.2009.02.010.
18. Sehnal B, Driák D, Kmonícková E et al. Současná klasifikace zhoubných nádorů v onkogynekologii – část II. Ceska Gynekol 2011; 76 (5): 360–366.
19. Mueller JJ, Pedra Nobre S, Braxton K et al. Incidence of pelvic lymph node metastasis using modern FIGO staging and sentinel lymph node mapping with ultrastaging in surgically staged patients with endometrioid and serous endometrial carcinoma. Gynecol Oncol 2020; 157 (3): 619–623. doi: 10.1016/j.ygyno.2020.03.025.
20. Vinklerová P, Minář L, Weinberger V et al. Změna trendu operační léčby a stagingu lymfatických uzlin u karcinomu endometria – výsledky Onkogynekologického centra Gynekologicko-porodnické kliniky FN Brno a LF MU v letech 2012–2021. Ceska Gynekol 2022; 87 (5): 308–316. doi: 10.48095/cccg2022308.
21. Burg L, Timmermans M, van der Aa M et al. Incidence and predictors of peritoneal metastases of gynecological origin: a population-based study in the Netherlands. J Gynecol Oncol 2020; 31 (5): e58. doi: 10.3802/jgo.2020.31.e58.
22. Bosse T, Nout RA, McAlpine JN et al. Molecular classification of grade 3 endometrioid endometrial cancers identifies distinct prognostic subgroups. Am J Surg Pathol 2018; 42 (5): 561–568. doi: 10.1097/PAS.00000000000 01020.
23. Assem H, Rottmann D, Finkelstein A et al. Minimal uterine serous carcinoma and endometrial polyp: a close clinicopathological relationship. Hum Pathol 2021; 118 : 1–8. doi: 10.1016/ j.humpath.2021.09.001.
24. Xu H, Cui SS, Ran L et al. Incidence of omental metastasis in uterine serous carcinoma: a systematic review and meta-analysis. J Gynecol Obstet Hum Reprod 2022; 51 (6): 102395. doi: 10.1016/j.jogoh.2022.102395.
25. Bosse T, Peters EE, Creutzberg CL et al. Substantial lymph-vascular space invasion (LVSI) is a significant risk factor for recurrence in endometrial cancer – a pooled analysis of PORTEC 1 and 2 trials. Eur J Cancer 2015; 51 (13): 1742–1750. doi: 10.1016/j.ejca.2015.05.015.
26. Tortorella L, Restaino S, Zannoni GF et al. Substantial lymph-vascular space invasion (LVSI) as predictor of distant relapse and poor prognosis in low-risk early-stage endometrial cancer. J Gynecol Oncol 2021; 32 (2): e11. doi: 10.3802/jgo.2021.32.e11.
27. Zhan X, Li L, Wu M et al. The prognosis of stage IA synchronous endometrial endometrioid and ovarian carcinomas. Arch Gynecol Obstet 2019; 300 (4): 1045–1052. doi: 10.1007/s00404-019-05288-5.
28. Veade AE, Foote J, Ehrisman J et al. Associations between lymphovascular space invasion, nodal recurrence, and survival in patients with surgical stage I endometrioid endometrial adenocarcinoma. World J Surg Oncol 2019; 17 (1): 80. doi: 10.1186/s12957-019-1620-x.
29. Anglesio MS, Wang YK, Maassen M et al. Synchronous endometrial and ovarian carcinomas: Eevidence of clonality. J Natl Cancer Inst 2016; 108 (6): djv428. doi: 10.1093/jnci/djv428.
30. WHO Classification of Tumours Editorial Board. Female Genital Tumours. Lyon: International Agency for Research on Cancer 2020.
31. Turashvili G, Gómez-Hidalgo NR, Flynn J et al. Risk-based stratification of carcinomas concurrently involving the endometrium and ovary. Gynecol Oncol 2019; 152 (1): 38–45. doi: 10.1016/j.ygyno.2018.10.033.
32. Schwameis R, Fanfani F, Ebner C et al. Verification of the prognostic precision of the new 2023 FIGO staging system in endometrial cancer patients – an international pooled analysis of three ESGO accredited centres. Eur J Cancer 2023; 193 : 113317. doi: 10.1016/j.ejca.2023.113317.
33. Weinberger V, Bednarikova M, Hausnerova J et al. A novel approach to preoperative risk stratification in endometrial C cancer: the added value of immunohistochemical markers. Front Oncol 2019; 9 : 265. doi: 10.3389/fonc.2019.00265.
34. Bednaříková M, Hausnerová J, Minář L et al. Molekulární testování karcinomu endometria – analýza prvních zkušeností z klinické praxe. Klin Onkol 2023; 36 (3): 215–223. doi: 10.48095/ccko2023215.
35. Hejl Z, Hanáček J, Pilka R. Fertilitu zachovávající postupy u mladých žen s karcinomem endometria. Ceska Gynekol 2022; 87 (3): 202–205. doi: 10.48095/cccg2022202.
ORCID autorů
M. Hruda 0000-0002-7606-5164
B. Sehnal 0000-0003-2622-2181
M. J. Halaška 0000-0001-6055-2569
J. Drozenová 0009-0005-5695-1221
H. Robová 0000-0002-6136-7602
T. Pichlík 0000-0001-6732-1421
L. Rob 0000-0003-3770-651X
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicineArticle was published in
Czech Gynaecology

2024 Issue 2
-
All articles in this issue
- Artificial activation of sperm motility in vitro
- Reactive oxygen species and their role in the andrological factor of couple fertility
- Metrics of uterine myomatosis symptomatology in clinical practice
- Trophoblast stem cells, trophoblast invasion, and organoids – advancements in gynecology
- Usage of the levonorgestrel releasing intrauterine system in perimenopause
- Combined contraceptives – the choice of estrogen matters
- Fecal incontinence risk factors and pregnancy
- Haemorrhagic stroke in pregnancy
- Interprofessional cooperation with a dermatovenerologist – specifics of hidradenitis suppurativa management in gynaecological practice
- New staging of endometrial carcinoma – FIGO 2023
- A new perspective on Endometrial Carcinoma classification and management strategies in context of molecular subtypes
- Dynamics of serum levels and reference ranges of copeptin in the 3rd trimester of pregnancy in healthy pregnant women with uncomplicated pregnancy and delivery
- Peritumoral stroma and systemic inflammatory response in cervical cancer
- Czech Gynaecology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- New staging of endometrial carcinoma – FIGO 2023
- Usage of the levonorgestrel releasing intrauterine system in perimenopause
- Metrics of uterine myomatosis symptomatology in clinical practice
- Trophoblast stem cells, trophoblast invasion, and organoids – advancements in gynecology
