Vaskularizovaná léze myometria
Enhanced myometrial vascularity
Objective: Case report of a gynecologically polymorbid patient with enhanced myometrial vascularity, and review of current scientific literature on incidence, diagnostic method, and management of this phenomenon. Case report: A 38-year-old patient that has been treated long-term for secondary sterility with a medical history of laparotomic cytoreduction surgery for adenomyosis and subsequent development and treatment of postoperative intrauterine adhesions. Currently presenting with enhanced myometrial vascularity after spontaneous abortion. For symptomatic prolonged course of the observation period without tendency for spontaneous regression and risk of acute hemorrhage, she was initially indicated for selective embolization of uterine arteries and consecutive definitive treatment via hysteroscopic resection. Conclusion: Due to low incidence and tendency for spontaneous resorption, early recognition, and correct management of enhanced myometrial vascularity, it still represents a medical challenge.
Keywords:
hysteroscopy – retained products of conception – enhanced myometrial vascularity – uterine artery embolization
Autoři:
Adéla Richtárová 1
; Kristýna Hlinecká 1
; Zdeňka Lisá 1
; B. Boudová 1,3
; R. Kocián 1
; J. Kaván 2
; Michal Mára 1
Působiště autorů:
Gynekologicko-porodnická klinika 1. LF UK a VFN v Praze
1; Radiodia gnostická klinika 1. LF UK a VFN v Praze
2; Gynekologicko-porodnické oddělení, Oblastní nemocnice Trutnov a. s.
3
Vyšlo v časopise:
Ceska Gynekol 2022; 87(4): 249-254
Kategorie:
Kazuistika, přehledový článek
doi:
https://doi.org/10.48095/cccg2022249
Souhrn
Cíl: Kazuistika gynekologicky polymorbidní pacientky s diagnózou vaskularizované léze myometria, shrnutí současných vědeckých poznatků o výskytu, diagnostice a léčbě tohoto fenoménu. Kazuistika: Třicetiosmiletá pacientka dlouhodobě léčena pro sekundární sterilitu s anamnézou laparotomické cytoredukční operace adenomyózy, s následným rozvojem a léčbou pooperačních nitroděložních srůstů. Nyní sledována pro diagnózu vaskularizované léze myometria po spontánním abortu. Vzhledem k symptomatickému protrahovanému průběhu bez tendence ke spontánní úpravě stavu a riziku rozvoje akutní hemoragie pacientka nejprve indikována k selektivní embolizaci uterinních tepen a následnému definitivnímu řešení cestou operační hysteroskopie. Závěr: Vzhledem k nízké incidenci a tendenci ke spontánní úpravě, ale také k potenciálně velmi vážným až letálním komplikacím zůstává včasné rozpoznání a správný management vysoce vaskularizovaných lézí myometria lékařskou výzvou.
Klíčová slova:
hysteroskopie – vysoce vaskularizovaná léze myometria – placentární rezidua – embolizace uterinních tepen
Úvod
Vysoce vaskularizovaná léze myometria (EMV – enhanced myometrial vascularity) je nález abnormálních cévních arteriovenózních spojek ve tkáni myometria [1,2]. V literatuře byl tento fenomén také popisován jako získaná arteriovenózní malformace (AVM) a je postupně nahrazován situaci lépe popisujícím termínem EMV [1–4].
Vysoce vaskularizovaná léze myometria vzniká u žen v reprodukčním věku výhradně v návaznosti na proběhlé těhotenství a je spojována s nesprávnou involucí placenty či placentárními rezidui (RPOC – retained product of conception) [5–7]. Jsou popisovány asymptomatické případy přes mírné průběhy projevující se slabým krvácením či špiněním až po pacientky s rozvojem akutního život ohrožujícího krvácení [1]. Diagnostika se opírá primárně o vaginální ultrasonografické vyšetření (USG) s použitím barevného dopplerovského zobrazování [3,8,9], kde v oblasti myometria pozorujeme typickou barevnou síť cév s turbulentním, vysokorychlostním a nízkoodporovým prouděním krve. Z laboratorních vyšetření bývá obvyklé přetrvávání mírné elevace hCG.
Management EMV je velmi individuální a závisí na klinických projevech pacientky a zkušenostech, resp. možnostech pracoviště. Podstatou léčby je však vždy vymizení, nebo kompletní odstranění placentárních reziduí, na něž navazuje rychlá involuce ložiska EMV.
Kazuistika
Pacientka, 38letá, jinak interně zdravá žena, nullipara, kuřačka, přichází na naše pracoviště k prvnímu vyšetření a rozvaze již v roce 2019 se symptomy těžké dysmenorey doprovázené nauzeou a zvracením, silným menstruačním krvácením vč. 2denního krvácení v koagulech, které pacientce znemožňovaly veškeré pracovní i sociální aktivity. Pacientka je od roku 2011 léčena se sterilitou, v anamnéze má tři spontánní prvotrimestrální aborty s nutností instrumentální revize dutiny děložní, následně dva cykly in vitro fertilizace (IVF) a vícečetné neúspěšné kryoembryotransfery (KET).
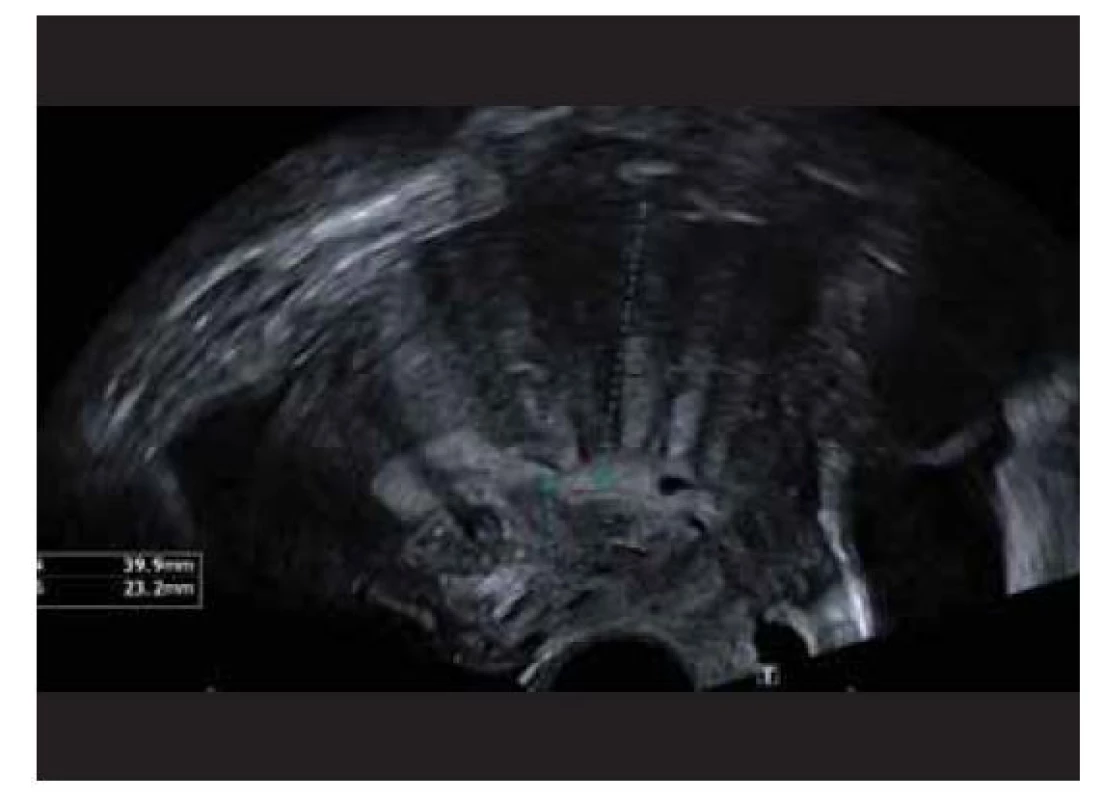
Dle našeho vstupního USG vyšetření je pacientce diagnostikována difuzní adenomyóza infiltrující kompletně (od zesílené junkční endomyometrální zóny až k zevnímu povrchu dělohy) přední stěnu děložní [10]. Poměr přední a zadní stěny děložní je 40/23 mm, léze má typický nepravidelný tvar, nehomogenní charakter, nejasné ohraničení vůči okolí s vějířovitým stínem (obr. 1). Pacientka je v říjnu 2019 indikována k elektivně laparotomické (pro velký objem léze) cytoredukční operaci adenomyózy, debulking. Peroperační nález potvrzuje USG nález, postupně je vytnut rozsáhlý adenomyotický uzel (123 g), který prostupuje celou přední stěnu děložní až k fundu a oběma děložním rohům. Byť peroperačně nedochází k makroskopicky evidentnímu intrauterinnímu průniku, právě v oblasti děložních rohů nelze drobné narušení dutiny zcela vyloučit. Operace probíhá jinak bez komplikací a pacientka je propuštěna do domácí péče 3. den po výkonu. Na plánované kontrole, s odstupem měsíce, USG nález odpovídá pooperačním změnám, myometrium přední stěny je kompaktní a bez nálezu signifikantního rezidua adenomyózy. Pacientka zde udává zásadní ústup menstruačních symptomů a je jí dovoleno koncipovat s odstupem 6 měsíců od operace.
Fig. 1. Diffuse uterine adenomyosis.
Pacientka je k nám opětovně odeslána v červenci 2020 po dalších dvou neúspěšných KET ke zvážení hysteroskopie. V té době menstruuje pravidelně, mírnější intenzitou než před primárním cytoredukčním výkonem, kdy však byla její menstruace zesilována adenomyózou (krvácení v koagulech). Hysteroskopie odhalila obraz pevných fibrózních synechií v oblasti obou děložních rohů, jež byly rozrušeny studenými nůžkami pomocí 8,5mm operačního hysteroskopu (Olympus Czech Group, s. r. o., člen koncernu). Nález byl v souladu se suspekcí na bilaterální nitroděložní průnik při primární operaci. Po provedené synechiolýze byl do dutiny děložní aplikován antiadhezivní gel s kyselinou hyaluronovou (Hyalobarrier Gel, Anika Therapeutics S.r. l. Corso Stati Uniti 4/U–35127 Padova (PD), Italy) jako prevence vzniku neoadhezí. Pacientce je doporučeno na hysteroskopii navázat dalším KET.
Pacientka po proběhlém KET otěhotněla a spontánně v listopadu 2020 potratila bez nutnosti provedení instrumentální revize dutiny děložní. Na naše pracoviště je opět odeslána v lednu 2021, 8 týdnů od potratu pro přetrvávající špinění a mírnou elevaci hCG (48–76 IU/l). Dle vaginálního USG je popsáno ložisko EMV velikosti 50 × 27 × 41 mm s mnoha cévními lakunami a turbulentním prouděním krve s maximální průtokovou rychlostí (PSV – peak systolic velocity) 90 cm/s (obr. 2). Vzhledem k potenciální závažnosti dané léze je pacientka odeslána k provedení magnetické rezonance (MR) jako doplňkové diagnostické metody, která tuto diagnózu i velikost ložiska potvrzuje (obr. 3). Pro neúspěch primárního expektačního postupu a perzistenci příznaků je přistoupeno ke kombinované intervenci. Vzhledem k velikosti ložiska EMV, výši hodnot PSV a s nimi spojenými riziky rozvoje profuzního děložního krvácení je nejprve pacientka indikována k selektivní embolizaci obou uterinních tepen (UAE – uterine artery embolization). Ta byla úspěšně provedena v březnu 2021 (obr. 4, 5) s použitím metalických embolizačních spirál. Pravá uterinní tepna byla kompletně uzavřena dvěma odpoutatelnými spirálami velikosti 5 × 150 mm, levá uterinní tepna byla kompletně uzavřena dvěma odpoutatelnými spirálami 5 × 150 mm a dvěma volnými spirálami 4 × 30 mm. S odstupem 10 dní po UAE byla pacientce provedena hysteroskopie. Peroperačně byla dutina děložní kompletně vyplněna bezcévným nekrotickým materiálem vzhledu placentárních reziduí. Ta jsou nejprve šetrně vybavena kyretou a poté doresekována bipolární kličkou resektoskopu (VersaPoint-Bipolar Resectoscopic System, Gynecare, Ethicon, Inc., USA). Při resekci je fenestrována cca 1,5cm lakuna myometria přední stěny, ze které odtéká stará, tmavá krev, vs. místo EMV, které díky provedené UAE dále nekrvácí. Poté je již spodina čistá, hladká, bez dalších placentárních reziduí či abnormálních cév. Výkon proběhl bez komplikací s minimální krevní ztrátou a pacientka byla týž den propuštěna. Při plánované kontrole s odstupem 1 měsíce je zcela asymptomatická, sérová hladina hCG je negativní a dle USG nálezu došlo ke kompletní regresi EMV. Výsledek histologie potvrzuje nález placentárních reziduí po proběhlém potratu.
EMV – vysoce vaskularizovaná léze myometria,
USG – ultrasonografie
Fig. 2. EMV lesion on USG examination.

EMV – vysoce vaskularizovaná léze myometria, MR – magnetická rezonance
Fig. 3. EMV lesion on MRI examination.

UAE – embolizace uterinních tepen
Fig. 4. Right uterine artery before UAE.
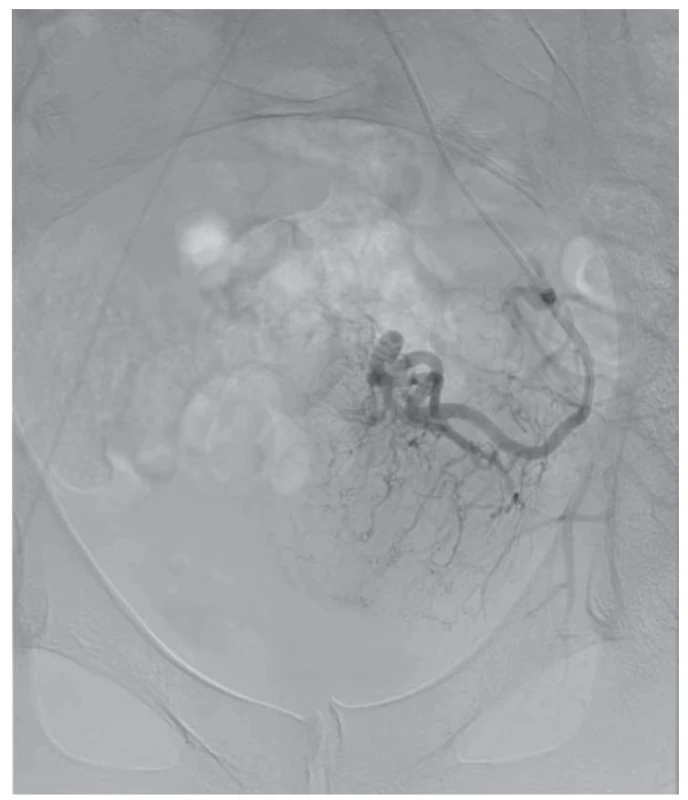
UAE – embolizace uterinních tepen
Fig. 5. Image after the performed UAE.

Diskuze
Získané AVM, nyní EMV, jsou patologicky vytvořené spojky mezi větvemi uterinních arterií a venózními plexy, které obchází kapilární řečiště [2]. Je pro ně charakteristická možnost postupného spontánního vymizení, čímž se liší od pravých, vrozených AVM, které jsou popisovány jako poruchy morfogeneze buněk, a nemají tudíž tendenci k samovolné regresi [11]. Vzniká v nich vysokorychlostní, nízkoodporové, turbulentní proudění krve potenciálně ohrožující pacientku rychlou a objemnou krevní ztrátou.
Incidence tohoto fenoménu není zcela jasná, částečně také proto, že se v literatuře doposud zaměňuje za dříve používaný název AVM [1,12]. Van den Bosch et al ve své studii na 385 pacientkách popsali ložisko EMV v rámci kontrolního USG vyšetření v šestinedělí po spontánním porodu či potratu v 8 % případů. Ložiska EMV byla přítomna zejména v časném stadiu puerperia, případně při nálezu placentárních reziduí, a to výhradně v oblasti předchozího uložení placenty [7]. Na tuto studii navazují Van Schoubroeck et al svou prospektivní prací na 93 pacientkách po nekomplikovaném vaginálním porodu, kde je ložisko EMV na USG popsáno až u 51 % pacientek 3. den po porodu oproti pouhým 4 % na konci šestinedělí [6]. Obě studie pracují s teorií, že charakter a rozsah EMV je tranzientní, jedná se do jisté míry o přirozený proces reflektující involuci placentárního lůžka, ve většině případů má tendenci ke spontánní regresi a přetrvává pouze za přítomnosti RPOC. Grewal et al stanovují incidenci EMV na 1,52 % na základě své studie na 2 627 ženách po prvotrimestrálním potratu [12]. Vzhledem k velikosti souboru lze považovat tuto hodnotu za nejreálnější.
Hlavním klinickým projevem EMV je abnormální děložní krvácení navazující na proběhlé těhotenství. Pacientky mohou být zcela asymptomatické, zde může být prvním projevem až akutně vzniklá hemoragie se signifikantní život ohrožující krevní ztrátou, nebo mohou udávat perzistující intermitentní spotting různé intenzity [1,2,5,6,8]. Vzhledem k etiologii EMV vázané na RPOC jsou tyto ženy také ohroženy rozvojem infekčních komplikací, sekundárně pak chronickou pánevní bolestí a subfertilitou [5,13].
Hlavní diagnostickou metodou je vaginální USG vyšetření s využitím barevného dopplerovského zobrazování. EMV se na USG prezentuje jako neohraničená, nehomogenní léze s četnými myometrálními a endometriálními cévními lakunami s fokálním či asymetrickým ztluštěním děložní sliznice a svaloviny. S použitím barevného dopplerovského zobrazení pozorujeme barevnou mozaiku rozšířených cév s vysokými maximálními průtokovými rychlostmi (PSV > 20 cm/s), nízkou rezistencí (mean resistive index < 0,3) a nízkou pulzatilitou [12,14]. Kaelin Agten et al vytvořili standardizovaný protokol k měření PSV u EMV. Na základě postupného navyšování frekvence opakování pulzů (PRF – pulse repetition frequency) vyselektovali cévy s největším průtokem a až následně změřili nejvyšší hodnotu PSV [18]. Doplňkovou diagnostickou metodou je pak MR, kde se EMV jeví jako fokální útvar ze serpiginózních struktur s porušením junkční zóny a oblastmi „flow void“, které reprezentují místa s turbulentním prouděním [15]. V laboratorním obraze typicky přetrvává mírná elevace sérové koncentrace hCG a při protrahovaném krvácení se může rozvíjet sekundární hypochromní anemie. V rámci diferenciální diagnostiky je třeba vyloučit gestační trofoblastickou nemoc, choriokarcinom, děložní sarkom či vrozenou AVM.
Terapie by měla být vždy individualizovaná, odvíjející se od příznaků, USG nálezu a reprodukčních plánů jednotlivých pacientek [16]. Závažnost EMV je dle literatury posuzována na základě PSV a od naměřené hodnoty se také částečně odvíjí zvolená terapie [8,17,18]. Léze s PSV < 40 cm/s se považují za málo rizikové a léze s PSV > 60 cm/s za vysoce rizikové stran rozvoje akutní život ohrožující metroragie. U asymptomatických žen bez známek rozvíjející se anemie a s naměřenými hodnotami PSV < 40 cm/s je možné zvolit expektační postup bez nutnosti chirurgické intervence. U těchto pacientek při pravidelných USG kontrolách většinou dochází k samovolné regresi ložiska EMV [1,3,6,12,17]. Timor-Tritsch et al uvádí vymizení fenoménu po 2–15 týdnech od proběhlého těhotenství, Grewal et al po 21–84 dnech [1,12].
U pacientek s prolongovaným krvácením, postupným rozvojem sekundární anemie a perzistujícím ložiskem EMV s PSV > 50–60 cm/s je terapeutickou metodu volby selektivní UAE [1,17,19]. Při přetrvávajícím nálezu RPOC na USG lze pak připojit jejich hysteroskopickou resekci [10], tak jak jsme postupovali v případě naší pacientky. I přesto, že je UAE považována za standardizovanou, bezpečnou a efektivní léčebnou metodu pro zvládnutí různých děložních patologií, nelze opomenout rizika s ní spojená (zejména při nechtěné „mistarget“ embolizaci jiných tkání či orgánů), a to možné tromboembolické komplikace, rozvoj spontánní perforace dělohy či střeva, vzniku píštěle či nekrózy. Diskutovaný je také její potenciální negativní vliv na ovariální rezervu, resp. stav endometriální dutiny a následnou plodnost u žen plánujících graviditu [5,20–26]. Někteří autoři proto před UAE upřednostňují dostatečnou dilataci a následně přesně cílenou kyretáž či jinou instrumentální evakuaci ložiska EMV pod USG kontrolou [5,25]. Literární zdroje nepopisují u využití této metody signifikantně vyšší krevní ztráty, a to v případě první studie byly cíleně selektovány pouze vysoce rizikové pacientky s PSV > 60 cm/s v ložisku EMV [5,27]. Při rozvoji život ohrožujícího nezastavitelného krvácení je poslední léčebnou možností provedení akutní hysterektomie.
Na základě této kazuistiky lze hypotetizovat, zda předchozí traumatizace dělohy, v našem případě cytoredukční výkon a hysteroskopická synechiolýza, nějakým způsobem zvyšuje pravděpodobnost vzniku EMV či ovlivňuje jeho velikost a perzistenci.
Závěr
Závěrem lze shrnout, že nehledě na relativně nízkou incidenci a častou tendenci ke spontánní úpravě zůstává včasné rozpoznání a zejména správný management EMV lékařskou výzvou. Doporučujeme, aby všechny pacientky plánované k chirurgickému řešení RPOC podstoupily dopplerovské USG vyšetření dělohy k vyloučení přítomnosti ložiska EMV, a tím k eliminaci rizika silného krvácení během hysteroskopie či kyretáže bez USG kontroly. Léčebný postup by měl být vždy zcela individualizován s přihlédnutím k symptomatice, USG nálezu a reprodukčním plánům dané ženy. Při verifikaci rizikové varianty EMV by, zejména u graviditu plánujících žen, měly být zváženy adekvátní preventivní opatření krvácení, jako je dělohu ischemizující zákrok (UAE, případně laparoskopická či vaginální okluze děložních tepen). Každá pacientka by také měla být řádně poučena o možnosti rozvoje akutního krvácení a instruována v takovém případě rychle vyhledat profesionální lékařskou pomoc. V případě chirurgického řešení EMV by pak zákrok měl být vždy proveden na operačním sále způsobilém k event. provedení akutní břišní operace, měl by být zajištěn adekvátní operační tým, anesteziologický tým by měl být předem řádně informován o riziku rozvoje rychlé a signifikantní krevní ztráty, měly by být zajištěny krevní deriváty a pacientka by měla být srozuměna s rizikem provedení život zachraňující hysterektomie.
ORCID autorů
A. Richtárová 0000-0001-7635-4858
K. Hlinecká 0000-0002-8452-8333
Z. Lisá 0000-0003-4961-7063
B. Boudová 0000-0003-0444-7160
R. Kocián 0000-0002-5896-4158
J. Kaván 0000-0001-5514-3162
M. Mára 0000-0001-8222-3141
Doručeno/Submitted: 23. 2. 2022
Přijato/Accepted: 24. 3. 2022
MUDr. Adéla Richtárová
Gynekologicko-porodnická klinika
1. LF UK a VFN v Praze
Apolinářská 18
128 00 Praha 2
Zdroje
1. Timor-Tritsch IE, Haynes MC, Monteagudo A et al. Ultrasound diagnosis and management of acquired uterine enhanced myometrial vascularity/arteriovenous malformations. Am J Obstet Gynecol 2016; 214 (6): 731.e1–731.e10. doi: 10.1016/j.ajog.2015.12.024.
2. O‘Rourke-Suchoff D, Benitez S, Higgins MC et al. Diagnosis and treatment of women with radiologic findings suspicious for uterine arteriovenous malformations. J Obstet Gynaecol 2021; 41 (5): 769–773. doi: 10.1080/01443 615.2020.1798905.
3. Timmerman D, Van den Bosch T, Peeraer K et al. Vascular malformations in the uterus: ultrasonographic diagnosis and conservative management. Eur J Obstet Gynecol Reprod Biol 2000; 92 (1): 171–178. doi: 10.1016/s0301-2115 (00) 00 443-7.
4. Groszmann YS, Healy Murphy AL, Benacerraf BR. Diagnosis and management of patients with enhanced myometrial vascularity associated with retained products of conception. Ultrasound Obstet Gynecol 2018; 52 (3): 396–399. doi: 10.1002/uog.18954.
5. Van den Bosch T, Van Schoubroeck D, Timmerman D. Maximum peak systolic velocity and management of highly vascularized retained products of conception. J Ultrasound Med 2015; 34 (9): 1577–1582. doi: 10.7863/ultra.15. 14.10050.
6. Van Schoubroeck D, Van den Bosch T, Scharpe K et al. Prospective evaluation of blood flow in the myometrium and uterine arteries in the puerperium. Ultrasound Obstet Gynecol 2004; 23 (4): 378–381. doi: 10.1002/uog. 963.
7. Van den Bosch T, Van Schoubroeck D, Lu C et al. Color Doppler and gray-scale ultrasound evaluation of the postpartum uterus. Ultrasound Obstet Gynecol 2002; 20 (6): 586–591. doi: 10.1046/j.1469-0705.2002.00851.x.
8. Timmerman D, Wauters J, Van Calenbergh S et al. Color Doppler imaging is a valuable tool for the diagnosis and management of uterine vascular malformations. Ultrasound Obstet Gynecol 2003; 21 (6): 570–577. doi: 10.1002/uog.159.
9. Van den Bosch T, Daemen A, Van Schoubroeck D et al. Occurrence and outcome of residual trophoblastic tissue: a prospective study. J Ultrasound Med 2008; 27 (3): 357–361. doi: 10.7863/jum.2008.27.3.357.
10. Lacheta J. Uterine adenomyosis: pathogenesis, diagnostics, symptomatology and treatment. Ceska Gynekol 2019; 84 (3): 240–246.
11. Alonso Pacheco L, Timmons D, Saad Naguib M et al. Hysteroscopic management of retained products of conception: a single center observational study. Facts Views Vis Obgyn 2019; 11 (3): 217–222.
12. Mulliken JB, Glowacki J. Hemangiomas and vascular malformations in infants and children: a classification based on endothelial characteristics. Plast Reconstr Surg 1982; 69 (3): 412–422. doi: 10.1097/00006534-198203000-00 002.
13. Grewal K, Al-Memar M, Fourie H et al. Natural history of pregnancy-related enhanced myometrial vascularity following miscarriage. Ultrasound Obstet Gynecol 2020; 55 (5): 676–682. doi: 10.1002/uog.21872.
14. Capmas P, Lobersztajn A, Duminil L et al. Operative hysteroscopy for retained products of conception: efficacy and subsequent fertility. J Gynecol Obstet Hum Reprod 2019; 48 (3): 151–154. doi: 10.1016/j.jogoh.2018.12.005.
15. Thakur M, Strug MR, De Paredes JG et al. Ultrasonographic technique to differentiate enhanced myometrial vascularity/arteriovenous malformation from retained products of conception. J Ultrasound 2021; 25 (2): 379–386. doi: 10.1007/s40477-021-00574-y.
16. Picel AC, Koo SJ, Roberts AC. Transcatheter arterial embolization with n-butyl cyanoacrylate for the treatment of acquired uterine vascular malformations. Cardiovasc Intervent Radiol 2016; 39 (8): 1170–1176. doi: 10.1007/ s00270-016-1328-z.
17. O‘Leary M, Sanders AP. Enhanced myometrial vascularity – the time has come for individualized treatment of focal uterine pathology. Fertil Steril 2021; 116 (3): 691–692. doi: 10.1016/ j.fertnstert.2021.06.059.
18. Timor-Tritsch IE, McDermott WM, Monteagudo A et al. Extreme enhanced myometrial vascularity following cesarean scar pregnancy: a new diagnostic entity. J Matern Fetal Neonatal Med 2021; 17 : 1–12. doi: 10.1080/ 14767058. 2021.1897564.
19. Kaelin Agten A, Ringel N, Ramos J et al. Standardization of peak systolic velocity measurement in enhanced myometrial vascularity. Am J Obstet Gynecol 2016; 215 (6): 802–803. doi: 10.1016/j.ajog.2016.08.013.
20. Bazeries P, Paisant-Thouveny F, Yahya S et al. Uterine artery embolization for retained products of conception with marked vascularity: a safe and efficient first-line treatment. Cardiovasc Intervent Radiol 2017; 40 (4): 520–529. doi: 10.1007/s00270-016-1543-7.
21. Berkane N, Moutafoff-Borie C. Impact of previous uterine artery embolization on fertility. Curr Opin Obstet Gynecol 2010; 22 (3): 242–247. doi: 10.1097/GCO.0b013e328338c179.
22. Acharya J, Bancroft K, Lay J. Perforation of transverse colon: a catastrophic complication of uterine artery embolization for fibroids. Cardiovasc Intervent Radiol 2012; 35 (6): 1524–1527. doi: 10.1007/s00270-012-0349-5.
23. Dewdney SB, Mani NB, Zuckerman DA et al. Uteroenteric fistula after uterine artery embolization. Obstet Gynecol 2011; 118 (2 Pt 2): 434–436. doi: 10.1097/AOG.0b013e31821082a3.
24. Maheux-Lacroix S, Lemyre M, Laberge PY et al. Uterine artery embolization complicated by uterine perforation at the site of previous myomectomy. J Minim Invasive Gynecol 2012; 19 (1): 128–130. doi: 10.1016/j.jmig.2011.10.004.
25. Pandey B, Sunanda GV, Crowe P. Enterouterine fistula: a rare and unusual complication of uterine artery embolisation. J Obstet Gynaecol 2012; 32 (1): 32–33. doi: 10.3109/01443 615.2011.615417.
26. Mara M, Horak P, Kubinova K et al. Hysteroscopy after uterine fibroid embolization: evaluation of intrauterine findings in 127 patients. J Obstet Gynaecol Res 2012; 38 (5): 823–831. doi: 10.1111/j.1447-0756.2011.01782.x.
27. Mara M, Maskova J, Fucikova Z et al. Midterm clinical and first reproductive results of a randomized controlled trial comparing uterine fibroid embolization and myomectomy. Cardiovasc Intervent Radiol 2008; 31 (1): 73–85. doi: 10.1007/s00270-007-9195-2.
28. Groszmann YS, Healy Murphy AL et al. Diag - nosis and management of patients with enhanced myometrial vascularity associated with retained products of conception. Ultrasound Obstet Gynecol 2018; 52 (3): 396–399. doi: 10.1002/uog.18954.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicínaČlánek vyšel v časopise
Česká gynekologie

2022 Číslo 4
-
Všechny články tohoto čísla
- Srovnání protokolu zrychleného zotavení s konvenční péčí u pacientů podstupujících urogynekologickou operaci
- Bariéry českých žen v účasti na screeningu karcinomu děložního hrdla
- Gravidita v jizvě po císařském řezu – retrospektivní analýza případů z let 2012–2021
- Vaskularizovaná léze myometria
- Pacientka s primárním adenokarcinomem apendixu metastazujícím do ovaria
- Embolie plodovou vodou – přehled a multicentrická případová analýza
- SARS-CoV-2 placentitida jako příčina intrauterinního úmrtí plodu u pacientky s infekcí covid-19 a probíhajícím HELLP syndromem
- Cefalothorakoomfalopagus – vzácný typ spojených dvojčat z pohledu patologa
- Unilaterálna makrocystická dysplázia a kontralaterálna agenéza obličky u monoamniálneho dvojčaťa
- Dělohu zachovávající operace adenomyózy a její vliv na reprodukční výsledky
- Role elektrické „power“ morcelace v minimálně invazivní gynekologické operativě
- Perforace dělohy při nitroděložních výkonech a její řešení
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Perforace dělohy při nitroděložních výkonech a její řešení
- Dělohu zachovávající operace adenomyózy a její vliv na reprodukční výsledky
- Embolie plodovou vodou – přehled a multicentrická případová analýza
- Gravidita v jizvě po císařském řezu – retrospektivní analýza případů z let 2012–2021
