Ultrazvukový staging karcinomu děložního hrdla – návrh standardního postupu
Ultrasonic staging cervical cancer –a proposal for the standard procedure
Objective:
To develop guidelines for the ultrasound examination of cervical cancer, including a unified ultrasound terminology.
Subject:
Original paper.
Setting:
Gynecological Oncology Center, Department of Obstetrics and Gynecology, Masaryk University and General Faculty Hospital Brno, and Gynecological Oncology Center, Department of Obstetrics and Gynecology, Charles University in Prague – First Faculty of Medicine and General Faculty Hospital Prague.
Subject and method:
The standard diagnostic algo-rithm for examination of cervical cancer in oncogynecology centers in the Czech Republic is based on published studies, own experience (Oncogynecological Center, Department of Gynecology and Obstetrics,1st Medical Faculty, Charles University) and the experiences of a group of ultrasonographers involved in the grant project IGA MZ ČR NT13070 focused on the implementation of an oncogynecological ultrasound into clinical practice. Standard ultrasound examination includes two-dimensional real-time ultrasound examination (sagittal and transverse views). Transrectal or transvaginal ultrasound examination is combined with transabdominal ultrasound. Prerequisites are quality ultrasound equipment, a high frequency microconvex linear probe and abdominal convex and linear probe. The examination is performed by an experienced sonographer (level 2 or 3 according to the recommendations of the Ultrasound division of the Czech Society of Obstetrics and Gynecology and the Czech Society of Ultrasound in Obstetrics and Gynecology). Intravenous administration of contrast material or three-dimensional ultrasound examination do not influence accuracy of the examination and is not a prerequisite.
Conclusion:
Based on the consensus of experienced sonographers and a review of the literature, guidelines were created for ultrasound staging of cervical cancer.
Keywords:
ultrasound, cervical cancer, staging
Autoři:
Vít Weinberger 1
; M. Dvořák 2; L. Haaková 3; L. Hašlík 3; P. Herboltová 4; B. Chaloupková 5; J. Kožnarová 6; B. Kubešová 7; I. Lukáčová 8; R. Marek 9; H. Neumannová 2; R. Peschout 4; V. Přibyl 8; I. Sedláková 10; Martin Smažinka 11
; P. Svobodová 7
; M. Vančo 12; P. Vlasák 11; D. Fischerová 13; Michal Zikán 13
Působiště autorů:
Onkogynekologické centrum, Gynekologicko-porodnická klinika LF MU a FN, Brno
přednosta prof. MUDr. P. Ventruba, DrSc., MBA
1; Onkogynekologické centrum, Gynekologicko-porodnická klinika 1. LF UK a Nemocnice Na Bulovce, Praha, přednosta prof. MUDr. M. Halaška, DrSc.
2; Ústav pro péči o matku a dítě, Praha, ředitel doc. MUDr. J. Feyereisl, CSc.
3; Onkogynekologické centrum, Gynekologicko-porodnické oddělení Nemocnice, Jihlava
primář prof. MUDr. A. Roztočil, CSc.
4; Onkogynekologické centrum, Porodnicko-gynekologické oddělení, Krajská nemocnice T. Bati, a. s., Zlín, primář MUDr. Z. Adamík, Ph. D.
5; Onkogynekologické centrum, Gynekologicko-porodnické odd. Nemocnice České Budějovice a. s.
primář MUDr. P. Sák, PhD.
6; Gynekologicko-porodnická klinika 3. LF UK a FNKV, Praha, přednosta doc. MUDr. E. Kučera, CSc.
7; Onkogynekologické centrum, Porodnicko-gynekologická klinika FN, Ostrava
přednosta doc. MUDr. V. Unzeitig, CSc.
8; Onkogynekologické centrum, Porodnicko-gynekologická klinika LF UP a FN, Olomouc
přednosta prof. MUDr. R. Pilka, Ph. D.
9; Porodnická a gynekologická klinika LF a FN, Hradec Králové, přednosta doc. MUDr. J. Špaček, PhD., IFEPAG.
10; Onkogynekologické centrum, Gynekologicko-porodnická klinika LF UK a FN, Plzeň
přednosta doc. MUDr. Z. Novotný, CSc.
11; Onkogynekologické centrum, Gynekologicko-porodnické odd., Masarykova nemocnice, Ústí nad Labem, přednosta doc. MUDr. T. Binder, CSc.
12; Onkogynekologické centrum, Gynekologicko-porodnická klinika 1. LF UK a VFN, Praha
přednosta prof. MUDr. A. Martan, DrSc.
13
Vyšlo v časopise:
Ceska Gynekol 2014; 79(6): 447-455
Souhrn
Cíl studie:
Cílem práce bylo vytvořit doporučený postup k ultrazvukovému vyšetření zhoubného nádoru děložního hrdla, včetně jednotné ultrazvukové terminologie.
Typ studie:
Původní práce.
Název a sídlo pracoviště:
Onkogynekologické centrum, Gynekologicko-porodnická klinika LF MU a FN Brno a Onkogynekologické centrum, Gynekologicko-porodnická klinika 1. LF UK a VFN, Praha.
Předmět a metoda studie:
Standardní vyšetřovací algoritmus pro vyšetření zhoubného nádoru děložního hrdla v onkogynekologických centrech v České republice vychází z publikovaných prací, vlastních zkušeností pracoviště (Onkogynekologické centrum, Gynekologicko-porodnická klinika 1. LF UK a VFN) a zkušeností skupiny sonografistů, kteří se podílejí na řešení grantového projektu IGA MZ ČR NT13070 zaměřeného na implementaci onkogynekologického ultrazvuku do klinické praxe. Standardní ultrazvukové vyšetření zahrnuje real-time ultrazvukové vyšetření v dvourozměrném obraze (sagitální a transverzální). Transrektální nebo transvaginální ultrazvukové vyšetření je kombinované s transabdominálním ultrazvukem. Podmínkou je kvalitní ultrazvukový přístroj, vysokofrekvenční mikrokonvexní lineární sonda a abdominální konvexní a lineární sonda. Vyšetření je provedeno zkušeným sonografistou (stupeň 2 nebo 3 podle doporučení sekce ultrazvukové diagnostiky ČGPS a České ultrazvukové společnosti v porodnictví a gynekologii). Intravenózní podání kontrastní látky ani třídimenzionální ultrazvuk neovlivní přesnost vyšetření a není podmínkou vyšetření.
Závěr:
Na základě konsenzu zkušených sonografistů a přehledu literatury byl vytvořen doporučený postup pro ultrazvukový staging zhoubného nádoru děložního hrdla.
Klíčová slova:
ultrazvuk, karcinom děložního hrdla, staging
ÚVOD
Karcinom děložního hrdla je třetí nejčastější gynekologickou malignitou a šestým nejčastějším zhoubným nádorem žen v České republice [6]. První vrchol incidence karcinomu děložního hrdla je ve třetí a čtvrté dekádě, druhý v šesté a sedmé dekádě. Často jsou pacientky diagnostikovány v pokročilém stadiu onemocnění. Karcinom děložního hrdla je diagnostikován ve fertilním věku u 44,7 % pacientek, z toho u 13,6 % před 35. rokem života. V této skupině žen je mnoho těch, které ještě nemají splněné svoje reprodukční plány a plánují těhotenství.
Přesné předoperační zjištění rozsahu onemocnění u karcinomu děložního hrdla je zásadní pro naplánování optimální léčebné strategie – primární radikální hysterektomie, neoadjuvantní chemoterapie s následnou radikální onkogynekologickou operací, primární radioterapie nebo pa-liativní chemoterapie. U žen plánujících graviditu nám navíc adekvátní předoperační staging umožní zvažovat a případně zvolit v indikovaných případech fertilitu šetřící chirurgický postup. Přesná znalost velikosti nádoru a uložení tumoru v hrdle dělohy umožňuje onkogynekologovi individualizovat chirurgickou léčbu, přizpůsobit radikalitu chirurgického výkonu dané pacientce, a tím při zachování onkologické bezpečnosti minimalizovat pooperační morbiditu.
Stávající doporučení FIGO (International Federation of Gynecology and Obstetrics) pro stanovení klinického stagingu je nadále založeno na fyzikálním vyšetření pacientky v celkové anestezii provedené zkušeným onkogynekologem [2, 17] . V porovnání s chirurgickým a patologickým stagingem je přesnost klinického vyšetření, které doporučuje FIGO, velmi omezená. Ve stadiu IB podle FIGO je skutečný rozsah onemocnění podhodnocen v 17–32 %, a ve vyšších stadiích až v 67 % případů [5, 12]. Nadhodnocen je až ve 2 ze 3 případů v pokročilém stadiu onemocnění [5, 12]. Hlavním nedostatkem klinického vyšetření je neschopnost přesně určit velikost nádoru, postižení parametrií, pánevní stěny a infiltrovaných lymfatických uzlin [1]. Všechny popsané struktury hrají zásadní roli ve stanovení prognózy pacientky [14].
V poslední revizi FIGO klasifikace karcinomu hrdla dělohy z roku 2009 je přidáno doporučení využít některé zobrazovací metody k určení rozsahu nádoru a k zhodnocení prognostických faktorů, jako jsou velikost tumoru, invaze do parametrií, prorůstání k pánevní stěně, infiltrace spádových i vzdálených lymfatických uzlin a postižení vzdálených orgánů [13]. Obecně akceptovanou metodou k hodnocení lokálního rozsahu onemocnění je magnetická rezonance (MRI – magnetic resonance imaging). Počítačová tomografie (CT – computed tomography) neprokázala vzhledem k nízkému kontrastu s okolními měkkými tkáněmi dostatečnou senzitivitu a specificitu při hodnocení invaze nádoru do parametrií a při hodnocení celkové velikosti nádoru. Může se však uplatnit především v hodnocení uzlinových a vzdálených metastáz. V posledních letech je věnována zvýšená pozornost onkogynekologickému ultrazvukovému vyšetření v předoperačním stagingu karcinomu děložního hrdla. Ultrazvuk je ve srovnání s MRI rychlejší, levnější, dostupnější a nevyžaduje žádnou přípravu pacienta. Prospektivní studie prokázaly, že přesnost transrektálního či transvaginálního ultrazvukového vyšetření je srovnatelná s MRI [8, 9, 19].
Návrh protokolu standardního stagingového vyšetření pacientky s verifikovaným karcinomem děložního hrdla obsahuje tab. 1. Popis metodiky zobrazení jednotlivých kategorií je v textu článku.
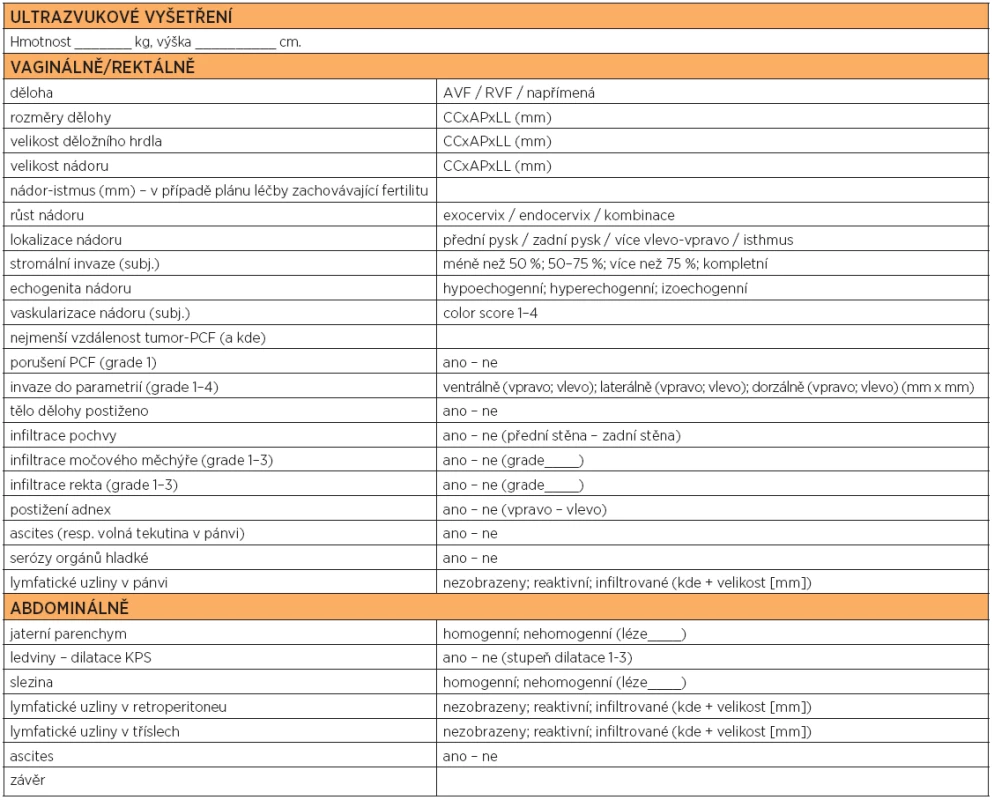
METODIKA ULTRAZVUKOVÉHO STAGINGU
Podmínkou vyšetření je kvalitní přístrojové vybavení a zkušený vyšetřující. Standardní ultrazvukové vyšetření zahrnuje ultrazvukové vyšetření v reálném čase, v dvourozměrném obraze. Transrektální nebo transvaginální ultrazvukové vyšetření je kombinované s transabdominálním ultrazvukem. Podmínkou je ultrazvukový přístroj vyšší třídy, vysokofrekvenční intrakavitální sonda, abdominální konvexní a lineární sonda. Vyšetření je provedeno zkušeným sonografistou (stupeň 2 nebo 3 podle doporučení sekce ultrazvukové diagnostiky ČGPS a České ultrazvukové společnosti v porodnictví a gynekologii) [3]. Intravenózní podání kontrastní látky ani třídimenzionální ultrazvuk neovlivní přesnost vyšetření a není podmínkou vyšetření. Pro ultrazvukové vyšetření není třeba speciální přípravy pacientky, není indikováno očistné klyzma před transrektálním ultrazvukovým vyšetřením ani lačnění před transabdominálním ultrazvukovým vyšetřením. Onkogynekologické ultrazvukové vyšetření provádíme v gynekologické poloze intrakavitální sondou ze zobrazení transvaginálního a/nebo transrektálního. Dosud nebyla publikována práce srovnávající výhody a nevýhody obou přístupů. Zatímco v rámci trans-vaginálního vyšetření je možné lépe posoudit vztah nádoru k poševním klenbám (lze posoudit i při klinickém vyšetření), transrektální přístup minimalizuje riziko krvácení z nádoru při vyšetření a po něm a dovoluje lepší přístup k zobrazení zadních a laterálních parametrií. Intrakavitální vyšetření (transvaginální a/nebo transrektální) je doplněno vyšetřením transabdominální konvexní sondou (event. při podezření na ingvinální lymfadenopatii lineární sondou) v poloze vleže na zádech s nataženými dolními končetinami. Při transabdominálním vyšetření je zobrazena celá břišní dutina včetně parenchymatózních orgánů a retroperitonea, kostofrenické prostory a retroperitoneum malé pánve.
Stanovení velikosti dělohy a děložního hrdla
Transrektální či transvaginální ultrazvukové vyšetření začínáme zjištěním polohy dělohy (AVF, RVF, napřímená) a změřením její velikosti ve třech rozměrech – kranio-kaudální (CC), antero-poste-riorní (AP) a latero-laterální (LL). Velikost děložního hrdla je změřena ve třech rozměrech (CC, AP a LL, mm), přičemž hranice děložního hrdla a těla je určena na základě vstupu uterinních cév do cervixu.
Detekce nádoru
Ultrazvuk je velmi přesná vyšetřovací metoda k zobrazení časného karcinomu děložního hrdla od stadia IB1. Schopnost detekovat histologicky verifikovaný reziduální nádor v hrdle pomocí ultrazvuku je vysoká, pohybuje se mezi 93–94 % [3, 6, 7].
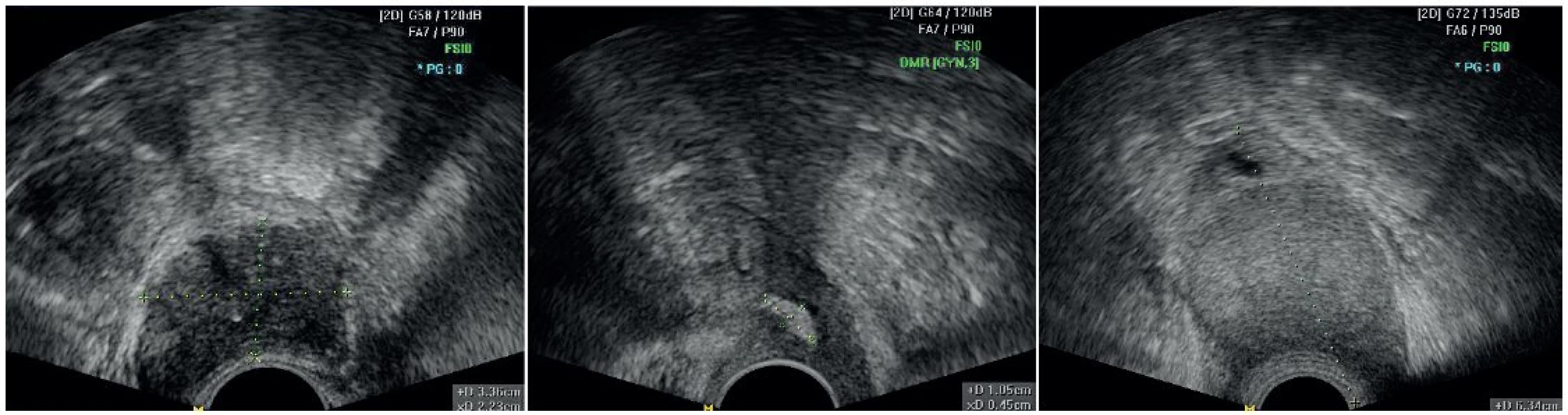
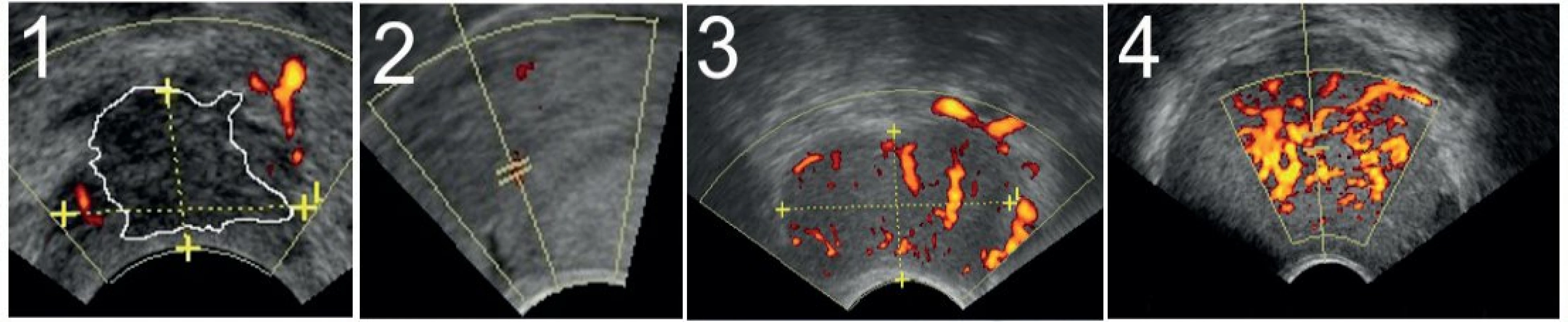
Nádor zobrazujeme na základě změny echogenity a rigidity ve srovnání s okolním stromatem a za využití dopplerovského zobrazení patologické vaskularizace. Je-li nádor přítomen, pak měříme jeho tři rozměry (CC, AP a LL v mm), hodnotíme jeho růst (převážně exocervix/převážně endocervix/kombinace růstu) a určíme jeho lokalizaci (přední pysk, zadní pysk, více vlevo, více vpravo, istmus). Hodnotíme echogenitu tumoru – rozlišujeme tumory hyperechogenní, hypoechogenní a izoechogenní (obr. 1). Dlaždicobuněčný karcinom je v 73 % případů hodnocen jako hypoechogenní a adenokarcinom je v 68 % případů hodnocen jako izoechogenní [7]. Izoechogenní tumory se ultrazvukem velmi obtížně detekují a ohraničují od okolního zdravého stromatu. K přesné vizualizaci a určení hranice tumoru a intaktního stromatu užíváme barevné dopplerovské mapování. Karcinom hrdla dělohy je v 95 % silně prokrven, a díky tomu je v ultrazvukovém obraze dobře patrna oblast patologické (vysoké) vaskularizace oproti okolnímu slabě vaskularizovanému stromatu. Intenzita prokrvení se hodnotí pomocí barevné škály subjektivně ve čtyřech stupních (1 – cévy nejsou přítomny, 2 – minimální perfuze – obtížně zachytíme nějakou cévu, 3 – střední hustota perfuze, 4 – bohatá perfuze) [21] (obr. 2). Nádorové cévy jsou nízkoodporové a lze v nich kvantitativně dopplerovsky měřit indexy rezistence (RI), pulzatility (PI) a indexy rychlosti průtoků TAMAX (průměrný čas k dosažení maximální rychlosti, time avereged maximal velocity) a PSV (vrchol systolické rychlosti, peak systolic velocity), v tuto chvíli nemáme žádná spolehlivá data o možném diagnostickém, prediktivním či prognostickém významu těchto vaskulárních parametrů. Další možností, jak lépe zobrazit izoechogenní tumor, je využití jedinečné vlastnosti ultrazvukového vyšetření – dynamického vyšetření. Intermitentním vyvíjením tlaku na děložní hrdlo prostřednictvím ultrazvukové sondy nebo rukou přes břišní stěnu jsme schopni detekovat špatně zobrazitelné ložisko tumoru, které se manifestuje a ohraničí vůči zdravému okolí jako nepoddajný rigidní úsek cervikální tkáně, který může být při dopplerovském mapování silně prokrvený.
Stanovení kraniálního volného okraje nádoru (plánování fertilitu šetřící léčby)
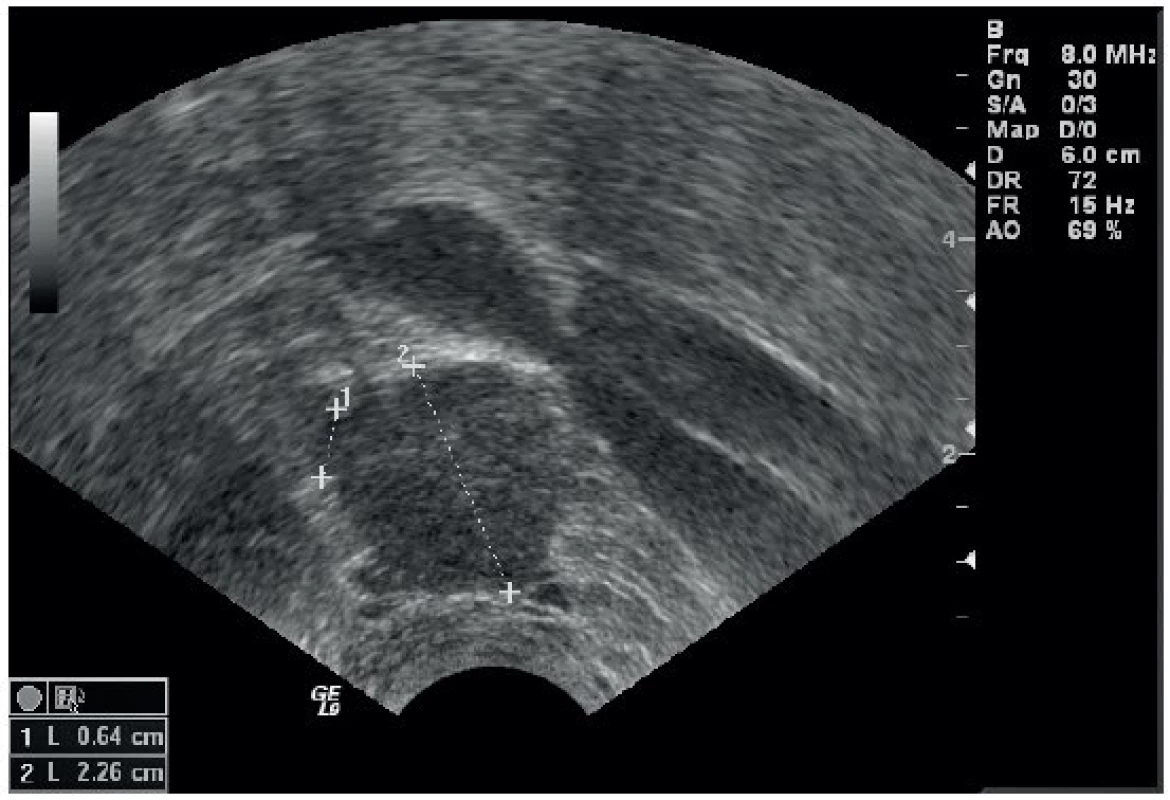
Pro pacientky, u kterých zvažujeme fertilitu zachovávající výkon, je zásadní posouzení vzdálenosti kraniálního okraje tumoru od istmu resp. vnitřní branky (oblast vstupu uterinních cév do dělohy). Pro provedení operace zachovávající fertilitu je nezbytné zachovat alespoň 10 mm délky nepostižené cervikální tkáně [18]. Nutností je přesně detekovat uložení nádoru, který může růst asymetricky v děložním hrdle, a zobrazit nejmenší vzdálenost horního pólu nádoru od vnitřní branky.
Stanovení stromální invaze
Dále hodnotíme rozsah postižení cervikálního stromatu. Podíl stromální invaze může být definován jako částečný (≤ 2/3 nebo > 2/3), nebo jako kompletní. Alternativní možností, jak hodnotit stromální invazi, je změřit nejmenší vzdálenost tumoru od pericervikální fascie (PCF) v místech úponu předních, postranních a zadních parametrií, a to oboustranně. Pericervikální fascie je hy-perechogenní pruh denzní tkáně obklopující děložní hrdlo. Podle rozměrů vzdálenosti tumoru od PCF a znalosti jeho šíření v hrdle dělohy, můžeme předoperačně naplánovat rozsah radikality operování na jednotlivých parametriích. Míra operační radikality (rozsah resekce parametrií) se může stranově lišit podle uložení nádoru v děložním hrdle. Stranově odlišná resekce parametrií může vést ke snížení pooperační morbidity.
Hodnocení invaze do parametrií
Klinické vyšetření parametrií bimanuálně trans-vaginálně či transrektálně je nepřesné a výsledky jsou jak nadhodnocovány, tak podhodnocovány. Celková shoda mezi klinickým stagingem a pooperačním patologickým nálezem pro stadium IB1 je 85,4 %, stadium IB2 77,4 %, stadium IIA 35,3 % a stadium IIB je 20,5 % [15]. Senzitivita vaginálního resp. transrektálního vyšetření ve stanovení invaze do parametrií je 59 %, specificita 74,1 %, negativní prediktivní hodnota 85,9 %, pozitivní prediktivní hodnota 37,4 % a přesnost (accuracy) 70,2 % [15]. Zvláště v případech incipientní infiltrace parametrií, u obézních pacientek nebo u bulky tumorů je klinické vyšetření velmi nepřesné. Tato skutečnost je v příkrém kontrastu s transrektálním nebo transvaginálním ultrazvukovým vyšetřením, které dosahuje přesnosti v hodnocení infiltrace parametrií 98,9 % (MRI dosahuje přesnosti 94,7 %) [9]. V popisu invaze tumoru do parametrií používáme čtyřstupňovou škálu (grading 1–4) [10] (tab. 2).
![Grading infiltrace primárního nádoru do okolích tkání (parametria, močový měchýř, rektum) a grading dilatace kalichopánvičkového systému ledvin (podle [17])](https://www.cs-gynekologie.cz/media/cache/resolve/media_object_image_small/media/image/0fb62aaeecb2d00caa52577680e779ef.png)
Anatomicky jsou přední parametria tvořena lig. vesicouterinum a lig. vesicovaginale, postranní parametria odpovídají tzv. paracervixu, v literatuře ligamentum cardinale, zadní parametria odpovídají ligamentum sacrouterinum a ligamentum sacrovaginale [4, 16]. Hodnocení parametrií podle ultrazvukového vyšetření provádíme standardizovaným způsobem, prohlížíme přední, postranní a zadní parametria na obou stranách v sagitální a transverzální rovině. Pro zobrazení parametrií je nutné si uvědomit, že v kraniokaudálním směru neleží tyto struktury v jedné rovině (zadní parametria jsou uložena kaudálněji, přední parametria kraniálněji). V ultrazvukovém zobrazení hodnotíme porušení PCF, rozsah infiltrace parametrií nádorem a místo (místa), kde k ní dochází. Rozsah infiltrace parametrií (resp. PCF) lze škálovat ve čtyřech stupních. Pokud nádor narušuje PCF, ale nepřesahuje její zevní okraj, hovoříme o stupni 1. Pokud paprsčitě vybíhá vně PCF (do maximální hloubky ≤5 mm), mluvíme o stupni 2. Nodulární infiltrace parametrií, tedy měřitelná prominence většinou hypoechogenní tkáně přes PCF do parametrií, je hodnocena jako stupeň 3. Jako stupeň 4 pak hodnotíme „skip“ metastázy, tj. diskontinuální šíření tumoru do parametrií. Tato ložiska nádoru v parametriích bez spojení s původním tumorem odpovídají viscerálním infiltrovaným paracervikálním uzlinám (obr. 3).
![Staging infiltrace parametrií (podle [17])](https://www.cs-gynekologie.cz/media/cache/resolve/media_object_image_small/media/image/e185f98abeab07c6ba7d908a9f910bda.jpg)
Hodnocení šíření karcinomu hrdla dělohy do močového měchýře
Pro hodnocení šíření nádoru do močového měchýře je nejčastěji používána cystoskopie. Ta však může detekovat pouze bulózní slizniční edém v případě infiltrace submukózy, nebo polypoidní změny na sliznici močového měchýře při kompletním prorůstání (FIGO stadium IVA). Pro rozvahu o způsobu léčby má však význam i detekce prorůstání do subserózní tukové vrstvy nebo dokonce do svaloviny měchýře. Zobrazovací vyšetření tak dává detailnější informaci o rozsahu onemocnění, která umožní lépe popsat lokální rozsah onemocnění.
Za fyziologických podmínek dosáhneme tlakem intrakavitální (transvaginální nebo trans-rektální) sondy na přední poševní stěnu a klenbu pochvy volné posunlivosti močového měchýře vůči děložnímu hrdlu. V případě infiltrace přilehlé svalově-tukové tkáně nedochází ke „klouzání“ orgánů mezi sebou a tkáně jsou vůči sobě rigidní, setrvávají v konstantní neměnné pozici [11]. Infiltraci močového měchýře hodnotíme ve třech stupních [10]. První stupeň představuje postižení povrchové tukové (hyperechogenní) vrstvy obalující močový měchýř. Druhý stupeň je charakterizován infiltrací hypoechogenní vrstvy močového měchýře, která odpovídá svalovině stěny a třetí stupeň je postižení hyperechogenní sliznice močového měchýře, eventuálně s přítomností nádoru protrudujícího do lumen měchýře (viz tab. 2).
Hodnocení šíření karcinomu děložního hrdla do rekta a sigmoidea
Tumor roustoucí dorzálně z hrdla do oblasti rekta poruší nejprve pericervikální fascii, poté zevní povrch střeva, který je hyperechogenní, následně hypoechogenní svalovinu a vrůstá do hyperechogenní sliznice. Nádor se také může šířit do rekta přes pochvu.
Transrektálním přístupem lze hodnotit všechny vrstvy stěny sigmoidea, transvaginálním přístupem lze lépe hodnotit stěnu rekta. Infiltraci stěny rektosigmoidea hodnotíme opět ve třech stupních obdobně jako u močového měchýře. První stupeň představuje postižení povrchové hyperechogenní zevní vrstvy. Druhý stupeň je charakterizován infiltrací hypoechogenní svaloviny a třetí stupeň je postižení hyperechogenní sliznice (viz tab. 2).
Hodnocení pánevních viscerálních a parietálních uzlin
Transvaginální či transrektální přístup umožní detailní hodnocení přítomnosti viscerálních a parietálních uzlin na základě změny jejich architektury a perfuze (obr. 4). Lze zobrazit uzliny paracervikálně a kolem zevních a vnitřních ilických cév až po interilickou bifurkaci a odstup vasa iliaca communia oboustranně [17].
Hodnocení dalších pánevních struktur
Ultrazvukové vyšetření malé pánve se dále zaměřuje na detekci adnex (tuba, ovarium) obou stran. Dále hodnotíme serózy orgánů v malé pánvi, všímáme si eventuálních známek karcinomatózy, která je však velmi vzácná u zhoubného nádoru děložního hrdla (obr. 5). Dokumentujeme přítomnost volné tekutiny v sagitálním řezu mezi dělohou a rektosigmoideem – v Douglasově prostoru.
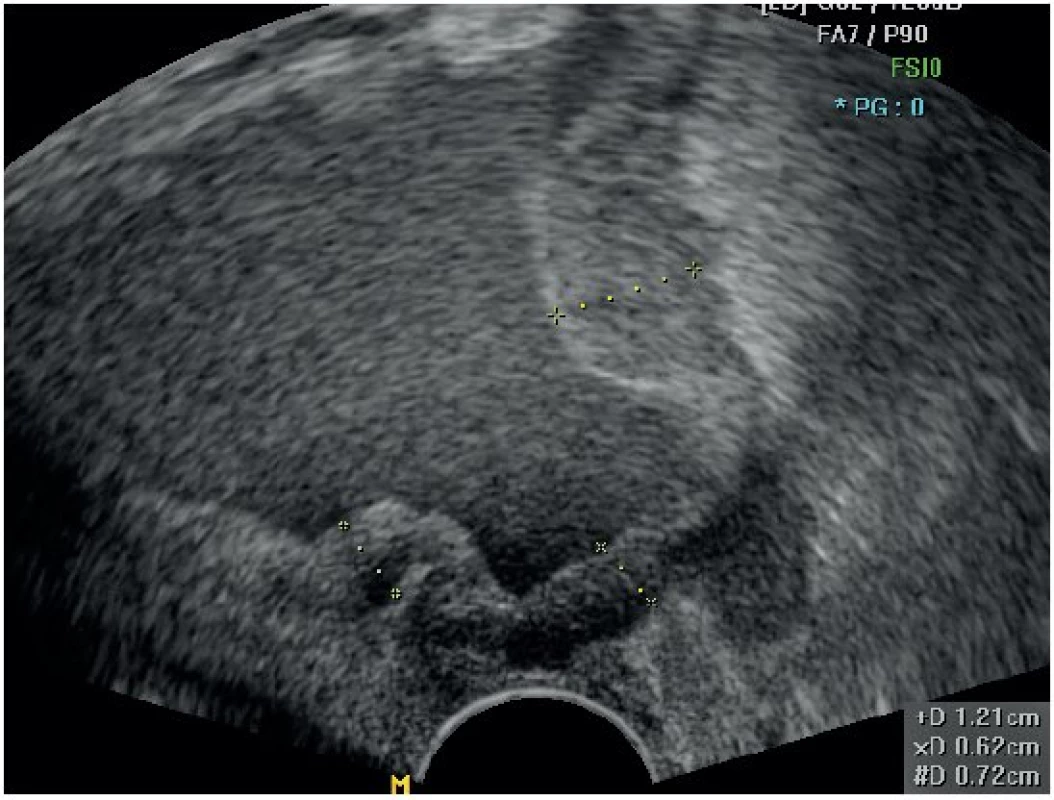
Transabdominální ultrazvukové vyšetření
Břišní sondou dokončujeme vyšetření tříselných uzlin, pánevních uzlin, které by nebylo možné transvaginálním nebo transrektálním přístupem spolehlivě zobrazit (tzn. uzliny uložené ventrálně na externích ilických cévách a kolem společných ilických cév) a věnujeme se zobrazení břišních parietálních (retroperitoneálních) a viscerálních uzlin. Připojujeme vyšetření parenchymatózních orgánů, kde si všímáme eventuální přítomnosti metastáz. Na ledvinách detekujeme případnou dilataci kalichopánvičkového systému (stupeň 1 – dilatace pánvičky, stupeň 2 – dilatace pánvičky a kalichů, stupeň 3 – redukce ledvinného parenchymu) (tab. 2). Dále odkazujeme pro podrobné informace o transabdominálním ultrazvukovém vyšetření v gynekologii na článek, který vyšel v České gynekologii 2011, 76, číslo 4, kde je popsána podrobně metodika i cíl tohoto vyšetření [23].
DISKUSE
Karcinom děložního hrdla zůstává jediným gynekologickým zhoubným tumorem, kde je doporučený staging založen na klinickém vyšetření (FIGO 2009) i přesto, že víme, že existuje zásadní rozdíl v přesnosti klinického a histopatologického stagingu. Přesnost klinického stagingu je sporná, jelikož se opírá o fyzikální vyšetření tumoru v pánvi, které často nález nadhodnocuje či podhodnocuje. Ve stadiu IB–IIB je korelace mezi klinickým stagingem (FIGO) a patologickým stadiem karcinomu slabá (κ = 0,409), shoda je pouze v 53,1 %. V 37,3 % dochází k nadhodnocení nálezu a v 9,7 % podhodnocení [15]. Shoda mezi klinickým vyšetřením a patologickým nálezem pro stadium FIGO I je 78 %, FIGO II 55 % a FIGO III 25 % [22]. Z těchto výše uvedených důvodů je zařazení komplementárních zobrazovacích metod k fyzikálnímu předoperačnímu vyšetření nutností, jelikož je třeba validně zhodnotit prognostické faktory, jako velikost nádoru, hloubku stromální invaze nádoru do hrdla, vzdálenost nádoru od periervikální fascie (PCF), stav parametrií a spádových lymfatických uzlin v pánvi a paraaortálně.
Magnetická rezonance je považována za zlatý standard k posouzení prognostických faktorů karcinomu děložního hrdla od stadia IB1 a více [1]. Výhodou MRI je vysoký tkáňový kontrast, není vliv ionizujícího záření, obraz je ve třech rovinách a je kdykoli znovu revidovatelný pro druhé čtení. Možnost provedení druhého čtení u MRI je argumentem pro objektivizaci výsledku vyšetření. Statický záznam však postrádá výhody dynamičnosti ultrazvukového vyšetření [20]. Zásadní přidanou hodnotou ultrazvukového vyšetření oproti MRI je možnost dynamického vyšetření – vyvinutím tlaku sondou na anatomické struktury je možné zjišťovat jejich pohyblivost vůči okolí, zkoumat jejich elasticitu, či naopak jejich rigiditu. V kombinaci s užitím dopplerovského mapování je možné dosáhnout srovnatelné či vyšší přesnosti než MRI v určení přítomnosti tumoru v hrdle, jeho velikosti, hloubky infiltrace do stromatu hrdla, postižení parametrií [8, 9, 19]. Navíc je ultrazvuk v porovnání s MRI rychlejší, levnější, dostupnější, nevyžaduje žádnou přípravu pacientky, není zde přítomno široké spektrum kontraindikací jako v případě MRI (kochleární implantát, kovové předměty apod.). Ultrazvuk také umožňuje hodnocení nádoru v mnoha rovinách (MRI ve třech rovinách). Přesnost ultrazvuku se během 3D vyšetření již nemění, ale slouží k objektivní archivaci záznamu pro možnost druhého čtení. V neposlední řadě je výhodou ultrazvukového vyšetření to, že může být provedeno zkušeným onkogynekologem nebo sonografistou úzce spolupracujícím s onkogynekologickým týmem, který má znalost o problematice onemocnění a parametrech důležitých pro rozhodování o managementu pacientky.
Kvalita popisu výstupu každé zobrazovací metody závisí na zkušenosti vyšetřujícího lékaře. Dosud neexistuje studie, která by porovnávala reprodukovatelnost výsledků vyšetření sonografistů navzájem. Naší snahou je zavést v České republice jednotnou ultrazvukovou terminologii a algoritmus postupu pro stanovení stagingu karcinomu děložního hrdla.
ZÁVĚR
Pro porozumění mezi lékařem sonografistou a lékařem rozhodujícím o další léčbě pacientky je třeba vytvořit standardní postup ultrazvukového vyšetření pacientek s karcinomem děložního hrdla, který by zohlednil jak specifika ultrazvukového vyšetření, tak parametry nutné pro klinické rozhodování. Tato práce předkládá návrh postupu při ultrazvukovém stagingovém vyšetření.
Práce vznikla za podpory grantu IGA MZ ČR NT 13070 a Univerzity Karlovy, projekty UNCE 204024 a PRVOUK P27/LF1/1.
Podpořeno MZ ČR – RVO (FNBr, 65269705).
korespondující autor
Doc. MUDr. Michal Zikán, Ph.D.
Onkogynekologické centrum
Gynekologicko-porodnická klinika 1. LF UK a VFN
Apolinářská 18
128 00 Praha 2
e-mail: michal.zikan@lf1.cuni.cz
Zdroje
1. Balleyguier, C., Sala, E., Da Cunha, T., et al. Staging of uterine cervical cancer with MRI: guidelines of the European Society of Urogenital Radiology. Eur Radiol, 2011, 21, 5, p. 1102–1110.
2. Benedet, JL., Bender, H., Jones, H., 3rd, et al. FIGO staging classifications and clinical practice guidelines in the management of gynecologic cancers. FIGO Committee on Gynecologic Oncology. Int J Gynaecol Obstet, 2000, 70, 2, p. 209–262.
3. Calda, P., Břešťák, M., Fischerová, D. Doporučený postup: ultrazvukové vyšetření v porodnictví a gynekologii: třístupňová koncepce a certifikace. Actual Gyn, 2011, 3, p. 42–46.
4. Cibula, D., Abu-Rustum, NR., Benedetti-Panici, P., et al. New classification system of radical hysterectomy: emphasis on a three-dimensional anatomic template for parametrial resection. Gynecol Oncol, 2011, 122, 2, p. 264–268.
5. Delgado, G., Bundy, B., Zaino, R., et al. Prospective surgical-pathological study of disease-free interval in patients with stage IB squamous cell carcinoma of the cervix: a Gynecologic Oncology Group study. Gynecol Oncol, 1990, 38, 3, p. 352–357.
6. Dušek, L. Epidemiologie zhoubných nádorů v České republice. 2010.
7. Epstein, E., Di Legge, A., Masback, A., et al. Sonographic characteristics of squamous cell cancer and adenocarcinoma of the uterine cervix. Ultrasound Obstet Gynecol, 2010, 36, 4, p. 512–516.
8. Epstein, E., Testa, A., Gaurilcikas, A., et al. Early-stage cervical cancer: tumor delineation by magnetic resonance imaging and ultrasound – a European multicenter trial. Gynecol Oncol, 2013, 128, 3, p. 449–453.
9. Fischerova, D., Cibula, D., Stenhova, H., et al. Transrectal ultrasound and magnetic resonance imaging in staging of early cervical cancer. Int J Gynecol Cancer, 2008, 18, 4, p. 766–772.
10. Fischerova, D. Ultrasound scanning of the pelvis and abdomen for staging of gynecological tumors: a review. Ultrasound Obstet Gynecol, 2011, 38, 3, p. 246–266.
11. Iwamoto, K., Kigawa, J., Minagawa, Y., et al. Transvaginal ultrasonographic diagnosis of bladder-wall invasion in patients with cervical cancer. Obstet Gynecol, 1994, 83, 2, p. 217–219.
12. Lagasse, LD., Creasman, WT., Shingleton, HM., et al. Results and complications of operative staging in cervical cancer: experience of the Gynecologic Oncology Group. Gynecol Oncol, 1980, 9, 1, p. 90–98.
13. Pecorelli, S. Revised FIGO staging for carcinoma of the vulva, cervix, and endometrium. Int J Gynaecol Obstet, 2009, 105, 2, p. 103–104.
14. Piver, MS., Chung, WS. Prognostic significance of cervical lesion size and pelvic node metastases in cervical carcinoma. Obstet Gynecol, 1975, 46, 5, p. 507–510.
15. Qin, Y., Peng, Z., Lou, J., et al. Discrepancies between clinical staging and pathological findings of operable cervical carcinoma with stage IB–IIB: a retrospective analysis of 818 patients. Aust N Z J Obstet Gynaecol, 2009, 49, 5, p. 542–544.
16. Querleu, D., Morrow, CP. Classification of radical hysterectomy. Lancet Oncol, 2008, 9, 3, p. 297–303.
17. Quinn, MA., Benedet, JL., Odicino, F., et al. Carcinoma of the cervix uteri. FIGO 26th Annual Report on the Results of Treatment in Gynecological Cancer. Int J Gynaecol Obstet, 2006, 95 Suppl 1, p. S43–103.
18. Rob, L., Skapa, P., Robova, H. Fertility-sparing surgery in patients with cervical cancer. Lancet Oncol, 2011, 12, 2, p. 192–200.
19. Testa, AC., Ludovisi, M., Manfredi, R., et al. Transvaginal ultrasonography and magnetic resonance imaging for assessment of presence, size and extent of invasive cervical cancer. Ultrasound Obstet Gynecol, 2009, 34, 3, p. 335–344.
20. Testa, AC., Van Holsbeke, C., Mascilini, F., Timmerman, D. Dynamic and interactive gynecological ultrasound examination. Ultrasound Obstet Gynecol, 2009, 34, 2, p. 225–229.
21. Timmerman, D., Valentin, L., Bourne, TH., et al. Terms, definitions and measurements to describe the sonographic features of adnexal tumors: a consensus opinion from the International Ovarian Tumor Analysis (IOTA) Group. Ultrasound Obstet Gynecol, 2000, 16, 5, p. 500–505.
22. Van Nagell, JR., Jr., Roddick, JW., Jr., Lowin, DM. The staging of cervical cancer: inevitable discrepancies between clinical staging and pathologic findinges. Am J Obstet Gynecol, 1971, 110, 7, p. 973–978.
23. Zikan, M., Fischerova, D., Slama, J., et al. [Transabdominal ultrasound examination in gynecology]. Ces Gynek, 2011, 76, 4, p. 252–257.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicínaČlánek vyšel v časopise
Česká gynekologie

2014 Číslo 6
-
Všechny články tohoto čísla
- Význam kvalitní diagnostiky v péči o pacientky se zhoubnými gynekologickými nádory
- Volba zobrazovací metody v onkogynekologii
- Staging zhoubného nádoru děložního hrdla (stanovení předoperačního rozsahu onemocnění) – přehled výsledků nejnovějších ultrazvukových studií
- Ultrazvukový staging karcinomu děložního hrdla – návrh standardního postupu
- Zhoubný nádor děložního těla – předoperační odlišení nádorů s nízkým a vysokým rizikem metastázování (přehled výsledků nejnovějších ultrazvukových studií)
- Ultrazvukový staging karcinomu endometria – doporučená metodika vyšetření
- Doporučený diagnostický postup u ženy s ovariální cystou nebo nádorem
- Volba vhodné bioptické metody u primárně inoperabilního nebo recidivujícího zhoubného nádoru a metodika bioptického odběru
- Význam screeningu v onkogynekologii
- Metody bezkrevní péče v gynekologii a onkogynekologii
- Rejstříky
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Doporučený diagnostický postup u ženy s ovariální cystou nebo nádorem
- Ultrazvukový staging karcinomu endometria – doporučená metodika vyšetření
- Ultrazvukový staging karcinomu děložního hrdla – návrh standardního postupu
- Zhoubný nádor děložního těla – předoperační odlišení nádorů s nízkým a vysokým rizikem metastázování (přehled výsledků nejnovějších ultrazvukových studií)
