Gastroschíza u plodu – současné možnosti prenatální diagnostiky a následný management
Gastroschisis – current options for prenatal diagnosis and subsequent management
Gastroschisis is a congenital abdominal wall defect characterized by the eventration of bowel loops through a right-sided paraumbilical opening. Prenatal detection of gastroschisis is generally straightforward due to advanced ultrasound techniques, and it is essential for optimizing both prenatal care and subsequent management. The prognosis for this condition is generally favorable, with positive long-term outcomes for most children. However, 10–15% of cases may follow a complicated course with an elevated risk of neonatal mortality or significant morbidity. Early detection enables effective monitoring of fetal development, risk assessment for potential complications, and risk minimization by planning childbirth at a tertiary center equipped with intensive neonatal care and the possibility of prompt surgical intervention.
Keywords:
Prognosis – prenatal diagnosis – ultrasound diagnosis – gastroschisis – omphalocele – abdominal wall defects
Authors:
Anna Jouzová 1,2
; Lenka Kučerová 1,2; Romana Gerychová 1,2; Jakub Turek 2,3
; Ondřej Marek 2,3; Martin Jouza 2,4
; L. Hruban 1,2,5
Authors‘ workplace:
Gynekologicko-porodnická klinika FN Brno
1; Lékařská fakulta, MU, Brno
2; Klinika dětské chirurgie, ortopedie a traumatologie FN Brno
3; Pediatrická klinika FN Brno
4; Ústav zdravotních věd, LF MU, Brno
5
Published in:
Ceska Gynekol 2025; 90(3): 247-253
Category:
doi:
https://doi.org/10.48095/cccg2025247
Overview
Gastroschíza je vrozená rozštěpová vada břišní stěny charakterizovaná eventerací střevních kliček obvykle pravostranným paraumbilikálním defektem. Prenatální detekce gastroschízy není díky pokročilým ultrazvukovým metodám obtížná. Časný záchyt vady je klíčový pro optimalizaci prenatální péče i následný management. Prognóza této vady je dobrá a dlouhodobý stav dětí je příznivý, nicméně 10–15 % případů má komplikovaný průběh s vysokým rizikem neonatální mortality či závažné morbidity. Časný záchyt umožňuje efektivní monitorování vývoje plodu, posouzení rizika rozvoje komplikací a jejich minimalizace plánováním porodu v perinatologickém centru s dostupností intenzivní neonatologické péče a možností okamžité chirurgické intervence.
Klíčová slova:
prognóza – prenatální diagnostika – ultrazvuková diagnostika – gastroschíza – omfalokéla – rozštěpy břišní stěny
Úvod
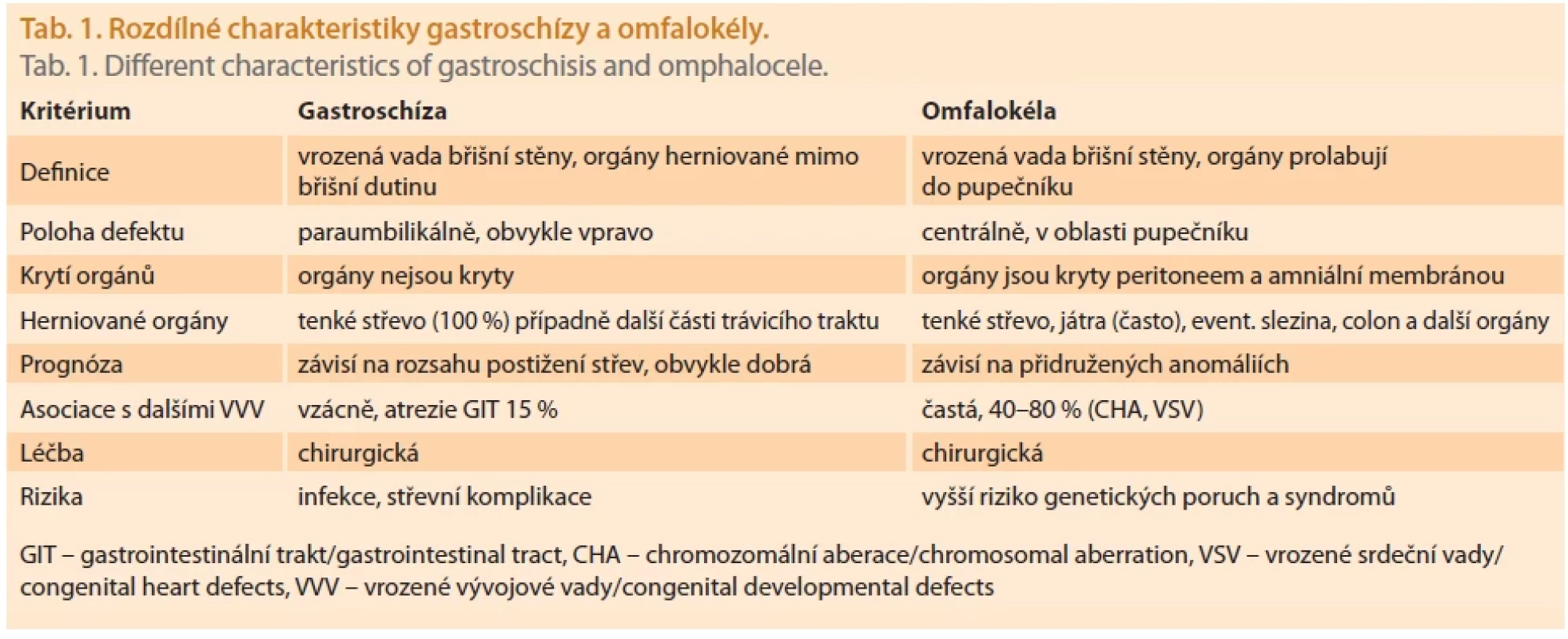
Gastroschíza (GS) je relativně častou vrozenou vývojovou vadou plodu s uváděnou incidencí okolo 2,8–4,3/10 000 porodů [1,2]. Patří do skupiny tzv. ventrálních defektů břišní stěny (AWDs – abdominal wall defects) a spolu s omfalokélou představuje nejčastější typ těchto rozštěpových vad. Prenatální detekce a vzájemné odlišení gastroschízy a omfalokély je klíčové, protože každá z nich má odlišný patofyziologický základ a vyžaduje specifický klinický přístup a léčebnou strategii [3].
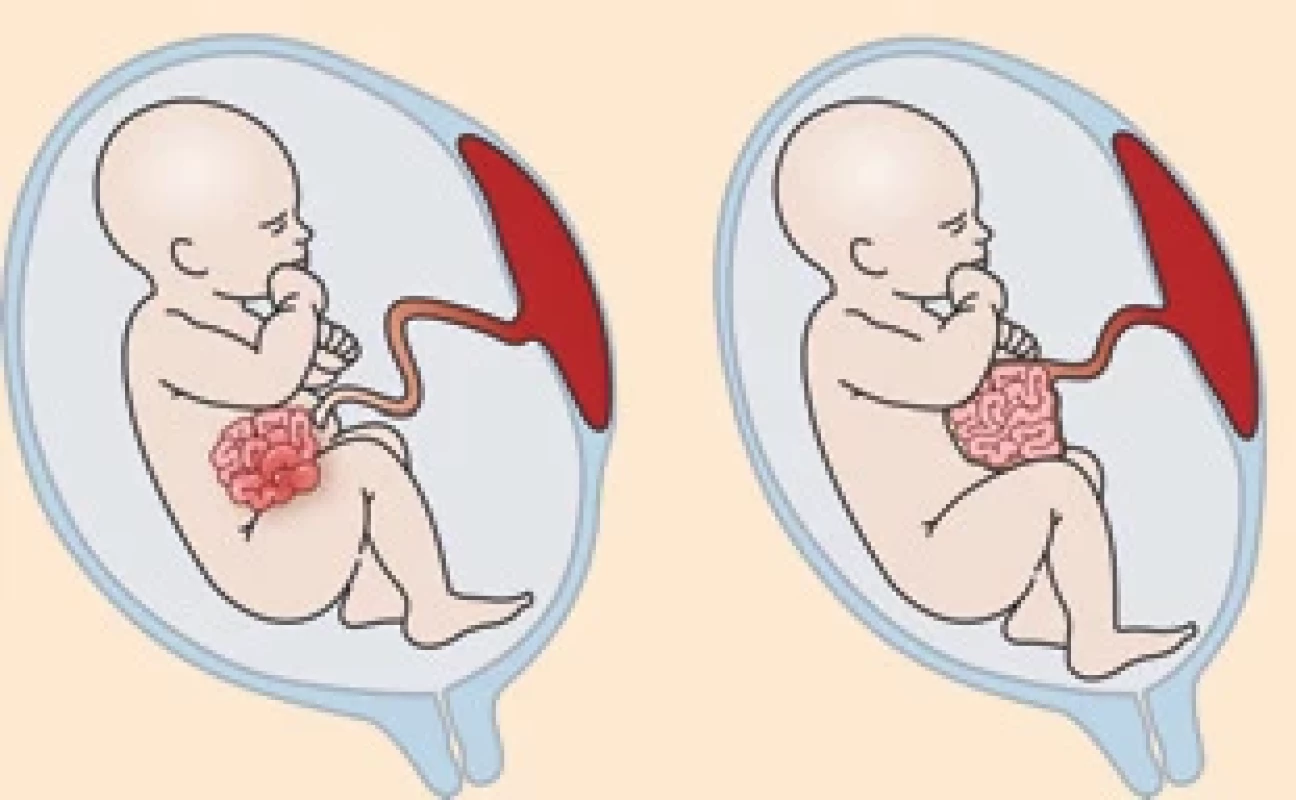
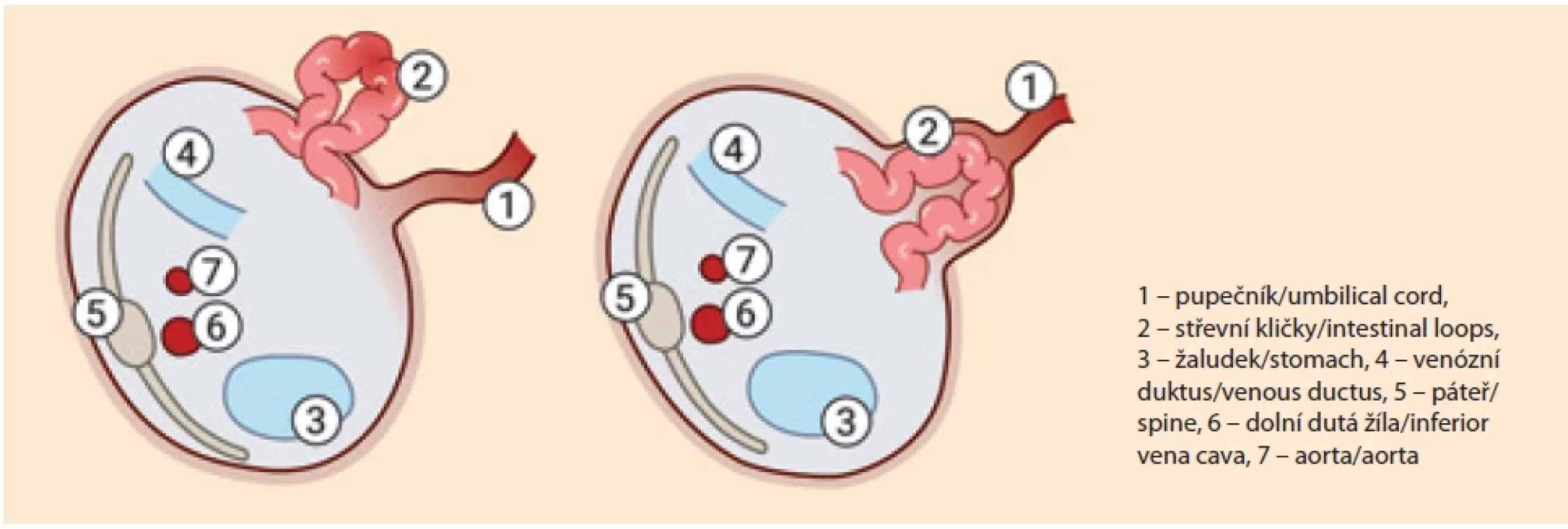
Gastroschíza je charakterizována obvykle pravostranným paraumbilikálním defektem přední břišní stěny s eventerací střevních kliček, které jsou volně uloženy v amniálním prostředí. Vada zpravidla není spojena s chromozomálními nebo dalšími strukturálními malformacemi, s výjimkou intestinálních atrezií, které se vyskytují přibližně v 10 % případů [4–6]. Naproti tomu u omfalokély dochází k herniaci břišních orgánů skrze umbilikální otvor, a tyto orgány jsou tudíž kryty peritoneem spolu s amniální membránou a chráněny před přímými účinky plodové vody (amniotoxicitou) [4,7]. Omfalokéla se často vyskytuje v asociaci s dalšími vrozenými vadami (30–60 %), nejčastěji chromozomálními aberacemi (např. trizomie 13, 18 a 21) či kardiovaskulárními anomáliemi, a prognóza je tak přímo závislá na přítomnosti těchto přidružených anomálií (tab. 1, obr. 1, 2).
Epidemiologie
Incidence GS vykazuje v posledních dvou desetiletích strmý vzestup [1,2,7,8]. Příčina tohoto nárůstu není zcela objasněna, trend je ale charakteristický napříč národními studiemi a registry. V úvahu přichází zlepšení metod prenatální diagnostiky, enviromentální vlivy či změna v chování žen. Přesnou příčinu tohoto nárůstu ale neznáme [4,9–12]. Gastroschíza se vyskytuje ve stejném poměru u chlapců i dívek [13].
Poslední data z registru EUROCAT (European Network of Population-Based Registries for the Epidemiological Surveillance of Congenital Anomalies), který čerpá z národních registrů, uvádí za rok 2022 incidenci GS 1,71/10 000 těhotenství, z toho 0,2/10 000 ukončení na základě žádosti rodičů [2].
V ČR je udávaná incidence 3,09/ 10 000 narozených dětí, z toho 2,19/ 10 000 je zachyceno prenatálně (70,9 %) [14]. Národní registr vrozených vad (NRVV) Ústavu zdravotnické informaticky a statistiky ČR (ÚZIS) uvádí za rok 2023 celkem 18 prenatálně zachycených případů GS, z nichž 15 skončilo abortem (spontánně či na žádost rodičů), a dále 10 dětí narozených s touto diagnózou. Problém je, že pokud se v národním registru nevyskytne záznam o vrozené vadě, neznamená to, že se vrozená vada nevyskytla, ale pouze to, že nebyla do registru nahlášena. Obecně se předpokládá, že počty prenatálně diagnostikovaných vrozených vad v NRVV jsou podhodnocené [15].
Rizikové faktory
Mezi rizikové skupiny patří kuřačky, uživatelky drog či některých léků v I. trimestru (ibuprofen, některá nesteroidní antiflogistika, kontraceptiva), či matky vystavené genitourinárním infekcím na počátku gravidity [1,16]. Specifickou a významnou rizikovou skupinu představují matky mladší 20 let, u nichž je popisován téměř 7krát vyšší výskyt ve srovnání se skupinou starších rodiček, což vyplývá z výsledků rozsáhlých analýz a národních registrů [9,11,17]. Pravděpodobným vysvětlením tohoto jevu by mohl být životní styl mladých rodiček, nicméně jednoznačná evidence není dosud k dispozici [18].
Etiopatogeneze
Gastroschíza se vyvíjí v rané fázi embryonálního vývoje, mezi 5. a 10. týdnem těhotenství. Patogeneze není jednoznačně objasněna a právě z důvodu narůstající incidence je předmětem mnoha diskuzí. Existuje řada hypotéz vzniku jako např. selhání diferenciace embryonálního mezenchymu nebo abnormální involuce pravé umbilikální vény. Další teorie mluví o možných vlivech genového polymorfizmu, estrogenních protrombotických disruptorů, mateřské imunitní odpovědi či enviromentálních vlivech (užívání některých léků, kouření, abúzus alkoholu apod.) [1,7,19–22]. V poslední době je často uváděna teorie chybného uzávěru pupečníkového prstence a ruptura amnia v důsledku multifaktoriálního oxidativního poškození [23].
Klasifikace
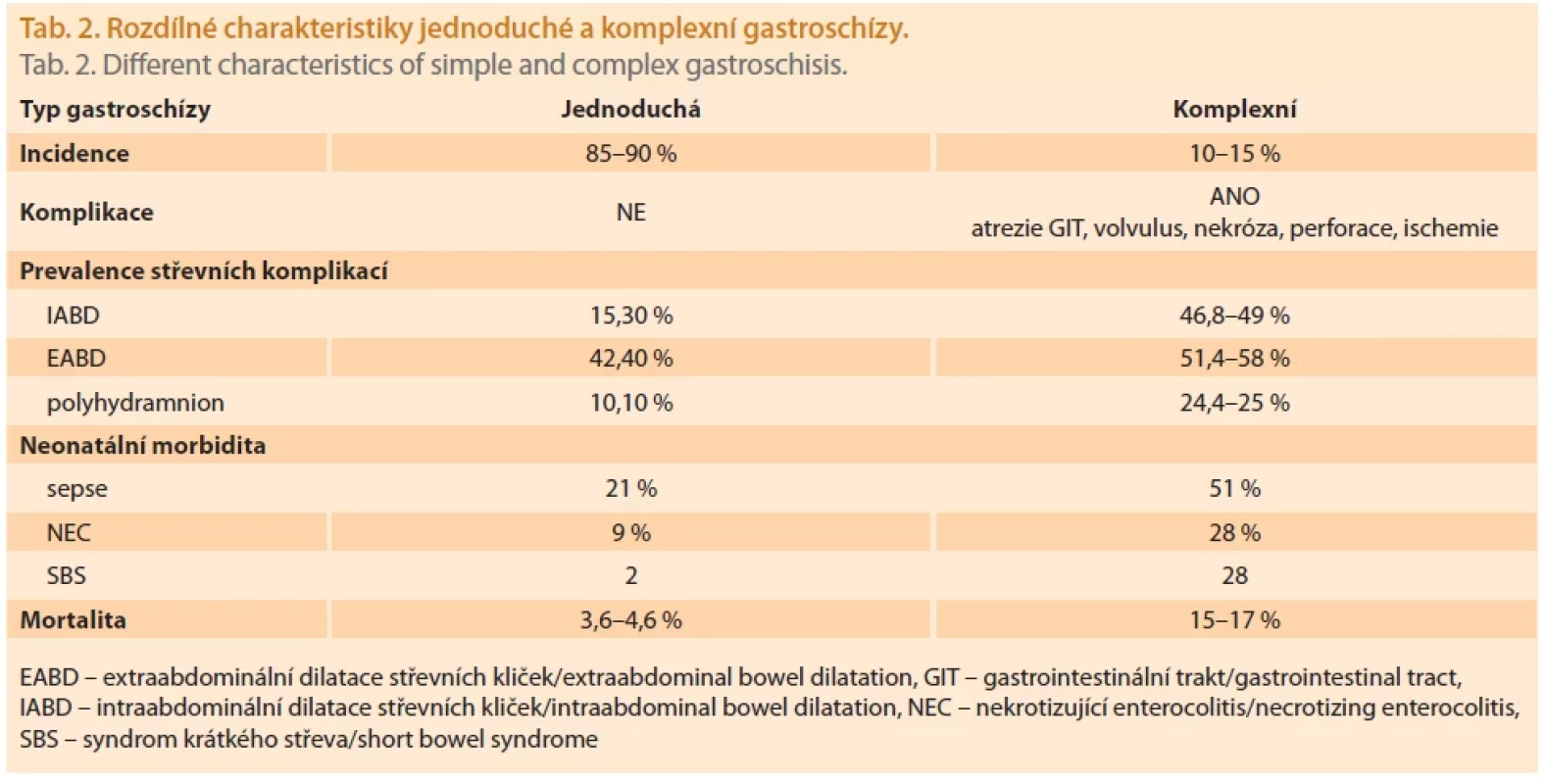
Klinicko-terapeutický význam má rozdělení GS na jednoduchou a komplexní na základě rozsahu a závažnosti postižení střevních kliček. Spolehlivě je možné stav hodnotit až postnatálně. V případě jednoduché GS je střevo v dobrém stavu bez přidružených primárních patologií. Komplexní GS je naopak typ spojený s vrozenými střevními komplikacemi v podobě atrezie, perforace, ischemie, nekrózy nebo volvulu [18] a je spojena s významně vyšším rizikem mortality (15–17 vs. 4 %) i neonatální morbidity (sepse, nekrotizující enterokolitida, syndrom krátkého střeva, pozdní zahájení enterální výživy, délka hospitalizace) (tab. 2) [7,24–27].
Vzácným a obávaným subtypem je uzavírající se (vanishing) GS. Jedná se o komplexní typ s atrezií střeva, při níž dochází ke spontánnímu uzávěru defektu břišní stěny s následnou strangulací střevních kliček. To vede ke vzniku závažných střevních komplikací (nekróza, ischemie) s mortalitou okolo 70 % [7,28,29].
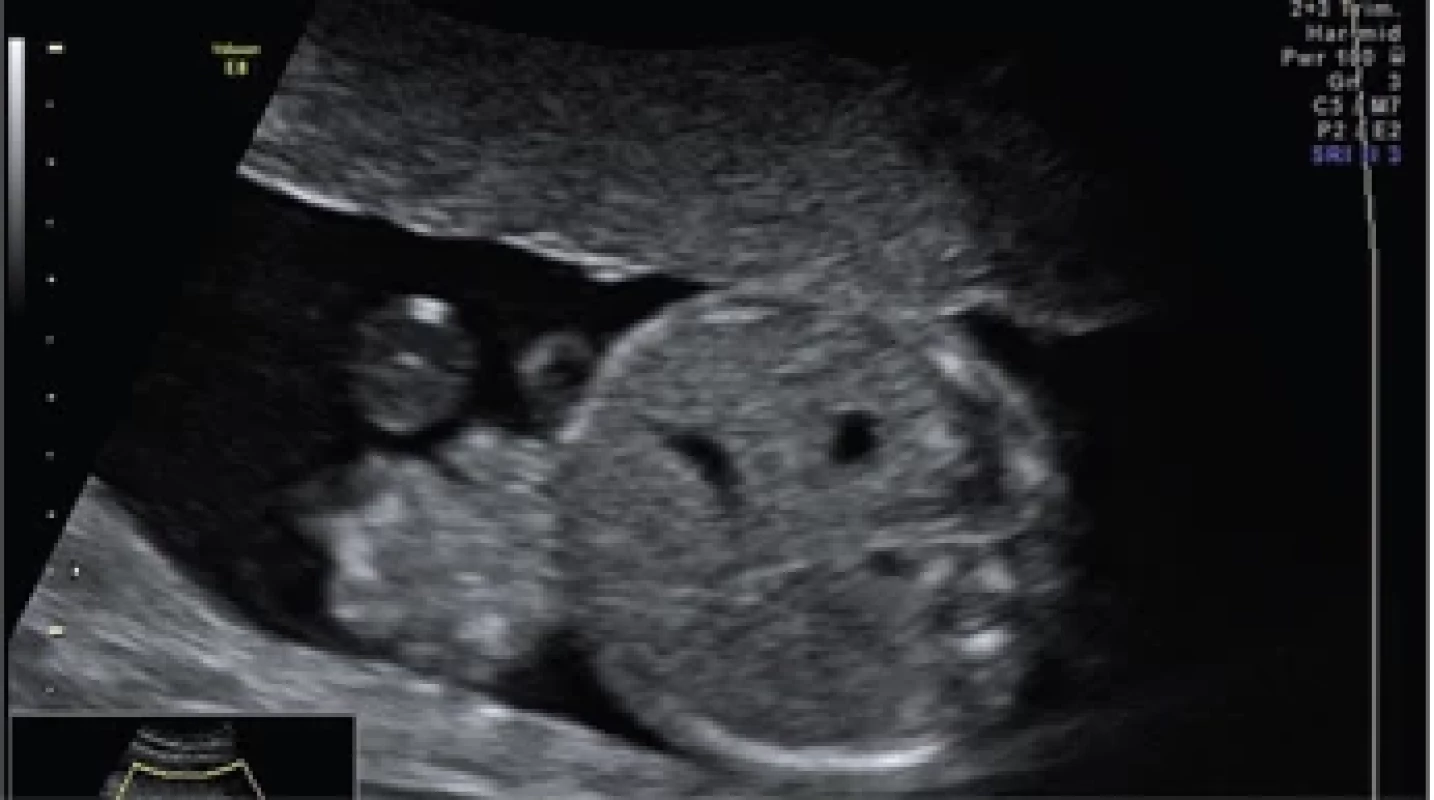
of intestinal loops through a paraumbilical defect.
Prenatální diagnostika
Úspěšnost záchytu GS je v rámci prenatální diagnostiky vysoká. Dle recentní metaanalýzy dosahuje záchyt mezi 11. a 14. týdnem až 96 % [8]. V ČR přesné údaje nemáme k dispozici, dle Gregora a Šípka nedosahuje prenatální záchyt ani tří čtvrtin případů a NRVV poskytuje jen velmi omezená data [14,15].
Typický ultrazvukový nález představuje relativně malý defekt břišní stěny (obvykle 2–5 cm ve II. a III. trimestru) nacházející se vpravo vedle úponu pupečníku, s výhřezem nitrobřišních orgánů. Nejčastěji se mimo dutinu břišní plodu nachází pouze střevní kličky, avšak součástí eventerovaného obsahu mohou být i játra a žaludek, výjimečně jiné intraabdominální orgány. Žaludek bývá často deviován ze své obvyklé polohy (obr. 1–3) [18].
Pomocí ultrazvuku lze dále popsat morfologii střevních kliček – dilataci a její rozsah (intraabdominální, extraabdominální), tloušťku střevní stěny a její vaskularizaci, výhřez dalších orgánů, jako je žaludek či játra, který je přítomen přibližně u 10–15 % případů [30]. Dále je nutné vyloučení přidružených komplikací, jako je růstová restrikce plodu (FGR – fetal growth restriction), odchylky v množství plodové vody či výskyt přidružených anomálií u plodu (tab. 2).
Posouzení morfologie střevních kliček je předmětem mnoha diskuzí, protože jejich stav při narození je klíčovým prognostickým faktorem novorozenecké morbidity. Z tohoto důvodu je proto namístě hledání ultrazvukových markerů, které by co nejspolehlivěji predikovaly komplexní GS, která je zatížena výrazně vyšší morbiditou a mortalitou.
Intraabdominální dilatace střevních kliček (IABD – intraabdominal bowel dilatation) je přítomna u 46,8 % plodů s komplexní GS a u 15,3 % plodů s jednoduchou GS [27]. Riziko komplexní GS oproti plodům bez IABD je dle recentních metaanalýz 3–5,5krát vyšší, zároveň je IABD nezávislým prediktorem vyšší mortality, nekrotizující enterokolitidy (NEC – necrotising enterocolitis), syndromu krátkého střeva (SBS – short bowel syndrome), pozdního zahájení perorálního příjmu a delší hospitalizace (LOS – lenght of stay) [31,32].
Extraabdominální dilatace střevních kliček (EABD – extraabdominal bowel dilatation) je popisována u 51,4 % plodů s komplexní GS a u 42,4 % plodů se simplexní GS [27]. Riziko nálezu komplexní GS oproti plodům bez EABD je 1,55–2,27krát vyšší, nicméně nebyl zjištěn významný rozdíl mezi skupinami EABD a non-EABD v postnatální mortalitě, SBS a LOS [31,32].
Je třeba zmínit, že referenční hodnoty dilatace střevních kliček se napříč studiemi značně liší, dle dosud nejrozsáhlejší metaanalýzy Sun et al. (36 studií, n = 3 054) se hodnoty dilatace střevní kličky pohybovaly v širokém rozmezí mezi 6 a 25 mm (medián 10 mm) (tab. 2).
Lze předpokládat, že dilatace střev (IABD i EABD) ≥ 10 mm mezi 20. a 22. týdnem má nejvyšší specificitu (96 %) pro predikci komplexní GS a spolu s nálezem polyhydramnia jsou nejcitlivějšími markery nepříznivého postnatálního outcome [31,32].
Množství plodové vody popisujeme pomocí měření nejhlubšího sloupce (SDP – single deepest pocket). Nález polyhydramnia (SDP > 8 cm) je častější u plodů s komplexní GS (RR 3,82) a často predikuje zejména přítomnost atrezie střeva [32]. Naopak snížené množství plodové vody – oligohydramnion (SDP ≤ 2 cm) může být spojeno s fetální růstovou restrikcí.
Tloušťka střevní stěny, která dosahuje při měření hodnotu > 3 mm (jako nejčastější cut-off hodnota značící prosáknutí, edém), nebyla studiemi prokázána jako statisticky významná pro predikci komplikací a zhoršení neonatálního výsledku [27,33,34].
Růst plodu patří mezi další sledované markery ve vztahu k predikci nepříznivých výsledků těhotenství. Některé studie uvádí poměrně vysoké procento plodů zatížených růstovou restrikcí (30–60 %), ovšem většina spadá do kategorie SGA (small for gestational age) [35–37]. Tento jev je vysvětlován jednak možnou ztrátou tekutin a bílkovin přes obnažené střevo, ale zejména systematickým podměřováním parametru AC (abdominal circumference / obvod břicha) [1]. Dle metaanalýzy Ferreiry et al. z roku 2024 se incidence FGR pohybuje pouze okolo 4,43 % a ve vztahu k prognóze GS a predikci komplexní GS nehraje zásadní roli [27].
Fetální terapie
S rozvojem prenatální diagnostiky je snaha o zavedení postupů, které by ve vybraných případech zlepšovaly postnatální výsledky metodami fetální terapie.
Využití výměny plodové vody (amnioexchange) k nahrazení potenciálně toxického amniálního prostředí se obecně nedoporučuje. Dosavadní studie neprokázaly významný přínos a některé musely být dokonce předčasně ukončeny kvůli riziku ohrožení plodu a horším výsledkům v exponované skupině [38].
Současný výzkum se ubírá směrem miniinvazivní fetoskopie, kde by se pomocí operačních technik in utero (reparace defektu, překrytí prolabovaných orgánů) mohlo zamezit expozici střevních kliček amniálnímu prostředí. Studie probíhající na animálních modelech řeší otázku optimální techniky, nástrojového vybavení a materiálu. Výzkum též naráží na etické aspekty [26,31,39].
Péče v období porodu
Při podezření na vrozenou rozštěpovou vadu břišní stěny by měla být prenatální péče a porod směřovány na pracoviště s možností intenzivní neonatologické péče a návazností na dětskou chirurgii. Porod mimo perinatologické centrum intenzivní péče (PCIP) je významným faktorem navyšujícím riziko následných komplikací u novorozenců s GS (zejm. čas zahájení a délka enterální výživy, délka hospitalizace) [40]. Při porodu by měl být přítomen neonatologický tým intenzivní péče. Ihned po porodu by mělo být exponované střevo překryto sterilním fyziologickým krytím a nepropustnou bariérou, aby se minimalizovalo riziko infekce a ztráty tekutin, které jsou v prvních 24 hod života 2,5krát vyšší než u zdravého novorozence [41]. Další poporodní péče zahrnuje neodkladné zavedení nasogastrické sondy k dekompresi žaludku, a tím k zabránění možné aspirace s fatálními následky [42,43].
Velkou kontroverzí zůstává otázka časování porodu. Mezi uváděné výhody elektivního předčasného porodu patří snížení délky expozice obnažených střevních kliček účinkům intraamniálního prostředí (plodové vody), která vede ke vzniku sterilního zánětu (aseptické peritonitidy) [20]. Rizika plánovaného předčasného porodu však zahrnují komplikace spojené s pozdní prematuritou a mohou také významně ovlivnit poporodní průběh u novorozence, dále zatíženého operačním výkonem. Původní předpoklad vycházel z teorie, že délka expozice plodové vodě přímo ovlivňuje funkci a stav střeva, a je tedy opodstatněné směřovat porod do období okolo 34.–35. týdne gravidity. Ze současných poznatků vyplývá, že ačkoli působení plodové vody vede ke vzniku edému, hypomotilitě a absorbční dysfunkci střeva, vztah mezi délkou expozice a mírou komplikací není přímý a je ovlivněn mnoha dalšími faktory. Význam má působení různých typů buněk v různých fázích aktivace, cytokiny, zvýšená exprese miRNA. Svou roli sehrává také variabilita ve složení plodové vody a řada dalších faktorů. Možnosti predikce střevní funkce a její vztah k postnatálnímu a pooperačnímu nálezu ve spojitosti s průběhem zánětlivého procesu je proto stále předmětem výzkumu [44–47].
Recentní rozsáhlý systematický přehled a metaanalýza 28 studií (Slidell et al. 2024; n = 8 250) uvádí relativně konzistentní poznatky. Porod před 34. týdnem těhotenství vede k závažným komplikacím pro novorozence (zejm. nutnost mechanické ventilace, závislost na parenterální výživě, riziko infekce vč. sepse, délka hospitalizace apod.) a porod po 37. týdnu těhotenství je spojen se signifikantně lepšími výsledky [24]. V plánování perinatálního managementu je nutno brát v potaz, že spontánní předčasný porod (před 37. týdnem těhotenství) nastává ve 30–60 % těhotenství s GS [42,43,48].
Stanovení optimálního způsobu vedení porodu zůstává nadále kontroverzní. Dle řady studií není vaginální porod spojený s vyšším rizikem komplikací pro novorozence. Přesto je často volen porod císařským řezem zejména pro možnost optimálního načasování následné operační korekce defektu. Elektivní výkon představuje řadu výhod spojených s naplánováním a organizací multidisciplinárního týmu (perinatolog, neonatolog, anesteziolog, chirurgický tým a vybavení). Někteří autoři doporučují volit operační porod pouze z důvodu porodnických indikací a obecně se způsob porodu v jednotlivých centrech velmi liší [1,24,27,49–51].
Z výše uvedeného tedy vyplývá, že elektivní porod po 37. týdnu těhotenství v perinatologickém centru je nejvýhodnější variantou minimalizující riziko následných komplikací. Způsob porodu by měl být volen individuálně.
Postnatální terapie
Primární léčbu GS u novorozence představuje operační terapie. Většinou jsou zvažovány tři způsoby chirurgického řešení:
- primární fasciální uzávěr;
- umístění sila s postupnou redukcí a opožděným uzávěrem;
- pupeční uzávěr bez stehu.
Volba konkrétní techniky je ovlivněna velikostí defektu, stavem a vzhledem střev a hemodynamickou stabilitou novorozence. Na operačním sále je gastrointestinální trakt dekomprimován zavedením žaludeční sondy a odsátím žaludečního obsahu, případně i evakuací smolky přes konečník. Velikost defektu se zpravidla zvětšuje o 1–2 cm, aby se minimalizovalo trauma střeva, a pokud je možné všechny vyhřezlé střevní kličky reponovat bez výrazného útlaku nitrobřišních orgánů či elevace bránice vedoucí k dechové insuficienci, je defekt břišní stěny uzavřen při primární operaci (tzv. primární plastika, cca v 70 % případů). Pokud jsou střevní kličky výrazně edematózní a není možné je bezpečně vrátit do dutiny břišní, uzavírá se břišní stěna dočasně s použitím syntetického materiálu – tzv. SILO technika. Po ústupu edému a návratu střevních kliček (obvykle po 1–2 týdnech) je defekt uzavřen definitivně. Při současné atrezii střeva nebo jeho pokročilém poškození je nutné poškozenou část střeva resekovat a provést anastomózu. Pooperační management zahrnuje co nejčasnější zahájení enterální výživy [24,52,53].
Prognóza
Prognóza novorozenců s GS je obecně velmi dobrá, míra přežití přesahuje 95 %. Riziko časné perinatální ztráty a intrauterinního úmrtí se pohybuje v desetinách procenta (0,34 %), po 36. týdnu okolo 1,28 %, neonatální mortalita se uvádí okolo 5 % [27,54,55]. Dlouhodobé komplikace se týkají zejména komplexní GS a zahrnují většinou gastrointestinální dysfunkci (abnormální střevní motilita, gastroezofageální reflux, hiátová hernie) [1]. Některé studie také uvádějí nižší růstový potenciál u dětí s GS [56,57], tento deficit se ale v průběhu vývoje v kojeneckém a dětském věku postupně normalizuje. Někteří autoři popisují obstrukční komplikace způsobené pooperačním adhezivním syndromem s nutností reoperace, převážně v prvním roce života [58]. Relativně velké procento dětí (až 40 %) pak může trpět opakovanou abdominální bolestí, často s nutností hospitalizace [59,60]. Mezi lokální dlouhodobé chirurgické komplikace patří vznik umbilikální hernie či nutnost plastické revize abdominální jizvy [59].
Závěr
Prenatální ultrazvuková diagnostika umožňuje téměř stoprocentní záchyt případů plodů s GS, ačkoli data reflektující záchyt v ČR jsou omezená. Díky pokročilým technikám jsme schopni odhadnout případy komplexní GS, které představují cca 15 % případů a jsou zatíženy vyšší mortalitou a morbiditou. Význam jednotlivých ultrazvukových markerů je omezený, ale nález dilatace střevních kliček ≥ 10 mm mezi 20. a 22. týdnem v kombinaci s polyhydramniem lze využít v predikci možného komplikovaného průběhu. Konzultace těhotenství s GS by měla být vedena fetomaternálním specialistou s možností identifikovat potenciálně vysoce rizikové případy. Na druhou stranu, v případě jednoduchých, méně rizikových GS je důležité těhotné zdůraznit velmi dobrou prognózu této vrozené vývojové vady. Těhotenství by mělo být sledováno ve specializovaných ambulancích a porod směřován do perinatologického centra s adekvátní poporodní péčí a možností včasné chirurgické intervence.
Sources
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicineArticle was published in
Czech Gynaecology

2025 Issue 3
-
All articles in this issue
- Analýza rizikových faktorov rastu plodu – vplyv maternálnych faktorov a kongenitálnej cytomegalovírusovej infekcie
- Vzdělávací hodnota chirurgických videí na YouTube – hodnocení kvality a soubor standardů videí o hysterektomii pomocí transluminální endoskopické operace s přirozeným vaginálním vstupem
- Účinnost fyzioterapie na úlevu od bolesti a funkční zotavení po císařském řezu
- Souvislost mezi hladinou kisspeptinu v séru v I. trimestru a prenatálními komplikacemi
- Hysterosalpingografické vyšetření po léčbě mimoděložního těhotenství
- Pozdní prenatální diagnostika kompletní pentalogie Cantrella
- Raritní děložní malignita dětského věku kombinovaná s kompletní inverzí dělohy
- Možnost využití indocyaninové zeleně v managementu endometriózy
- Gastroschíza u plodu – současné možnosti prenatální diagnostiky a následný management
- Robsonova klasifikácia – cesta k zníženiu počtu cisárskych rezov?
- Shromáždění členů
- Czech Gynaecology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Účinnost fyzioterapie na úlevu od bolesti a funkční zotavení po císařském řezu
- Analýza rizikových faktorov rastu plodu – vplyv maternálnych faktorov a kongenitálnej cytomegalovírusovej infekcie
- Robsonova klasifikácia – cesta k zníženiu počtu cisárskych rezov?
- Gastroschíza u plodu – současné možnosti prenatální diagnostiky a následný management
