Monofolikulární vývoj – cíl indukce ovulace folitropinem beta pro intrauterinní inseminaci
Mono-follicular Development – the Objective of Ovulation Induction with Follitropin beta Combined with Intrauterine Insemination
Objective:
To assess the effect of different starting follitropin’s beta dose (50 IU, 75 IU and 100 IU daily) for ovulation induction combined with intrauterine insemination on mono-follicular development.
Subject:
Prospective study.
Setting:
Centre for Assisted Reproduction SANUS, Pardubice.
Subject and method:
From March 2005 to November 2007 we performed a total number of 111 ovarian stimulations for patients with unexplained infertility, anovulatory disorder or mild male factor. We divided patients into groups based on patient’s response to clomifen citrate treatment. We examined follicular growth day 9 by transvaginal ultrasound and if necessary we adjusted gonadotropins’s dose.
Results:
We performed 104 intrauterine inseminations (94% of cycles with ovulation induction). We proved mono-follicular development in 36%, 37% and 36% (ns), number of follicles 1,9 ± 0,8, 2,2 ± 1,2 and 2,5 ± 1,8 (ns), endometrial thickness (mm) 8,5 ± 1,2, 8,6 ± 1,7 and 9,1 ± 1,8 (ns), total dose of rFSH (IU) 440 ± 156, 583 ± 154 and 830 ± 268 (p
Conclusions:
50 IU follitropin beta daily offers 36% probability of mono-follicular development. The disadvantage may be an increased risk of cycle cancellation due to low ovarian response. Daily doses 75 IU or 100 IU increase total consumption of rFSH.
Key words:
ovulation induction, intrauterine insemination, clomifene citrate, gonadotropins, follitropin beta, pregnancy rate, OHSS
Autoři:
R. Středa 1; J. Štěpán 1; J. Tošner 2
Působiště autorů:
Centrum asistované reprodukce SANUS, Pardubice, prim. MUDr. J. Štěpán, CSc.
1; Gynekologicko-porodnická klinika, Fakultní nemocnice Hradec Králové, přednosta doc. MUDr. J. Tošner, CSc.
2
Vyšlo v časopise:
Ceska Gynekol 2008; 73(2): 93-97
Souhrn
Cíl:
Zhodnocení účinku rozdílných počátečných dávek rekombinantního gonadotropinu (rFSH) folitropinu beta (PUREGON PEN - 50 IU, 75 IU a 100 IU denně) na monofolikulární vývoj ve spojení s intrauterinní inseminací.
Typ studie:
Prospektivní studie.
Název a sídlo pracoviště:
Centrum asistované reprodukce SANUS, Pardubice.
Předmět a metoda:
Od května 2005 do listopadu 2007 jsme realizovali 111 ovariálních stimulací u pacientek s idiopatickým faktorem neplodnosti, anovulací nebo mírným andrologickým faktorem. Pacientky jsme rozdělili do skupin s denní úvodní dávkou 50 IU, 75 IU a 100 IU folitropinu beta na základě znalosti ovariální odpovědi na anamnestickou léčbu klomifencitrátem. Aplikaci gonadotropinů jsme začali 3. den menstruačního cyklu a 9. den jsme provedli ultrazvukovou kontrolu vývoje foliklů s případnou úpravou dávky.
Výsledky:
Intrauterinní inseminaci jsme realizovali u 104 pacientek (94 % pacientek, které zahájily léčbu). Prokázali jsme monofolikulární vývoj v 36 %, 37 % a 36 % (ns), počet foliklů 2 ± 0,8, 2,2 ± 1,1 a 2,5 ± 1,8 (ns), výšku endometria 8,5 ± 0,9, 8,7 ± 1,4 a 9,1 ± 1,8 mm (ns), celkovou spotřebu rFSH (IU) 440 ± 156, 583 ± 154 a 830 ± 268 (p
Závěr:
Počáteční dávka 50 IU rFSH denně nabízí 36% pravděpodobnost monofolikulárního vývoje. Nevýhodou může být zvýšené riziko zrušení cyklu pro nízkou ovariální odpověď. Počáteční dávka 75 IU nebo 100 IU denně zvyšuje celkovou spotřebu rFSH.
Klíčová slova:
indukce ovulace, intrauterinní inseminace, gonadotropiny, folitropin beta, těhotenský index, OHSS
ÚVOD
Nejdůležitějším úkolem v terapii gonadotropiny [20] je určení počáteční dávky rekombinantního FSH (rFSH) k zajištění monofolikulárního vývoje (vývoj jednoho foliklu). V případě nízké nebo naopak vysoké ovariální odpovědi, je nutné úpravou dávky rFSH dosáhnout ovulace bez navození ovariální hyperstimulace. Cílem indukce ovulace folitropinem beta v této studii je dosažení účinné dávky rFSH (threshold dose) potřebné k vývoji jednoho preovulačního foliklu.
HYPOTÉZA
Počáteční dávka 50 IU rFSH denně umožňuje u většiny pacientek rychle reagujících na anamnestické podání antiestrogenů zajistit vývoj foliklu, minimalizuje riziko vysoké ovariální odpovědi, ale může vést k vyššímu riziku zastavení léčebného cyklu pro nízkou ovariální odpověď v porovnání s vyšší počáteční dávkou.
Počáteční dávka 75 IU nebo 100 IU rFSH denně zvyšuje počet foliklů a snižuje riziko zastavení léčebných cyklů pro nízkou ovariální odpověď v porovnání s počáteční dávkou 50 IU. Na druhé straně je možné očekávat zvýšené riziko zrušení cyklů pro vysokou ovariální odpověď (více než 4 folikly), nárůst rizika vícečetného těhotenství i ovariálního hyperstimulačního syndromu (OHSS).
CÍLE STUDIE
Primárním cílem studie je zhodnocení účinku rozdílných počátečných dávek folitropin beta (Puregon pen - 50 IU, 75 IU a 100 IU denně) na monofolikulární vývoj, počet foliklů > 16 mm, výšku endometria a celkovou spotřebu rFSH.
Sekundárním cílem studie je zhodnocení účinku rozdílných počátečných dávek folitropinu beta (PUREGON PEN - 50 IU, 75 IU a 100 IU denně) na délku stimulace, riziko zastavení cyklu a riziko ovariálního hyperstimulačního syndromu.
SOUBOR PACIENTEK A METODIKA
Od května 2005 do listopadu 2007 jsme realizovali 111 ovariálních stimulací u pacientek s idiopatickým faktorem neplodnosti, anovulací nebo mírným andrologickým faktorem.
Vstupní kritéria
- Sterilita nejméně 1 rok.
- Věk 18 až 38 let.
- BMI 18-30 kg/m2.
- Bazální hladiny FSH a LH < 10 IU/l.
- Normální tvar dutiny děložní a prokázaná průchodnost vejcovodů hysterosalpingografií nebo diagnostickou hysteroskopií a laparoskopií s chromopertubací.
- Léčba klomifencitrátem v anamnéze.
- Počet spermií > 5 mil/ml po swim-up (WHO, 1999).
Kritéria zamítnutí účasti ve studii
- Spontánní těhotenství.
- Ovariální cysta.
Průběh studie:
- Ultrazvukovým vyšetřením před aplikací gonadotropinů jsme vyloučili ovariální cysty.
- Pacientky jsme rozdělili do skupin s denní úvodní dávkou 50 IU, 75 IU nebo 100 IU folitropinu beta na základě znalosti ovariální odpovědi na anamnestickou léčbu klomifencitrátem. Pacientkám s rychlou odpovědí na klomifencitrát 1x1 tbl. 3.-7.den menstruačního cyklu jsme aplikovali úvodní dávku 50 IU rFSH. Pacientkám s pomalou odpovědí na klomifencitrát 1x1 tbl. nebo dobrou odpovědí na 2x1 tbl. jsme aplikovali úvodní dávku 75 IU rFSH. Pacientkám s pomalou odpovědí na klomifencitrát 2x1 tbl. nebo s potřebou aplikace klomifencitát 3x1 tbl. jsme aplikovali úvodní dávku 100 IU rFSH. Subkutánní aplikaci určené dávky gonadotropinů jsme začali 3. den menstruačního cyklu.
- Folikulární vývoj jsme monitorovali ultrazvukovým vyšetřením 9. den menstruačního cyklu a v případě potřeby jsme změnili dávku gonadotropinů (dávky rFSH jsme zvýšili pro folikly < 12 mm v průměru nebo snížili při průkazu 4 foliklů > 14 mm).
- hCG 5 000 IU jsme aplikovali při dosažení průměru foliklu 18 mm a výšky endometria 8 mm.
- Intrauterinní inseminaci jsme realizovali po 36 hodinách pomocí Cookova katétru po přípravě spermií metodou swim-up.
- Luteinní fázi jsme podpořili mikronizovaným progesteronem 200 mg denně vaginálně.
- Těhotenský test jsme provedli za 14 dní.
VÝSLEDKY
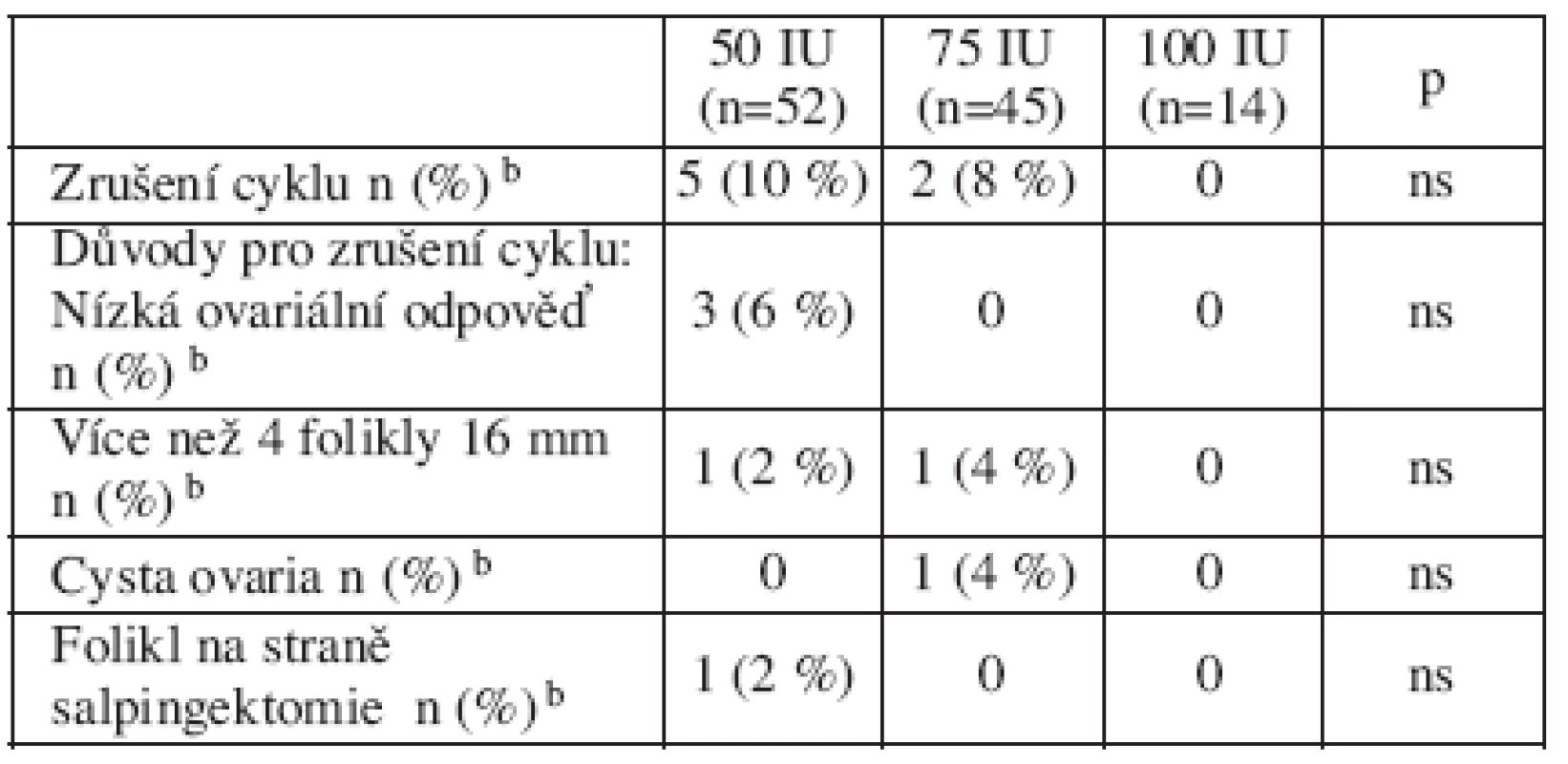
Intrauterinní inseminaci jsme realizovali u 104 pacientek (94 % pacientek, které zahájily léčbu) a celkově jsme dosáhli 18 těhotenství (těhotenský index 17 %). Charakteristiky pacientek a léčebných cyklů zobrazují tabulky 1-4. Nebyl pozorován projev ovariálního hyperstimulačního syndromu. Cyklus jsme zrušili (zastavili jsme aplikaci dalších gonadotropinů) u 7 pacientek, tj. 6 % z celkového počtu pacientek, které zahájily ovariální stimulaci gonadotropiny (tab. 4).

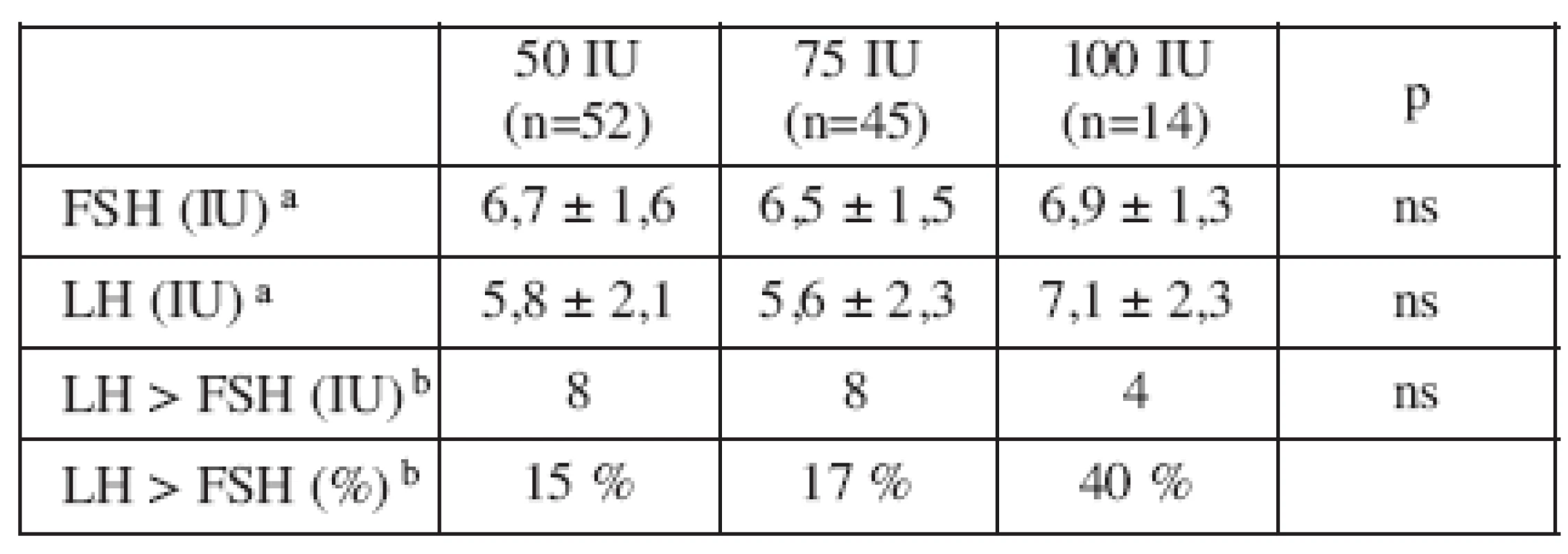

Statistická analýza byla provedena χ2 testem a ANOVA (metoda analýzy variance). Hladina významnosti alfa 0,05 (p<0,05) je považována za statisticky významnou. Statisticky nevýznamná data značíme ns.
DISKUSE
Intrauterinní inseminace (IUI) by měla být léčbou první volby pro idiopatický faktor neplodnosti i mírný andrologický faktor [8, 19, 22, 35]. V přirozených cyklech je účinek intrauterinní inseminace omezený (těhotenský index 6,3 %) [34]. Indukce ovulace zvyšuje těhotenský index [34]. Metaanalýza randomizovaných studií [9] i studie [2] prokázala zvýšený těhotenský index při provedení intrauterinní inseminace s indukcí ovulace klomifencitrátem než v přirozených cyklech. Klomifencitrát je doporučován jako úvodní léčba pro páry s idiopatickým faktorem neplodnosti, mírným andrologickým faktorem i pro ženy s anovulací WHO skupiny II [11, 27]. Touto léčbou se dosahuje ovulace přibližně u 70 % pacientek a kumulativní těhotenský index v období 6 měsíců je 35 % [15, 24]. Omezením použití klomifencitrátu je klomifencitrátová rezistence a případný antiestrogenní účinek na cervikální hlen a endometrium (nízká sliznice). Mnohočetný vývoj foliklů vysvětluje vysoké riziko vícečetného těhotenství po terapii klomifencitrátem – 15 % dvojčat a okolo 5 % trojčat [10]. Užití klomifencitrátu neumožňuje individualizaci léčby, pouze změnu dávky.
Metaanalýza randomizovaných studií [9] i studie [3] prokazuje zvýšený těhotenský index pro intrauterinní inseminaci s indukcí ovulace gonadotropiny než klomifencitrátem. Nejprve byly použity urinární gonadotropiny, jejichž omezením jsou vysoké dávky FSH (75 IU nebo 150 IU denně), riziko vývoje více než 4 foliklů a potřeba nitrosvalové aplikace přípravku. Nově existují výsledky studií porovnávající klomifencitrát s rekombinantními gonadotropiny pro indukci ovulace společně s intrauterinní inseminací [7, 17, 26]. Výhodou rFSH je možnost aplikace malých denních dávek – 50 IU denně – podkožně samotnou pacientkou, změna dávky v malých krocích (např. 25 IU rFSH) a bezpečný profil léčby. Porovnáním rozdílných gonadotropinů ve spojení s intrauterinní inseminací [14, 16, 21] bylo prokázáno, že přípravky rekombinantních FSH [25, 30, 33] vedou k lepším výsledkům pro idiopatický faktor neplodnosti než přípravky urinárních gonadotropinů [12, 13]. Byly použity počáteční dávky rFSH od 50 IU do 100 IU denně [21].
Pro neplodné ženy s PCO syndromem a anovulací se studie [18, 24] shodují na počáteční dávce 50 IU rFSH. Je doporučeno dávku zvýšit po 7–14 dnech po podání přípravku, pokud nejsou prokázány folikly v průměru alespoň 12 mm. Doporučené zvýšení dávky je 25 IU rFSH denně [24], zvýšení dávky o 50 IU rFSH denně zvyšuje riziko nadměrné ovariální odpovědi. Okolo 5 % cyklů bývá zastaveno pro nízkou ovariální odpověď [24]. Obě prospektivní studie [9, 18] a dále i randomizovaná studie [20] v závěru konstatují, že úvodní dávka 50 IU rFSH je pro tuto skupinu žen patřičná.
Pro idiopatický faktor neplodnosti nebo páry s mírným andrologickým faktorem je počáteční dávka 50 IU rFSH denně navržená na základě nerandomizovaných studií [6]. Jedna retrospektivní studie [29] porovnává aplikaci 50 IU a 75 IU rFSH denně společně s intrauterinní inseminací pro idiopatický faktor neplodnosti a nabízí těhotenský index 10 %. Studie konstatuje, že minimální FSH stimulace pro intrauterinní inseminace může snížit riziko dvoj - a vícečetného těhotenství bez negativního vlivu na dosažený těhotenský index.
Nejčastějším důvodem pro zastavení cyklu v naší studii byla nízká ovariální odpověď (neprokázali jsme vývoj foliklu ani po opakovaném zvýšení dávky rFSH). Dalšími důvody byly: vývoj 4 a více foliklů v průměru 16 mm (vysoká ovariální odpověď), přítomnost funkční ovariální cysty nebo vývoj foliklu na straně po odstranění vejcovodu. V případě vysoké ovariální odpovědi jsme doporučili neaplikovat hCG a podpořili jsme použití mechanické formy antikoncepce (kondom) jako prevenci vzniku vícečetného těhotenství.
Protože jsme studii připravili pro pacientky s idiopatickým faktorem neplodnosti, anovulací a páry s mírným andrologickým faktorem, skutečnost klomifencitrátové rezistence jsme nezkoumali, neboť tuto skutečnost bereme jako součást léčby pacientek s PCO syndromem (LH > 10 IU). Nezabývali jsme se ani použitím metforminu[28] či letrozolu[4, 5], za jiných okolností úspěšně použitých pro modifikaci folikulárního růstu.
Účinek GnRH antagonistů v protokolu s folitropinem beta jsme nestudovali v rámci této studie. Přestože bylo provedeno několik randomizovaných studií o účinku GnRH antagonistů v protokolu s intrauterinní inseminací, výsledky jsou rozporuplné. Některé studie [2, 31, 32] podporují užití GnRH antagonistů pro prevenci předčasného vzestupu LH a zvýšení těhotenského indexu. Jiné studie [1, 23, 36] tyto výsledky neprokazují, odhalují zvláště vysoké riziko potratu a naznačují případný nežádoucí účinek GnRH antagonistů na endometrium. Výsledky italských autorů [10] – těhotenský index 12 % ve skupině s GnRH antagonistou – jsou nižší než v našem souboru.
ZÁVĚR
Počáteční dávka 50 IU rFSH denně je účinná ve spojení s intrauterinní inseminací a nabízí 36% pravděpodobnost monofolikulárního vývoje. Nevýhodou může být zvýšené riziko zrušení cyklu pro nízkou ovariální odpověď.
Počáteční dávka 75 IU nebo 100 IU denně zvyšuje celkovou spotřebu rFSH.
Správné určení počáteční dávky rFSH a v případě potřeby její přizpůsobení podle rychlosti vývoje vývoje foliklů, jsou důležité kroky k minimalizaci rizika vývoje více foliklů, vícečetného těhotenství a ovariálního hyperstimulačního syndromu.
Poděkování
Autoři děkuji pracovníkům embryologické laboratoře Centra asistované reprodukce SANUS Pardubice za přípravu spermií k provedení intrauterinních inseminací.
MUDr. Robert Středa
Centrum asistované reprodukce SANUS, Pardubice
Nábřeží Závodu míru 2740
530 02 Pardubice
rstreda@seznam.c
Zdroje
1. Allegra, A., Marino, A, Coffaro, F., et al. GnRH antagonist-induced inhibition of the premature LH surge increases pregnancy rates in IUI-stimulated cycles. A prospective randomized trial. Hum Reprod, 2006, 22, p. 101-108.
2. Arici, A., Byrd, W., Bradshaw, K., et al. Evaluation of clomiphene citrate and human chorionic gonadotropin treatment: a prospective, randomized, crossover study during intrauterine insemination cycles. Fertil Steril, 1994, 61, p. 314-318.
3. Balasch, J, Ballesca JL, Pimentel C, et al. Late low-dose pure follicle stimulating hormone for ovarian stimulation in intra-uterine insemination cycles. Hum Reprod, 1994, 9, p. 1863-1866.
4. Barroso, G., Menocal, G., Felix, H., et al. Comparison of the efficacy of the aromatase inhibitor letrozole and clomiphene citrate as adjuvants to recombinant follicle-stimulating hormone in controlled ovarian hyperstimulation: a prospective, randomized, blinded clinical trial. Fertil Steril, 2006, 86, p. 1428-1431.
5. Bedaiwy, MA., Forman, R., Mousa, NA., et al. Cost-effectiveness of aromatase inhibitor co-treatment for controlled ovarian stimulation. Hum Reprod, 2006, 21, p. 2838-2844.
6. Calaf, AJ., Ruiz Balda, JA., Romeu, SA., et al. Ovulation induction with a starting dose of 50 IU of recombinant follicle stimulating hormone in WHO group II anovulatory women: the IO-50 study, a prospective, observational, multicentre, open trial. BJOG, 2003, 110, p. 1072-1077.
7. Cohlen, BJ., Vandekerckhove, P., te Velde, ER., et al. Timed intercourse versus intra-uterine insemination with or without ovarian hyperstimulation for subfertility in men. Cochrane.Database.Syst.Rev. 2000, CD000360.
8. Collins, J. Stimulated intra-uterine insemination is not a natural choice for the treatment of unexplained subfertility. Current best evidence for the advanced treatment of unexplained subfertility. Hum Reprod, 2003, 18, p. 907-912.
9. Costello, MF. Systematic review of the treatment of ovulatory infertility with clomiphene citrate and intrauterine insemination. Aust NZJ Obstet Gynaecol, 2004, 44, p. 93-102.
10. Crosignani, PG., Somigliana, E. Effect of GnRH antagonists in FSH mildly stimulated intrauterine insemination cycles: a multicentre randomized trial. Hum Reprod, 2007, 22, p. 500-505.
11. Dankert, T., Kremer, JA., Cohlen, BJ., et al. A randomized clinical trial of clomiphene citrate versus low dose recombinant FSH for ovarian hyperstimulation in intrauterine insemination cycles for unexplained and male subfertility. Hum Reprod, 2007, 22, 3, p. 792-797.
12. Daya, S., Gunby, J. Recombinant versus urinary follicle stimulating hormone for ovarian stimulation in assisted reproduction. Hum Reprod, 1999, 14, p. 2207-2215.
13. Daya, S., Gunby, J. Recombinant versus urinary follicle stimulating hormone for ovarian stimulation in assisted reproduction cycles. Cochrane Database Syst Rev, 2000, CD002810.
14. Demirol, A., Gurgan, T. Comparison of different gonadotrophin preparations in intrauterine insemination cycles for the treatment of unexplained infertility: a prospective, randomized study. Hum Reprod, 2007, 22, p. 97-100.
15. Dickey, RP., Taylor, SN., Lu, PY., et al. Clomiphene citrate intrauterine insemination (IUI) before gonadotropin IUI affects the pregnancy rate and the rate of high-order multiple pregnancies. Fertil Steril, 2004, 81, p. 545-550.
16. Gerli, S., Casini, ML., Unfer, V., et al. Ovulation induction with urinary FSH or recombinant FSH in polycystic ovary syndrome patients: a prospective randomized analysis of cost-effectiveness. Reprod Biomed Online, 2004, 9, p. 494-499.
17. Gerli, S., Casini, ML., Unfer, V., et al. Recombinant versus urinary follicle-stimulating hormone in intrauterine insemination cycles: a prospective, randomized analysis of cost effectiveness. Fertil Steril, 2004, 82, p. 573-578.
18. Hayden, CJ., Rutherford, AJ., Balen, AH. Induction of ovulation with the use of a starting dose of 50 units of recombinant human follicle-stimulating hormone (Puregon). Fertil Steril, 1999, 71, p. 106-108.
19. Hughes, EG. Stimulated intra-uterine insemination is not a natural choice for the treatment of unexplained subfertility. ‘Effective treatment’ or ‘not a natural choice’? Hum Reprod, 2003, 18, p. 912-914.
20. Hugues, JN., Cedrin-Durnerin, I., Howles, CM., et al. use of a decremental dose regimen in patients treated with a chronic low-dose step-up protocol for WHO Group II anovulation: a prospective randomized multicentre study. Hum.Reprod. 2006, 21, p. 2817-22.
21. Isaza, V., Requena, A., Garcia-Velasco, JA., et al. Recombinant vs. urinary follicle-stimulating hormone in couples undergoing intrauterine insemination. A randomized study. J Reprod Med, 2003, 48, p. 112-118.
22. Khalil, MR., Rasmussen, PE., Erb, K., et al. Homologous intrauterine insemination. An evaluation of prognostic factors based on a review of 2473 cycles. Acta Obstet Gynecol Scand, 2001, 80, p. 74-81.
23. Lambalk, CB., Leader, A., Olivennes, F., et al. Treatment with the GnRH antagonist ganirelix prevents premature LH rises and luteinization in stimulated intrauterine insemination: results of a double-blind, placebo-controlled, multicentre trial. Hum Reprod, 2006, 21, p. 632-639.
24. Leader, A. Improved monofollicular ovulation in anovulatory or oligo-ovulatory women after a low-dose step-up protocol with weekly increments of 25 international units of follicle-stimulating hormone. Fertil Steril, 2006, 85, p. 1766-1773.
25. Levi Setti, PE. The importance of consistent FSH delivery in infertility treatment. Reprod Biomed Online, 2006, 12, p. 493-499.
26. Lopez, E., Gunby, J., Daya, S., et al. Ovulation induction in women with polycystic ovary syndrome: randomized trial of clomiphene citrate versus low-dose recombinant FSH as first line therapy. Reprod Biomed Online, 2004, 9, p. 382-390.
27. Messinis, IE. Ovulation induction: a mini review. Hum Reprod, 2005, 20, p. 2688-2697.
28. Palomba, S., Falbo, A., Orio, F. Jr., et al. A randomized controlled trial evaluating metformin pre-treatment and co-administration in non-obese insulin-resistant women with polycystic ovary syndrome treated with controlled ovarian stimulation plus timed intercourse or intrauterine insemination. Hum Reprod, 2005, 20, p. 2879-2886.
29. Papageorgiou, TC., Guibert, J., Savale, M., et al. Low dose recombinant FSH treatment may reduce multiple gestations caused by controlled ovarian hyperstimulation and intrauterine insemination. BJOG, 2004, 111, p. 1277-1282.
30. Platteau, P., Andersen, AN., Balen, A., et al. Similar ovulation rates, but different follicular development with highly purified menotrophin compared with recombinant FSH in WHO Group II anovulatory infertility: a randomized controlled study. Hum Reprod, 2006, 21, p. 1798-1804.
31. Ragni, G., Alagna, F., Brigante, C., et al. GnRH antagonists and mild ovarian stimulation for intrauterine insemination: a randomized study comparing different gonadotrophin dosages. Hum Reprod, 2004, 19, p. 54-58.
32. Ragni, G., Caliari, I., Nicolosi, AE., et al. Preventing high-order multiple pregnancies during controlled ovarian hyperstimulation and intrauterine insemination: 3 years’ experience using low-dose recombinant follicle-stimulating hormone and gonadotropin-releasing hormone antagonists. Fertil Steril, 2006, 85, p. 619-624.
33. Revelli, A., Poso, F., Gennarelli, G., et al. Recombinant versus highly-purified, urinary follicle-stimulating hormone (r-FSH vs. HP-uFSH) in ovulation induction: a prospective, randomized study with cost-minimization analysis. Reprod Biol Endocrinol, 2006, 4, p. 38.
34. Středa, R., Štěpán, J., Zadrobílková, I., et al. Indukce ovulace zvyšuje těhotenský index u intrauterinní inseminace. Čes Gynek, 2007, 64, s.159-163.
35. Verhulst, SM., Cohlen, BJ., Hughes, E., et al. Intra-uterine insemination for unexplained subfertility. Cochrane Database Syst Rev, 2006, CD001838.
36. Williams, RS., Hillard, JB., De Vane, G., et al. A randomized, multicenter study comparing the efficacy of recombinant FSH vs recombinant FSH with Ganirelix during superovulation/IUI therapy. Am J Obstet Gynecol, 2004, 191, p. 648-651.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicínaČlánek vyšel v časopise
Česká gynekologie

2008 Číslo 2
-
Všechny články tohoto čísla
- Poranění velkých cév v gynekologické endoskopii
- Význam sonografie a hysteroskopie u suspektních nálezů na endometriu menopauzálních žen
- Vliv idiopatického střevního zánětu na interval potřebný pro početí pacientek
- Císařský řez a anální inkontinence
- Indukce potratů ve II. trimestru na Gynekologicko porodnické klinice FN na Bulovce
- Adrenokortikálne choroby v gravidite
- NOVÉ KNIHY
- Výsledky kombinované léčby endometriózy v šestiletém období (2001-2007) na oddělení gynekologie a minimálně invazivní chirurgie Nemocnice Na Homolce Praha
- NOVÉ KNIHY
- Mrtvorozenost v České republice v roce 2005II. Vzájemné vztahy některých evidovaných údajů
- Perzistující trofoblastická nemoc v Centru pro trofoblastickou nemoc v ČR v letech 1955 – 2007
- Význam chromozomálních změn ve vztahu k prognostickým faktorům u zhoubných nádorů vaječníku a děložního hrdla
- Význam metylace v genomu lidského papillomaviru 16 u karcinomu děložního hrdla
- Monofolikulární vývoj – cíl indukce ovulace folitropinem beta pro intrauterinní inseminaci
- Hladiny prostaglandinu E2 , (PGE2) v ovulačním hlenu u spontánně potrácejících pacientek
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Indukce potratů ve II. trimestru na Gynekologicko porodnické klinice FN na Bulovce
- Perzistující trofoblastická nemoc v Centru pro trofoblastickou nemoc v ČR v letech 1955 – 2007
- Význam sonografie a hysteroskopie u suspektních nálezů na endometriu menopauzálních žen
- Adrenokortikálne choroby v gravidite
