Možnost využití indocyaninové zeleně v managementu endometriózy
Possible use of indocyanine green in the management of endometriosis
Endometriosis affects approximately 10% of women of fertile age and its deep infiltrating form causes serious consequences for fertility, clinical problems depending on which organs are affected (urinary and digestive tract) and causes serious pain which seriously impairs quality of life. Resection of the affected tissue tend to be complex and often require multidisciplinary approach. Resection in the field of severe deep infiltrating endometriosis is complicated by the difficulty of resection line identification. Although we are able to perform most of the resections laparoscopically, there is still significant risk of intra and postoperative complications, the most serious of which is the formation of rectovaginal fistulas. Identification of boundaries of the endometrial nodule and preservation of tissue vitality is crucial in resection procedures. Endometriotic nodules, based on the pathogenesis of the lesion, have various vascularity and therefore different perfusion patterns. According to nature of tissue and the degree of vascularization, most deep infiltrating nodules have rather hypoperfusion pattern. A substance that would be able to guide the resection by live monitoring of the tissue perfusion, could have useful therapeutic applications. Such substance could be the fluorescent dye indocyanine green. With resection guidance by fluorescence dye, we could be able of pathogenesis oriented management of the disease and therefore perform more gentle tissue preparation, with less collateral damage, reduction of intra and postoperative complications, and thus improvement of the quality of life of patients in terms of pain, risk of recurrence, and preservation of fertility.
Keywords:
indocyanine green – deep infiltrating endometriosis – tissue perfusion – guided resection
Autoři:
Vladimír Baláž 1,2
; Martin Syrůček 3; Jiří Presl 2,4
Působiště autorů:
Gynekologické oddělení, Nemocnice na Homolce, Praha
1; LF UK v Plzni
2; Oddělení patologie, Nemocnice Na Homolce, Praha
3; Gynekologicko-porodnická klinika FN Plzeň
4
Vyšlo v časopise:
Ceska Gynekol 2025; 90(3): 238-246
Kategorie:
Přehledová práce
doi:
https://doi.org/10.48095/cccg2025238
Souhrn
Endometrióza postihuje přibližně 10 % žen ve fertilním věku a její hluboká infiltrující forma způsobuje závažné důsledky na plodnost, klinické potíže dle postižených orgánů (močový a trávicí trakt) a bolest, která výrazně ovlivňuje kvalitu života. Resekční výkony na postižených orgánech bývají složité a často si vyžadují multioborový přístup. Resekce v terénu těžké hluboké infiltrující endometriózy je komplikovaná obtížnou identifikací resekční linie. I když jsme schopni většinu resekčních výkonů provádět laparoskopickým přístupem, pořád jsou zatíženy významným rizikem per - a pooperačních komplikací, z nichž nejzávažnější je vznik rektovaginálních píštělí. Identifikace hranic endometriálního uzlu a zachování vitality tkání je u resekčních výkonů z tohoto pohledu kruciální. Endometriotické uzly na základě patogeneze vzniku léze mají různou vaskularitu, a tím pádem i různé perfuzní vzorce, přičemž vzhledem k charakteru tkáně a stupni vaskularizace má většina hluboko infiltrujících uzlů spíše hypoperfuzní vzor. Prostředek, který by umožňoval cílení (vedení) resekce pomocí sledování perfuze tkání, by mohl mít užitečné terapeutické využití. Takovým prostředkem by mohlo být fluorescenční barvivo indocyaninová zeleň. Cílením resekce pomocí fluorescenčního barviva bychom mohli být schopni managementu orientovaného na patogenezi onemocnění, a tím i šetrnější resekce s menší destrukcí tkání, s redukcí per - a pooperačních komplikací a zároveň zlepšení kvality života pacientek, co se týká bolestivosti, rizika recidivy a zachování fertility.
Klíčová slova:
indocyaninová zeleň – perfuze tkání – cílená resekce – hluboko infiltrující endometrióza
Úvod
Endometrióza je relativně časté onemocnění, které postihuje přibližně 10 % žen [1]. Její hluboká infiltrující forma postihuje v 8–12 % gastrointestinální trakt a z toho v 90 % je postiženou částí rektum [2].
Chirurgická léčba hluboké infiltrující endometriózy je vždy složitá, často vyžadující multidisciplinární přístup (účast nejen gynekologa, ale i kolorektálního chirurga a urologa).
I když je chirurgické léčba rezervována pro případy, kdy selže nebo neúčinkuje prvostupňová symptomatická (medikamentózní) léčba, indikace k operaci a volba optimálního postupu je obtížná, a i tak s sebou přináší určitá per - a postoperační rizika.
Ulehčení operačního výkonu zlepšenou vizualizací postižené tkáně a využití její histopatologické charakteristiky by mohlo mít významný dopad na úspěšnost léčby. Takovou metodou by mohlo být využití perfuzní charakteristiky postižené tkáně pomocí fluorescenčního barviva, jako je třeba indocyaninová zeleň (ICG – indocyanine green).
Indocyaninová zeleň je dobře známá molekula, která se používá v medicíně přes 50 let a nachází využití napříč různými chirurgickými obory. V onkologické operativě se používá k označení sentinelové uzliny, což umožňuje kontrolovat úroveň radikality výkonu, a redukovat tak rizika léčby. V oborech jako oční lékařství, chirurgie a hepatologie má ICG prokázanou účinnost v hodnocení perfuze tkání. Jedná se fluorescenční barvivo, které má schopnost reemitovat světlo po světelné excitaci. Spektrum absorpce a fluorescence je blízko infračerveného spektra (NIR – near infra red). Absorbuje vlnové délky mezi 600 a 900 nm a emituje fluorescenci mezi 750 a 950 nm (max. cca 830 nm v krvi) [3].
Indocyaninová zeleň patří mezi benzoindotricarbocyaniny, je lipofilní a díky sulfátové skupině rozpustná i ve vodě. To jí dává výjimečné amfifilní vlastnosti. Po i.v. aplikaci se váže se sérovým albuminem, lipoproteiny, fosfolipidy a plazmatickými proteiny. Dle druhu rozpouštědla a koncentrace barviva může docházet k posunu absorpčního spektra. ICG je eliminována výhradně jaterními buňkami do žluče [4].
Plazmatická clearance je bifázická, s iniciální fází s poločasem rozpadu 2–4 min [3–5] s přetrvávající sekundární fází s nízkou koncentrací po dobu 60 min [6].
ICG má mimořádně dobrý bezpečnostní profil, s frekvencí nežádoucích reakcí max. mezi 0,15 a 1,1 %, přičemž těžká reakce po aplikaci je jen na úrovni 0,05 % [5,7]. Nebylo potvrzeno zvýšené riziko těžké alergické reakce či anafylaxe u pacientů s alergií na jód či mořské plody [8].
Nejčastější dávkování u i.v. aplikace je 0,2–0,3 mg/kg [9–12], přičemž max. dávka může být až 5 mg/kg za 24 hod. Toho času jediný v ČR registrovaný přípravek obsahující ICG je přípravek Verdye obsahující 5 mg barviva na 1 ml připraveného roztoku. Příprava barviva, které je ve formě prášku, se provádí rozpuštěním 1 ampule v 10 ml vody pro přípravu injekcí. U běžné pacientky do hmotnosti cca 50 kg vystačí na celkově čtyři aplikace po celou dobu výkonu.
Dle SPC přípravku je Verdye určen primárně k funkční diagnostice srdeční, oběhové, mikrooběhové a tkáňové perfuze (SÚKL SPC Verdye), což je oblast, jejíž potenciál zůstává v oboru gynekologie zatím nevyužitý.
Přehled práce
Použití ICG v hodnocení tkáňové perfuze má rozsáhlé využití ve sledování vaskularizace v rekonstrukčních operacích střeva, ureterů, pochvy, provádění derivace moči, kožních laloků, transpozice a transplantace dělohy a rekonstrukce nervů [5].
Jak již bylo zmíněno, po i.v. aplikaci se molekuly ICG rychle vážou na plazmatické proteiny a peroperační fluorescence má rychlý nástup. V krátké době difunduje celý orgán a umožňuje získat přehled o cévním zásobení v jednotlivých částech po případné resekci.
Dlouhodobě se tato vlastnost využívá v gastrointestinální chirurgii k hodnocení cévního zásobení v místě anastomózy jako prevence jejího prosakování. Prosakování anastomózy a dehiscence je závažný stav spojený s vysokou mortalitou kvůli rozvoji septického stavu, proto informace umožňující prevenci ischemie je v tomto případě klíčová. Použití ICG fluorescence je asociováno se signifikantní redukcí prosakování anastomózy po kolorektálních resekcích jak pro zhoubné onemocnění, tak i pro benigní nálezy, jako je třeba divertikulóza [13–15].
Se stejným efektem může být ICG využita k prevenci iatrogenního poškození ureterů vzhledem k tomu, že 52–82 % všech iatrogenních poranění ureterů se vyskytuje právě u gynekologických operací [16]. Použití fluorescence může být nápomocné v identifikaci jejich průběhu, tak i případné ischemie. Aplikace může být provedena cystoskopicky zavedením stentu do ureteru [17], nebo intravenózně ke zhodnocení perfuze stěny ureteru po rozsáhlejší disekci v blízkosti jeho průběhu [18]. Druhá varianta se jeví jako slibnější, což je ale potřeba potvrdit dalšími studiemi.
Další možností využití ICG angiografie je prevence dehiscence vaginálního pahýlu po hysterektomii. Frekvence dehiscence vaginálního pahýlu je 0,11–1,27 % po laparoskopické, 0,45–1,64 % po robotické, 0,05–0,13 % po vaginální a 0,02–0,38 % po otevřené hysterektomii [19]. Mírná převaha laparoskopické a robotické operativy je zřejmě z četnějšího užití koagulace. Užití ICG perfuze po i.v. aplikaci by mohlo pomoct odhalení ischemických částí vaginálního pahýlu ještě před suturou a snížit riziko dehiscence [20].
Co se peroperačního iatrogenního poškození týče, poranění pánevních nervů přináší kombinaci motorické, senzorické a autonomní dysfunkce. ICG lze využít k identifikaci genitofemorálního, obturatorního a hypogastrického nervu [21]. ICG fluorescence byla detekována v histopatologických vzorcích nervů a byla distribuována zejména v axonech. Tuto vlastnost lze využít k cílenému, nervy šetřícímu operování i ve výrazně anatomicky nepřehledném terénu [22].
S hodnocením perfuze souvisí i další využití ICG, a sice fluorescenčně vedená resekce, kdy lokální anebo systémové podání přípravku slouží k cílení resekce a identifikaci anatomických struktur a k identifikaci neoplastické či jinak postižené tkáně ve srovnání se zdravými tkáněmi.
Stále častěji je tato technika využívána u resekce jater, kde je prokazatelně častěji dosaženo R0 a menší nutnost použití krevní transfuze [23].
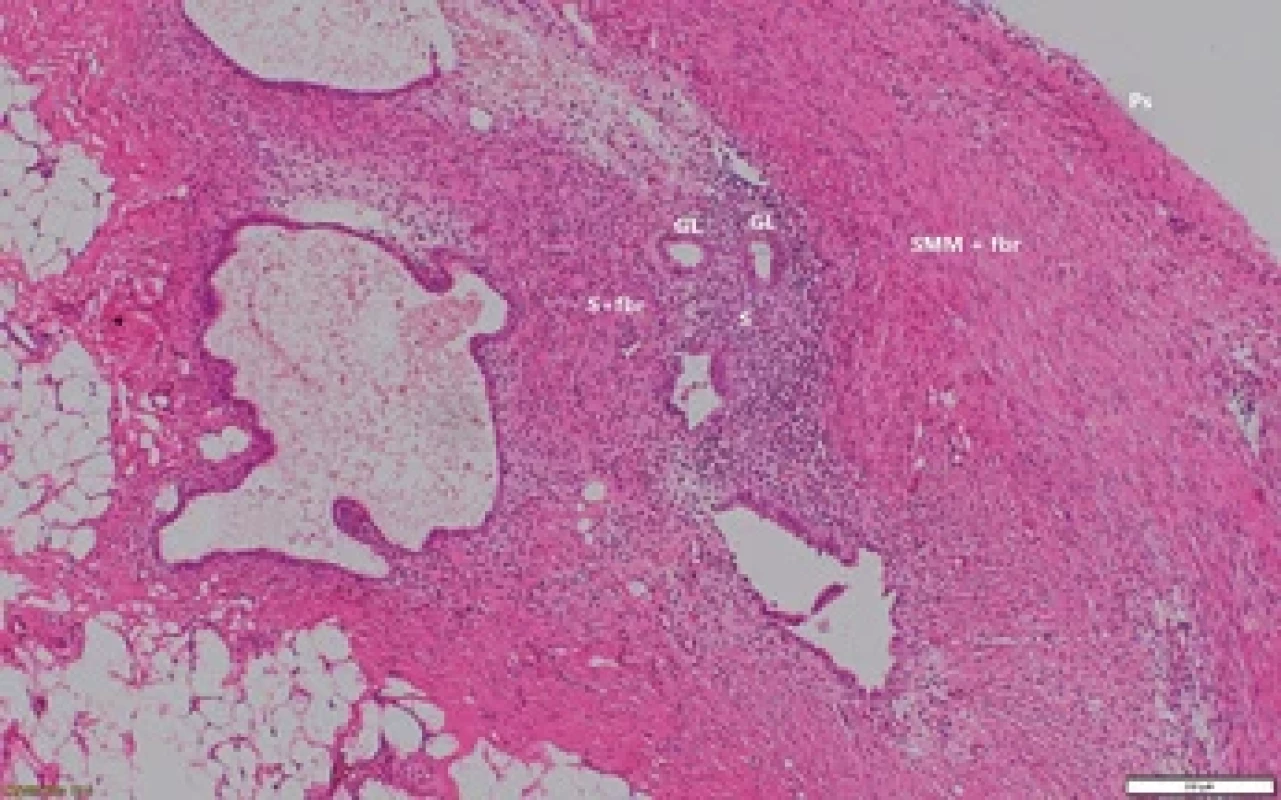
Fig. 2. Peritoneal lesion from Fig. 4 and 5, magnifi cation 100×, H+E (hematoxylin + eosin) staining.
GL – endometrial gland, Ps – peritoneal surface, S – stroma, S+fbr – stroma with fi brosis, SMM+fbr – smooth muscle metaplasia with fi brosis
Z benigních onemocnění by se fluorescenčně vedená resekce mohla využít u operací hluboké infiltrující endometriózy.
Odstranění endometriotického ložiska rekta je prováděno jednak tzv. shavingem neboli nodulektomií, diskoidní resekcí nebo segmentární resekcí střeva [24]. V současnosti lze všechny tyto techniky provádět pomocí laparoskopického přístupu. Vzhledem k celkovému objemu provedených výkonů má každá technika již standardizovaný postup. To vedlo k významné redukci komplikací i následné rekurence. Z metaanalýz vyplývá, že riziko komplikací, zejména riziko rektovaginální fistuly, je nejvyšší u segmentární resekce, a sice u 0–18,1 % případů, dále u diskoidní excize u 0–11,6 % případů a u shavingu je riziko nejnižší, a sice u 0–2,3 % případů, a to včetně rizika peroperační perforace střeva na úrovni 0–11 % [24]. V rukách zkušeného operatéra může být shavingem řešeno 80–90 % lézí [24].
Co se týká rizika rekurence bolestivosti u segmentární resekce, je na úrovni 17,2 %, u diskoidní excize 11,7 % a shavingu 7,9 %, to ale může rovněž souviset s tím, že rozsáhlejší výkony jsou rezervovány pro agresivnější formy nemoci [24]. Co se kvality života po operaci týká, největší omezení je u segmentárních resekcí kvůli riziku syndromu nízké přední rektální resekce (LARS – low anterior rectal resection syndrome) [24].
U pooperační rekurence nemoci neexistuje významný důkaz ke zhodnocení exaktního rizika rekurence. Rovněž nelze jednoznačně určit, zda se jedná o recidivu, nebo o ložisko nově vzniklé v již resekované oblasti. Recidiva je velmi špatně hodnotitelná i z pohledu reziduální nemoci v resekčním okraji, nenulové reziduum je často ve více než 10 % případů [24]. Okultní uzly v preparátech, pokud byla po nodulektomii provedena resekce části střeva, byly identifikovány v 19–43,8 % [25,26]. Mikroskopické okultní léze se dokonce mohou vyskytovat až ve 14,6 % přímo v resekčním okraji preparátů po segmentární resekci [27]. Z pozorování ale vyplývá, že když je odstraněno centrum ložiska, nejsou reziduální žlázy schopny se dál vyvíjet [28].
Z toho vyplývá, že stran operační léčby by měl být preferován nejméně invazivní typ výkonu, a sice shaving (nodulektomie) rekta. I když je u tohoto výkonu v rukou zkušeného operatéra dobrá reproduktibilita s nízkým rizikem komplikací, jistý stupeň asistence a cíleného vedení by mohly mít potenciál ke zlepšení perioperačních výsledků nebo i zkrácení délky operačního výkonu v rukou méně zkušeného operatéra, i když dosažení nulového rezidua je de facto nemožné.
Cílená detekce lézí v případě managmentu endometriózy se zdá být esenciální, protože endometrióza není nádorové onemocnění a excesivní radikalita může zvyšovat perioperační morbiditu a způsobit závažné funkční poškození.
Více prací naznačilo, že ICG by mohlo mít potenciál jak v diagnostice, tak i v chirurgické léčbě endometriózy právě ve smyslu cílení resekce [7–10,29].
Bylo zjištěno, že postižení peritonea endometriózou může ovlivnit perfuzi tkání jak ve smyslu hyper-, tak i hypoperfuze [29].
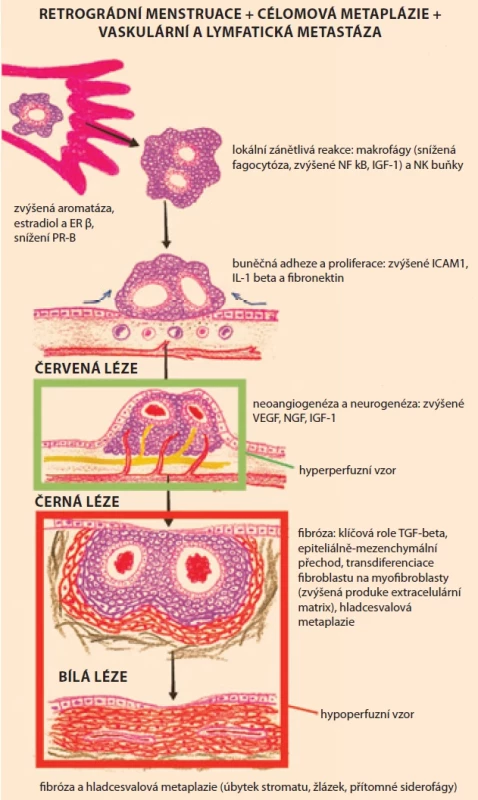
Z toho, co zatím víme o patogenezi vzniku endometriotických lézí, když vycházíme z histopatologického nálezu, lze léze rozdělit na: typické (tzv. černé), červené a bílé (obr. 1). Tyto léze mají rozdílnou morfometrickou charakteristiku. Takzvané léze červené mají vaskularitu a mitotickou aktivitu signifikantně vyšší a takzvané léze bílé mají vaskularitu a mitotickou aktivitu nižší než typické léze [30]. Vaskularizace a indukce angiogeneze mají roli v uhnízdění léze a jejím rozvoji aktivací angiogenních růstových faktorů a látka selektivně cílená na vaskularizaci lézí by mohla mít užitečné terapeutické využití [31]. Výše zmíněné typy lézí lze považovat za různá vývojová stadia postupující od aktivní léze (červený typ) přes typickou lézi až do inaktivního typu léze (bílé).
Zánětlivý proces, který červená léze vyvolá v okolí, aktivuje skarifikační proces, léze se ohraničí a uzavře. Následná fibróza devaskularizuje ložisko, a bílá léze je tak avaskulární latentní formou endometriózy (obr. 1) [30].
Studie prokázaly, že endometriální léze nejsou tvořeny jen endometriálním epitelem a stromatem, ale rovněž hladce svalovou komponentou a fibrózou (obr. 2) [32–34]. Endometriotická léze, obzvláště její intersticium, by mohla být tvořena sekundární reakcí jako biodefenzivní reakce [35].
Fibróza v ložisku bývá asociována ze symptomatologií bolestivosti v důsledku uvěznění nervových struktur ve fibróze [36]. Pozorování asociované s přítomností perineurálního a endoneurálního postižení v rektovaginálních endometriotických nebo adenomyotických lézích nabízí možnost jistého „neurotropizmu“ hluboké endometriózy [37]. Z toho důvodu se hyperalgezia u fyzického vyšetření vyskytuje signifikantně častěji u pacientek s hlubokým adenomyotickým uzlem (až v 96 %). Zde se předpokládá role nervového růstového faktoru (NGF – nerve growth faktor), která byla u hlubokých uzlů vyšší ve všech fázích cyklu s účastí specifického receptoru pro NGF/TrkA, který je exprimován ve všech nervech obklopených nebo invadovaných endometriózou.
Silná exprese NGF/TrkA cesty u adenomyotických uzlů může vysvětlit, proč tyto léze infiltrují v bohatě inervovaných anatomických lokacích [38]. Zánětlivé buňky (makrofágy, lymfocyty) a fibroblasty mají důležitou roli v tvorbě endometriotického intersticia prostřednictvím cytokinů [36].
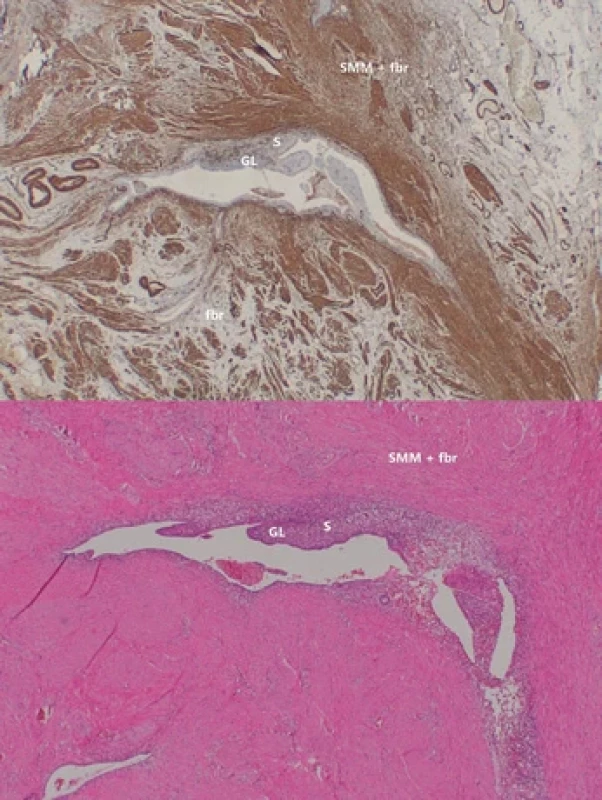
Hluboko infiltrující uzly jsou charakteristické sporým obsahem endometriálních buněk, které jsou obklopené myofibroblastovou komponentou s absencí stromatu (obr. 3) [34], což by mimo jiné mohlo vysvětlovat i variabilní reakci uzlů na hormonální terapii [39]. I když byly popsány léze se zvýšenou koncentrací receptorů v hladké svalovině léze, a u kterých lze předpokládat jistou míru progrese vlivem ženských pohlavních hormonů [40].
Existuje vztah mezi hypoperfuzním vzorem a velikostí uzlu [29]. To může být dáno vlivem oxidačního stresu, v důsledku chronického zánětlivého procesu, což může hrát zásadní roli v progresi hluboko infiltrující léze vedoucí k hyperaktivaci signální cesty a k rozvoji fibrózy [41]. Perzistující myofibroblastová aktivita způsobuje akumulaci a kontrakci kolagenové extracelulární matrix, progresivně expandující velikost uzlu a redukci vaskulární denzity [35].
Ze všeho výše uvedeného vyplývá, že ve fluorescenčním zobrazení lze očekávat u čerstvých lézí vzor spíše hyperperfuzní a u fibrotických lézí, což je většina hluboko infiltrujících ložisek, spíše vzor hypoperfuzní.
To by mohlo poskytnout teoretický základ vysvětlující prozatímní výsledky použití ICG v detekci a v pokusech o cílení resekce lézí endometriózy. Jednou z možností posuzování resekční linie by mohlo být zjišťování přítomnosti progresivní endometriózy (žlázky, stroma) v resekční linii. Fibróza v okolí nodulu je považována za součást těla, není progresivní, a proto může být ponechána in situ [42,43].
První publikovaná práce o použití ICG v detekci ložisek endometriózy je z roku 2014 [44]. Jednalo se o kazuistiku, která naznačila možný budoucí potenciál v detekci endometriálních lézí s použitím fluorescenčního zobrazení robotického systému Da Vinci Si. Autor počítal spíše se zvýrazněním vaskularizace dle stupně neovaskularizace léze.
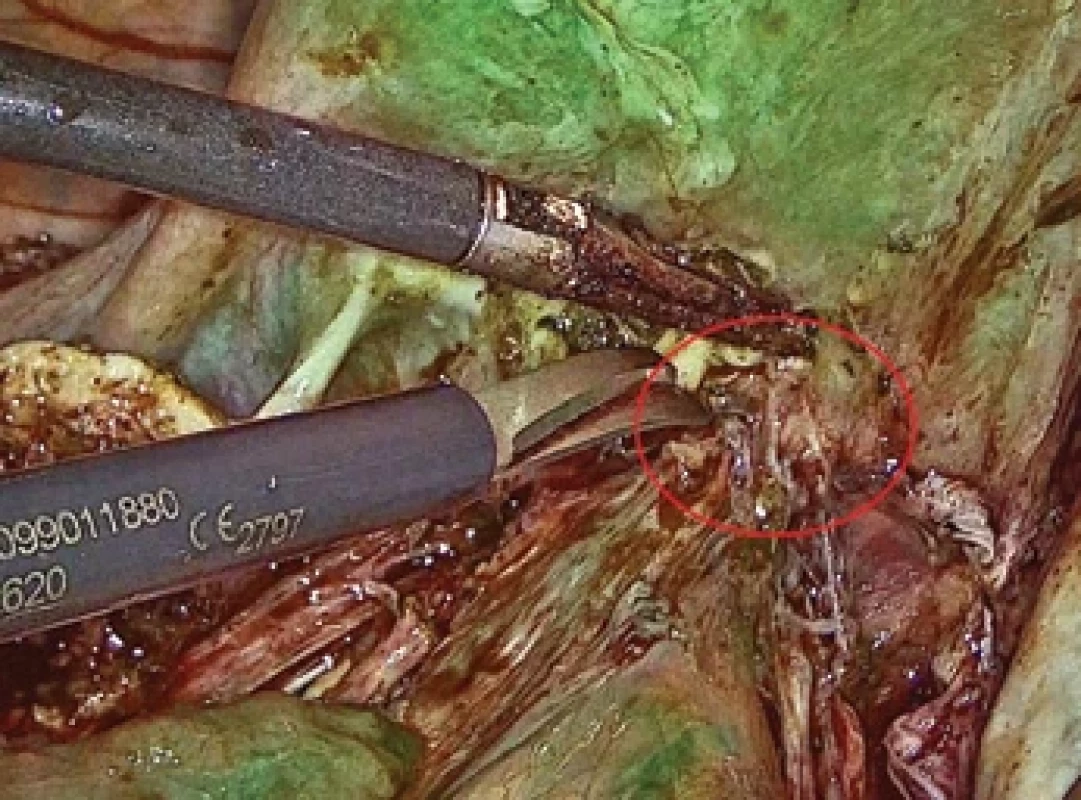
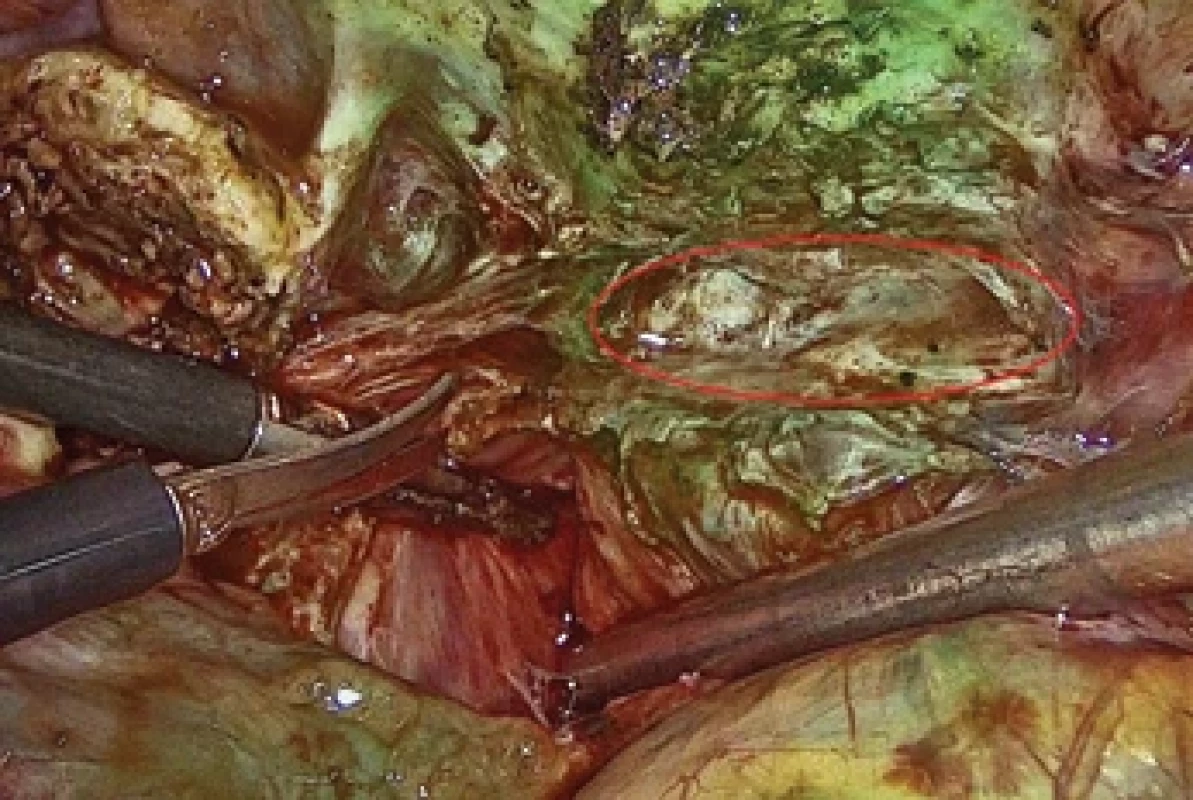
Jedna z dalších publikací od De Neefa et al. [10] z roku 2018 se snažila zjistit možný vliv intravenózního podání ICG při resekci hluboké infiltrující endometriózy rektovaginálního septa s plánovaným provedením shavingu rekta. Soubor čítal pouze šest pacientek, nebyla zaznamenána žádná perforace ani pooperační fistula v období do 16 měsíců po výkonu. Z práce vyplynulo, že kromě toho, že by tato technika mohla být nápomocná v rozlišení hluboké infiltrující endometriózy rektovaginálního septa od zdravé tkáně, mohla by být rovněž užitečná v rozhodování o nutnosti případného rozšíření resekce i na poševní fornix (obr. 4, 5). Poprvé byla vyslovena hypotéza, že fluorescencí vedená operace by mohla mít přínos v kompletní resekci bez nadměrné invazivity, a předpokládalo se využití zejména u pacientek s postižením svalové vrstvy rekta.
Publikace Siegenthaler et al. z roku 2020 [12] se snažila využít ICG v detekci ložisek endometriózy pro jejich polymorfní vzhled. Práce zahrnovala 63 subjektů. Závěrem práce bylo, že diagnostická hodnota NIR-ICG v identifikaci ložisek peritoneální endometriózy se jeví jako minimální. Jen při použití delší expozice (> 20 min) a bez anamnézy předchozích operačních výkonů byl zjištěn signifikantně pozitivní efekt na detekci. Obdobný efekt byl zjištěn i u ložisek hluboké endometriózy.
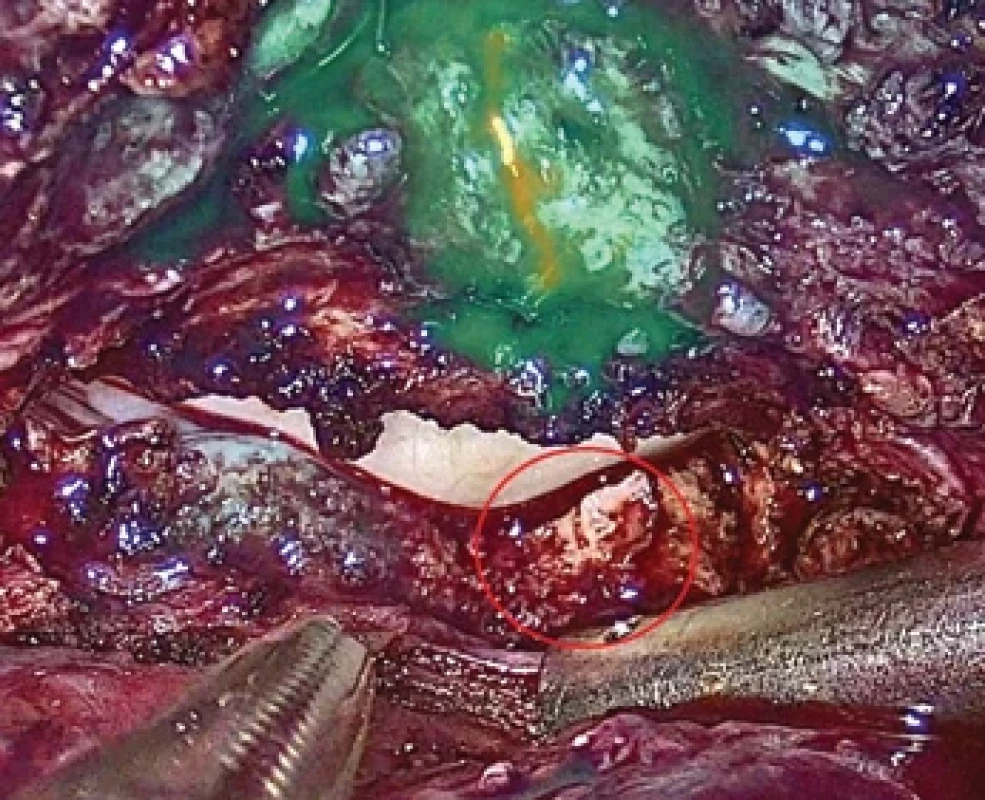
Další studie proveditelnosti je z roku 2020 od Bourdela et al. [9] s celkem 21 pacientkami a s laparoskopickým shavingem rekta pro hlubokou infiltrující endometriózu. Byla zaměřena spíše než na peroperační vedení resekce na hodnocení perfuze v oblasti místa resekce, a to jak v oblasti fornixu pochvy, tak i rekta. Nebyly pozorovány žádné závažné per - ani pooperační komplikace. Závěrem byla tato metoda zhodnocena jako potenciálně přínosná při prevenci vzniku pooperačních komplikací, zejména rektovaginálních píštělí, v jejichž etiopatogenezi se předpokládá právě významná role ischemie v operované oblasti (obr. 6).
Turco et al. [11] publikovali v roce 2021 prospektivní studii čítající 51 pacientek, kde se prokázal vliv na detekci zejména okultních lézí, kdy NIR-ICG jako doplňkové zobrazení v kombinaci se zobrazením ve viditelném spektru ukázalo vynikající úroveň detekce.
Vizzielli et al. [45] v roce 2020 popsali retrospektivní multicentrickou case control studii na 20 případech operovaných roboticky ve srovnání s 27 pacientkami v kontrolní skupině operovaných laparoskopicky. Primárním cílem bylo zaměření se na již zmiňované okultní léze. Dle celkové detekce se ukázalo, že NIR-ICG zobrazení by mohlo být dobrým diagnostickým a screeningovým testem.
Ianieri et al. [46] v roce 2020 provedli metaanalýzu 17 prací pojednávajících o využití ICG v léčbě endometriózy. V osmi z nich byla potvrzena užitečnost využití ICG. V osmi se také zjistila užitečnost v hodnocení vaskularizace u intestinálních anastomóz, což v současnosti patří ke standardnímu využití v gastrointestinální chirurgii. Jedna randomizovaná a jedna prospektivní studie ale užitečnost použití nepotvrdily. Užitečnost v detekci endometriózy při operaci tak zatím vykazuje jistou míru inkonzistence.
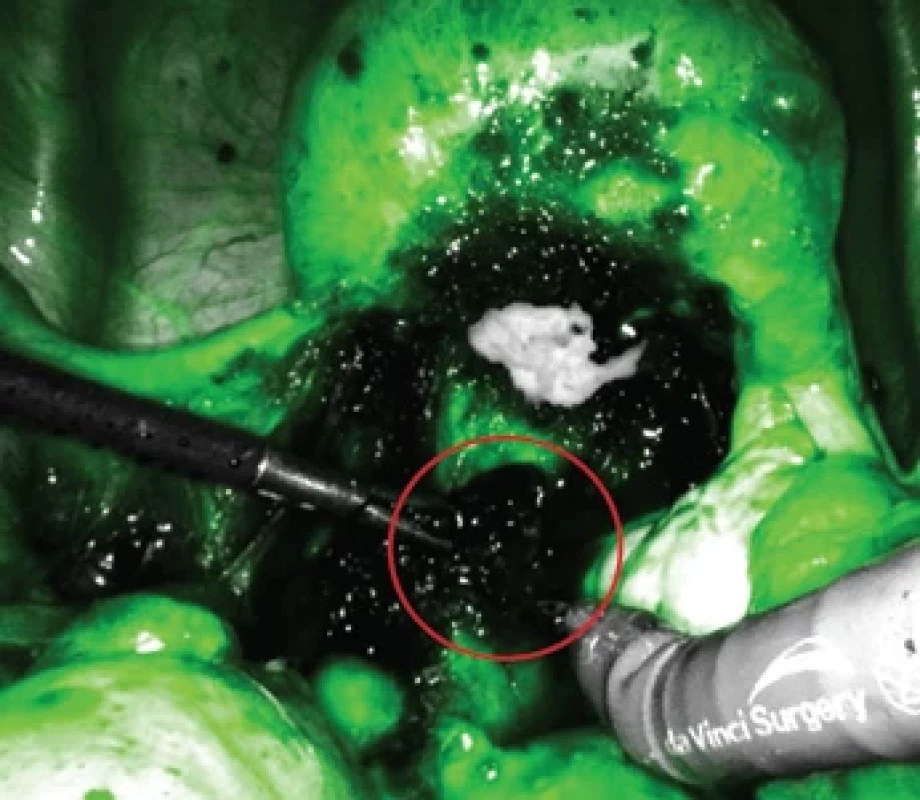
Dle histopatologického obrazu v práci Raimonda et al. [29] z roku 2020 bylo na souboru 30 pacientek zjištěno, že až 60 % hluboko infiltrujících uzlů v oblasti rekta mělo hypoperfuzní vzor, u 40 % byl popsán vzor hyperperfuzní. Byla dokonce popsána korelace mezi perfuzí a velikostí uzlu. U větších uzlů dominoval spíše hypoperfuzní vzor (obr. 7) [29].
Většina dnes dostupných důkazů ve využití fluorescence u resekčních výkonů hluboko infiltrující endometriózy je na úrovni ojedinělých kazuistik, studií proveditelnosti a empirických zkušeností operatérů [9–12,45]. V podstatě chybí vědecký důkaz vlivu využití fluorescenčního barviva na resekční linii na histopatologické úrovni a od toho se odvíjející potenciál na patogenezi orientovaný management onemocnění endometriózou. Je proto potřeba více prospektivních studií, které se budou věnovat této problematice. V současnosti připravujeme multicentrickou, prospektivní, randomizovanou, kontrolovanou studii vlivu ICG vedené resekce na charakteristiku resekční linie u pacientek se stadiem endometriózy rekta C2 dle #ENZIAN. Protokol studie IRRLA (Indocyanine Green for Rectal Endometriosis Resection Line Assessment) budeme publikovat samostatně v blízké době.
Závěr
Molekula ICG má jedinečné chemické vlastnosti, dobrý bezpečnostní profil a prokázanou účinnost v hodnocení perfuze tkání.
Využití NIR-ICG perfuze tkání k cílení resekce nejen u maligních, ale i u závažnějších forem benigních onemocnění, jako jsou například ložiska hluboké infiltrující endometriózy, by mohlo mít vliv na cílení resekčního výkonu, omezení rizika nadměrné resekce a mohlo by umožnit nervy šetřící operování a redukci rizika závažných komplikací. Využití fluorescenčního barviva by mohlo mít přínos v managementu orientovaném na patogenezi onemocnění. V budoucnosti je potřeba prospektivních studií s dostatečně velkou kohortou, které by přinesly dostatečný důkaz, že tento přístup má klinické opodstatnění a vliv na kvalitu života pacientek.
Zdroje
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicínaČlánek vyšel v časopise
Česká gynekologie

2025 Číslo 3
-
Všechny články tohoto čísla
- Shromáždění členů
- Analýza rizikových faktorov rastu plodu – vplyv maternálnych faktorov a kongenitálnej cytomegalovírusovej infekcie
- Vzdělávací hodnota chirurgických videí na YouTube – hodnocení kvality a soubor standardů videí o hysterektomii pomocí transluminální endoskopické operace s přirozeným vaginálním vstupem
- Účinnost fyzioterapie na úlevu od bolesti a funkční zotavení po císařském řezu
- Souvislost mezi hladinou kisspeptinu v séru v I. trimestru a prenatálními komplikacemi
- Hysterosalpingografické vyšetření po léčbě mimoděložního těhotenství
- Pozdní prenatální diagnostika kompletní pentalogie Cantrella
- Raritní děložní malignita dětského věku kombinovaná s kompletní inverzí dělohy
- Možnost využití indocyaninové zeleně v managementu endometriózy
- Gastroschíza u plodu – současné možnosti prenatální diagnostiky a následný management
- Robsonova klasifikácia – cesta k zníženiu počtu cisárskych rezov?
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Účinnost fyzioterapie na úlevu od bolesti a funkční zotavení po císařském řezu
- Analýza rizikových faktorov rastu plodu – vplyv maternálnych faktorov a kongenitálnej cytomegalovírusovej infekcie
- Robsonova klasifikácia – cesta k zníženiu počtu cisárskych rezov?
- Gastroschíza u plodu – současné možnosti prenatální diagnostiky a následný management
