Klinicky významné histopatologické charakteristiky a biomarkery karcinomu endometria
Clinically relevant histopathological features and biomarkers in endometrial cancer
Objective: To provide an overview of the most important histopathological characteristics and biomarkers of endometrial carcinoma that have clinical relevance for prognosis, prediction of treatment response, and decision-making regarding adjuvant therapy. Methods and results: Endometrial carcinoma represents the most common malignancy of the female reproductive tract in developed countries. Disease prognosis is determined not only by the anatomical extent, but also by a number of non-anatomical factors. The histological tumour type, presence of lymphovascular space invasion, and specific patterns of myometrial invasion (such as the MELF pattern) play major roles. Current molecular classification divides endometrial carcinomas into four groups (POLEmut, MMRd, NSMP, and TP53mut), which differ in prognosis as well as in therapeutic response. Additional clinically applicable biomarkers include oestrogen and progesterone receptors, L1CAM, HER2, CA125, and HE4. Emerging research focuses on novel biomarkers such as TROP2, circulating tumour DNA (ctDNA), circular RNA (circRNA), tumour - -infiltrating lymphocytes (TILs), and folate receptor alpha (FRa). These markers enable more precise risk stratification and identification of patients suitable for targeted therapies. Integration of multiple biomarkers with clinicopathological parameters further enhances the accuracy of risk assessment and prediction of treatment response. Conclusion: Incorporating histopathological features and biomarkers into routine clinical practice allows for a more accurate estimation of prognosis and a more rational selection of adjuvant therapy. An increasing number of non-anatomical biomarkers are becoming an integral part of the decision-making algorithm in endometrial carcinoma management.
Keywords:
Prognosis – histopathology – biomarkers – targeted therapy – Endometrial carcinoma – molecular classification
Autoři:
B. Sehnal 1
; J. Drozenová 2
; L. Vaněk 1
; M. O. Ndukwe 3
; M. J. Halaška 1
; M. Hruda 1
; L. Rob 1
; R. Matěj 2,4
Působiště autorů:
Gynekologicko-porodnická klinika 3. LF UK a FNKV, Praha
1; Ústav patologie, 3. LF UK a FNKV, Praha
2; Porodnická a gynekologická klinika LF UK a FN Hradec Králové
3; Ústav patologie a molekulární medicíny, 3. LF UK a FTN, Praha
4
Vyšlo v časopise:
Ceska Gynekol 2026; 91(2): 131-141
Kategorie:
Přehledová práce
doi:
https://doi.org/10.48095/cccg2026131
Souhrn
Cíl studie: Poskytnout přehled nejdůležitějších histopatologických charakteristik a biomarkerů endometriálního karcinomu, které mají klinický význam pro prognózu, predikci odpovědi na léčbu a rozhodování o adjuvantní terapii. Metodika a výsledky: Endometriální karcinom je nejčastější malignitou ženského reprodukčního traktu v rozvinutých zemích. Prognóza onemocnění je určena nejen anatomickým rozsahem onemocnění, ale i řadou neanatomických faktorů. Významnou roli hraje histologický typ nádoru, přítomnost lymfovaskulární invaze nebo specifický vzorec invaze do myometria (MELF). Současná molekulární klasifikace rozděluje karcinomy do čtyř skupin (POLEmut, MMRd, NSMP a TP53mut), které se liší prognózou i odpovědí na terapii. Mezi další klinicky využitelné biomarkery patří estrogenové a progesteronové receptory, L1CAM, HER2, CA125 a HE4. Perspektivní výzkum se zaměřuje na nové biomarkery, jako jsou TROP2, cirkulující nádorová DNA (ctDNA), kruhové RNA (circRNA), TILs a folátový receptor alfa (FRa). Tyto markery umožňují lepší stratifikaci rizika a identifikaci pacientek vhodných pro cílenou léčbu. Kombinace více biomarkerů s klinicko-patologickými charakteristikami zvyšuje přesnost stratifikace rizika a predikce odpovědi na zvolenou terapii. Závěr: Integrace histopatologických znaků a biomarkerů do rutinní praxe umožňuje přesnější odhad prognózy a racionálnější volbu adjuvantní terapie. Stále větší počet neanatomických biomarkerů se u karcinomu endometria stává nedílnou součástí rozhodovacího algoritmu.
Klíčová slova:
prognóza – biomarkery – endometriální karcinom – cílená léčba – histopatologie – molekulární klasifikace
Úvod
Karcinom endometria (EC – endometriální karcinom) je ve vyspělých zemích nejčastější malignitou ženského reprodukčního traktu [1]. Globální incidence malignit děložního těla zůstává v posledních letech relativně stabilní, v roce 2022 byl počet nově diagnostikovaných případů stanoven na 420 242 (97 704 úmrtí), což odpovídá kumulativnímu celoživotnímu riziku 1,01 % do věku 74 let [2]. Česká republika vykazuje jednu z nejvyšších incidencí – v roce 2019 dosáhla nejvyšší hodnoty 37,1 nových případů na 100 000 žen [3].
Zatímco většina případů EC má dobrou prognózu, určité podtypy se chovají agresivně a často recidivují. Prognóza pacientek je zásadně ovlivněna nejen anatomickým rozsahem onemocnění (velikost tumoru, hloubka myometrální invaze, infiltrace stromatu děložního hrdla, postižení lymfatických uzlin), ale i celou řadou neanatomických faktorů, které jsou předmětem intenzivního výzkumu. V roce 2021 vydaly tři evropské odborné společnosti – Evropská společnost pro gynekologickou onkologii (ESGO – European Society of Gynaecological Oncology), Evropská společnost pro radioterapii a onkologii (ESTRO – European Society for Radiotherapy and Oncology) a Evropská patologická společnost (ESP – European Society of Pathology) – společné doporučené postupy pro diagnostiku, léčbu a sledování pacientek s karcinomem endometria, které při definování rizikových skupin inkorporovaly – mimo anatomický rozsah onemocnění i další neanatomické prognostické faktory. Definice rizikových skupin se liší, pokud je znám výsledek molekulární klasifikace nádoru [4,5]. Velkou změnou v nahlížení na etiopatogenezi EC bylo začlenění histokopatologických a molekulárních veličin do definice stadií I a II v novém stagingovém systému karcinomu endometria FIGO 2023 [6,7]. Neustále se studují další nonanatomické parametry, které by vedle stanovení spolehlivé diagnostiky mohly umožnit přesnější odhad prognózy, poskytnout cílenou terapii a sledovat úspěšnost léčby v rámci follow up [8].
Histopatologický typ nádoru
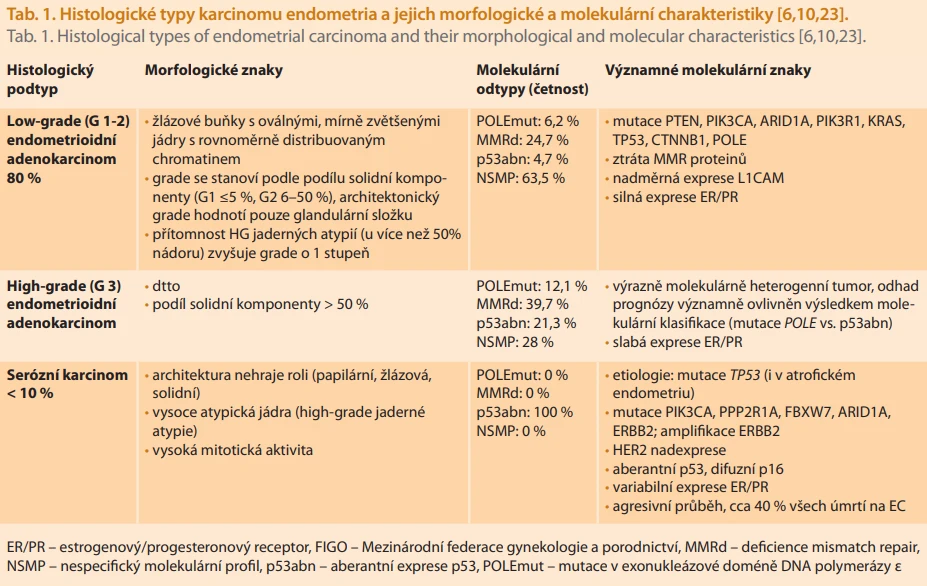
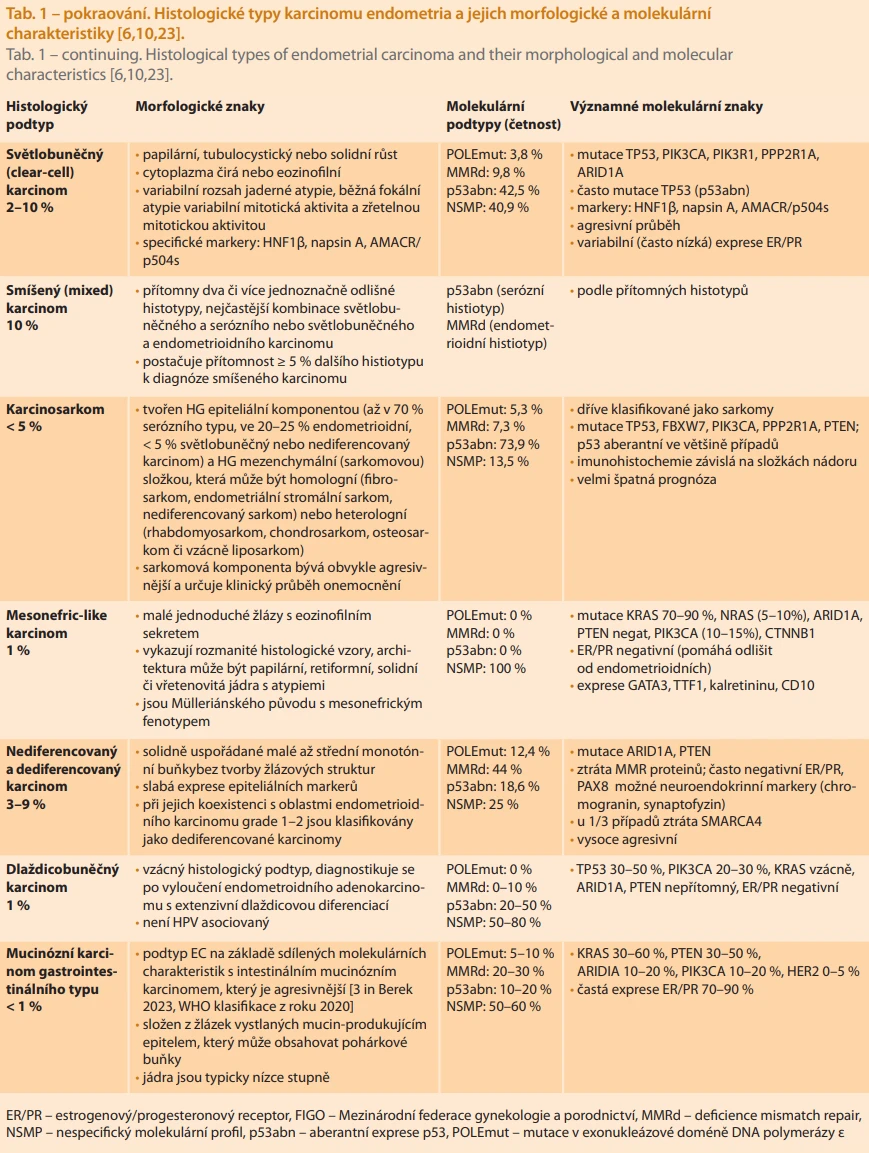
Histologický typ EC zůstává zásadním prognostickým faktorem [5,6]. EC představuje histologicky heterogenní malignitu, která byla v roce 1983 rozčleněna podle svých vlastností a prognózy na typ I a typ II [8,9]. Typ I EC (80–90 % všech případů), estrogen dependentní endometroidní adenokarcinom s absencí specifických genetických determinant, je spojen s příznivou prognózou a etablovanými rizikovými faktory (hyperestrogenizmus, obezita, metabolický syndrom, syndrom polycystických ovarií, nulliparita). Typ II EC, nonestrogen dependentní, zahrnuje histologicky různorodou skupinu agresivních nádorů s výrazně horší prognózou a 5letým přežitím okolo 50 % [8]. Přestože je tato klasifikace široce využívána, nedokáže plně postihnout heterogenitu EC [8]. Také Mezinárodní federace gynekologie a porodnictví (FIGO – International Federation of Gynaecology and Obstetrics) rozlišuje neagresivní histologické typy s dobrou prognózou (low-grade 1 a 2 endometroidní karcinom) a agresivní histologické typy s horší prognózou (grade 3 endometroidní, serózní, světlobuněčný, smíšený, nediferencovaný, karcinosarkom a některé další vzácné histiotypy) [6]. Tyto histologické podtypy vykazují odlišné molekulární profily, histopatologické znaky, prekurzorové léze i klinické chování (tab. 1) [6,10,11]. Zcela odlišné chování agresivních a neagresivních histologických typů je tak zásadní, že se toto dělení promítlo i do stagingového systému FIGO 2023 [6,7].
Lymfovaskulární invaze
Lymfovaskulární invaze (LVSI – lymphovascular space invasion) je při histopatologickém hodnocení charakterizována přítomností nádorových buněk ve strukturách vystlaných endotelem mimo primární nádorovou masu (tzn. v lymfatických či krevních cévách). Ačkoli je LVSI přítomna pouze u menšiny případů endometriálního karcinomu, její průkaz představuje klíčový prognostický ukazatel rizika recidivy a metastáz. Např. v dánské kohortové studii zahrnující 3 377 pacientek s EC byla přítomnost podstatné LVSI nezávislým 5letým prediktorem recidivy (39,0 vs. 10,5 %; HR – hazard ratio 4,7) [12]. V jiné kohortě 524 pacientek ve stadiu I (FIGO 2009) byla podstatná LVSI spojena se signifikantně nižším 5letým celkovým přežitím (OS – overall survival) (70,6 vs. 99,5 %; p < 0,001) a byla identifikována jako vůbec nejsilnější rizikový prognostický parametr pro OS (HR = 11,9; p = 0,001) [13].
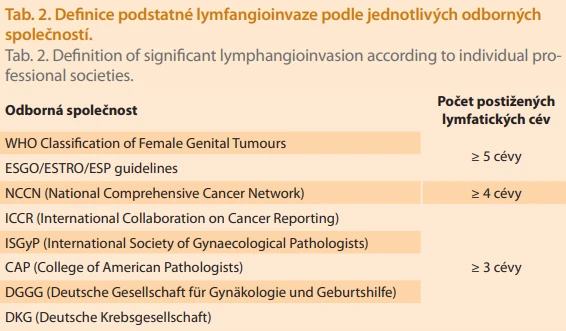
Klinicky významné je rozlišení mezi podstatnou (substantial) neboli extenzivní (extensive) a fokální (focal) LVSI [6,14]. Podstatná LVSI jako důležitý nezávislý a významný negativní prognostický faktor byla začleněna do společných doporučených postupů evropských odborných společností ESGO/ESTRO/ESP [4,5] a také do stagingu FIGO 2023 [6]. Nicméně i fokální LVSI bývá spojována s nepříznivou prognózou. Ve studii zahrnující 1 555 pacientek s EC ve stadiu I dle FIGO 2009 byla zaznamenána 5letá míra přežití bez progrese u 68,7 % pacientek s podstatnou LVSI, u 70,5 % pacientek s fokální LVSI a u 90,7 % případů bez přítomnosti LVSI (p < 0,001) [15]. Jiné výsledky přinesla studie PORTEC. Mezi pacientkami s EC bez zevní radioterapie byla 5letá frekvence recidivy v pánevních lymfatických uzlinách u 3,3 % LVSI negativních případů, u 6,7 % případů s fokální LVSI (postižení 1–3 cév; p = 0,51) a u 26,3 % u případů s podstatnou LVSI (postižení ≥ 4 cév; p < 0,001) [16]. Problémem zůstává nejednotná definice pro podstatnou LVSI mezi různými odbornými společnostmi (tab. 2) [14].
MELF
Microcystic, elongated and fragmented (MELF) představuje specifický histopatologický typ myometriální invaze u endometroidního karcinomu endometria. Žlázová architektura procházejí morfologickou přeměnou do mikrocystických (dilatovaných), protáhlých a fragmentovaných (nepravidelných) struktur. Tyto žlázky mohou pronikat do myometria jako jednotlivé buňky nebo mohou vytvářet malé shluky buněk [17]. Prognostický význam MELF vzorců u endometroidního endometriálního karcinomu (EEC) zůstává předmětem probíhající diskuze. Většina studií neprokázala statisticky významný negativní dopad MELF invaze na klinické výsledky, avšak několik studií uvádí opačné závěry [17–20]. Někteří autoři dokonce doporučují, aby přítomnost MELF byla zohledněna při rozhodování o adjuvantní terapii [19]. Přestože je MELF často spojován s jinými nepříznivými prognostickými faktory (LVSI, hlubokou invazí do myometria, metastázami do lymfatických uzlin) a s agresivním biologickým chováním nádoru, jeho definitivní prognostický význam zůstává nejasný vzhledem k rozporuplným datům a absenci rozsáhlých prospektivních studií [20].
Molekulární klasifikace
Cancer Genome Atlas (TCGA) dělí EC do čtyř molekulárních skupin s odlišnou prognózou [4–6,10,21–23]:
1. POLEmut (inaktivace DNA polymerázy e POLE, ultramutovaný);
2. MMRd (mismatch repair deficient, hypermutované s mikrosatelitovou nestabilitou – MSI);
3. NSMP (no specific molecular profile, copy number low);
4. TP53mut (mutace/abnormalita genu TP53, označovaná také jako p53abn, copy number high).
Problematika molekulární klasifikace EC byla na stránkách České gynekologie publikována opakovaně [7,21,22,24,25].
Estrogenové a progesteronové receptory
Estrogenové (ER) a progesteronové (PR) receptory představují u EC klíčové biomarkery, jejich pozitivita je spojována s příznivou prognózou, a naopak ztráta s agresivními EC [26,27]. Jedná se o jaderné proteiny vázající hormony estrogen a progesteron, čímž regulují genovou expresi a ovlivňují buněčnou proliferaci a diferenciaci. ER existuje ve více izoformách, přičemž ERa obvykle stimuluje proliferaci buněk, zatímco ERb má spíše antiproliferativní a proapoptický účinek a může tlumit funkci Era [28]. V časných stadiích EC bývá exprese ERa vyšší, zatímco v pokročilých stadiích je patrný pokles ERb. Ztráta ER (zejména ERa) je spojena s horší prognózou, vyšším rizikem recidivy a častější metastázou do lymfatických uzlin. PR se vyskytuje ve více jaderných i membránových izoformách a jeho exprese je ovlivněna estrogenovou signalizací – exprese ERa stimuluje PR, zatímco ERb ji může potlačovat. Ztráta PR může být důsledkem nádorové transformace, vede k relativní převaze estrogenového stimulu a podporuje proliferaci [28].
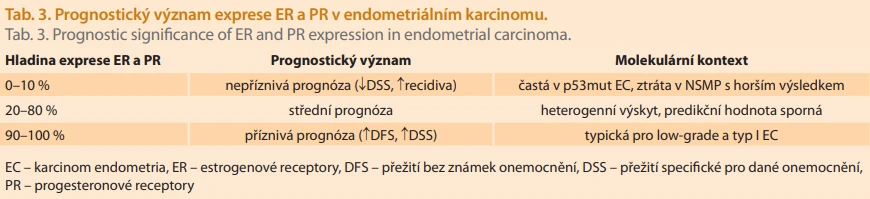
Podle výsledků recentní studie umíraly pacientky s EC s molekulární skupinou NSMP během 5 let od stanovení diagnózy výrazně častěji, pokud byly ER negativní a/nebo měly histologický grade 3 (HR 16,3) [29]. Jiná studie na 648 případech ukázala, že pouze ER pozitivita byla nezávisle spojena se sníženým rizikem recidivy (HR 0,33) u vysoce rizikových endometriálních karcinomů ve skupině NSMP [30]. Aktuálně používaný práh pozitivní exprese ER a PR není u EC jednotný (nejčastěji > 1 %, nebo > 10 %) a je převzat z výzkumu karcinomu prsu [27]. V poslední době se prosazuje upravený tříúrovňový model rizikové stratifikace, který prokázal zlepšení predikční hodnoty ve srovnání s běžně používaným 10% prahem (tab. 3) [27]. Pacientky s expresí ER 90–100 % dosáhly signifikantně lepší specifické přežití (DSS – disease - -specific survival) ve srovnání se skupinami s expresí ER 20–80 % (p < 0,001) a ER 0–10 % (p < 0,001), a to jak v celé kohortě, tak v jednotlivých molekulárních skupinách. Dokonce i pacientky s prokázanou p53abn a s expresí PR 90–100 % vykázaly vynikajícího 5letého DSS. Kupodivu v molekulární skupině NSMP byl na rozdíl od ostatních molekulárních skupin identifikován jako signifikantní práh ztráty exprese ER < 10 % a využití tříúrovňové stratifikace nemá v této molekulární skupině význam [27]. Proto někteří autoři navrhují u pacientek s ER pozitivitou a profilem NSMP EC zvážit deeskalaci léčby [29].
L1CAM
L1 buněčná adhezní molekula (L1CAM – L1cell adhesion molecule) je transmembránový imunoglobulinový glykoprotein, který hraje zásadní roli ve vývoji nervové soustavy při migraci neuronů a navigaci axonů [31]. U nádorů se L1CAM podílí na podpoře buněčné motility, invazivity, chemorezistence a metastazování. Nadměrná exprese L1CAM je v EC častěji pozorována u agresivnějších (neendometroidní histologické typy, grade 3, LVSI) a pokročilejších EC s extrauterinním šířením a slouží jako prediktor nepříznivého klinického výsledku [31,32].
V multivariační analýze 1 021 pacientek s EC ve stadiu I byla exprese L1CAM nezávislým prediktorem pravděpodobnosti vzniku recidivy (HR 16,33; p < 0,001) a úmrtí (HR 15,01; p < 0,001). Na základě těchto výsledků autoři konstatují, že zařazení L1CAM do preoperačního rizikového skóre může pomoci identifikovat pacientky, u nichž je vhodnější rozšířená chirurgická stagingová operace nebo časnější indikace adjuvantní terapie [33]. Giannini et al. zahrnuli do své studie 548 pacientek s EC ve stadiu I a pozitivita L1CAM byla zaznamenána u 10–15 % všech pacientek. Výsledky této studie prokázaly, že vyšší exprese L1CAM (> 10 % nádorových buněk) prokázaná již v preoperačních vzorcích z endometriální biopsie byla asociována s přítomností mikrometastáz v pánevních lymfatických uzlinách (OR – odds ratio 5,76; p = 0,015), přítomností vzdálených metastáz (HR 4,08; p = 0,001) a časného relapsu do 3 let (p < 0,001). Horší prognóza byla i u pacientek, které podle běžných parametrů spadaly do nízkorizikové skupiny [31]. Také publikovaná metaanalýza prokázala, že vysoká exprese L1CAM je významně spojena se zkráceným celkovým přežitím (HR 2,16; p < 0,001) i přežitím bez recidivy (DFS – disease-free survival; p < 0,001) a tento vztah přetrvává nezávisle na stadiu nemoci, metodě detekce a použitém cut-off [32]. Výsledky studií podporují zařazení L1CAM mezi doplňkové biomarkery jak pro předoperační stratifikaci rizika při rozhodování o rozšířeném chirurgickém stagingu, tak při rozvaze o adjuvantní terapii. Na druhou stranu zatím není ujasněna role L1CAM v monitoraci po ukončení léčby a je předmětem probíhajícího výzkumu [31,32].
HER2 protein
HER2 protein (human epidermal growth factor – receptor 2 kódovaný genem HER2) je transmembránový tyrosinkinázový receptor, který se v posledních letech stal významným terapeutickým cílem u karcinomů prsu, gastrointestinálního traktu a serózního karcinomu endometria. HER2 aktivuje signální dráhy MAPK a PI3K, čímž podporuje karcinogenezi ovlivněním buněčné proliferace, diferenciace a apoptózy. Vysoká exprese HER2 byla zaznamenána u přibližně 1 % všech pacientek s endometrioidním EC, ale až u 44 % serózních EC [10,34].
Mimo prognostickou hodnotu poskytuje HER2 jako cílový marker i terapeutický potenciál. Randomizovaná studie fáze II prokázala, že kombinace trastuzumabu s karboplatina-paklitaxelem a následnou udržovací léčbou vedla u pacientek s pokročilým nebo recidivujícím HER2 pozitivním serózním EC k významnému prodloužení přežití bez progrese (PFS – progression-free survival; HR 0,44; p = 0,015) a celkového přežití OS (HR 0,49; p = 0,04) [10]. Podle doporučení NCCN (National Comprehensive Cancer Network USA) by měl být trastuzumab součástí první linie systémové léčby u pacientek s pokročilým HER2 pozitivním serózním EC. U HER2 pozitivních neserózních nádorů by se jeho podání mělo rovněž zvážit, i když terapeutický potenciál v high grade endometroidních EC je dosud nejasný [34].
CA125 a HE4
Cancer antigen 125 (CA125) a human epididymis protein 4 (HE4) jsou biomarkery často využívané při diagnostice, prognóze a sledování léčby ovariálních a také endometriálních karcinomů. Cirkulující biomarker CA125 je kódován genem MUC16, jedná se o antigenní determinant (epitop) na extracelulární části proteinu MUC16 (membránově vázaný glykoprotein ukotvený v membráně epitelových buněk). Sérový glykoprotein HE4 je kódován genem WFDC2 a patří do rodiny proteinů s WAP doménou (Whey Acidic Protein domain, proteázové inhibitory) [26]. Vysoké hladiny HE4 i CA125 v séru korelují s horší prognózou EC, vč. agresivnějších forem s metastázami do lymfatických uzlin, invazí do myometria a postižením cervixu [35–37]. CA125 se jako makromolekulární antigen podílí na tumorogenezi, buněčné proliferaci a metastázování u různých typů malignit. Metaanalýza 25 studií zahrnující 7 716 pacientek s EC vypočítala, že zvýšené hladiny CA125 jsou statisticky významně asociovány jak s kratším celkovým přežitím OS (HR 1,848; p < 0,001), tak s přežitím specifickým pro onemocnění (DSS – disease-specific survival) (HR 2,854; p < 0,001) [36]. Podle jiné studie predikují vyšší hodnoty CA125 metastázy do lymfatických uzlin se senzitivitou a specificitou 0,78 [38]. Nicméně přestože se jedná o poměrně senzitivní nádorový marker, hladiny CA125 jsou často zvýšené i při neonkologických stavech (menstruace, gravidita, zánět, endometrióza, neonkologický ascites) [36].
Vyšší senzitivitu než CA125 vykazuje pro EC sérový maker HE4, a to jak pro diagnostiku (senzitivita 0,71 vs. 0,35) [39], tak pro invazi do myometria (senzitivita 0,76 vs. 0,65) [40] a pro metastázy do lymfatických uzlin (senzitivita 0,82 vs. 0,72) [41]. HE4 je nadměrně exprimován převážně v serózních a endometroidních typech ovariálního karcinomu. Ačkoli přesná funkce HE4 není dosud plně objasněna, jeho nadměrná exprese podporuje buněčnou adhezi a migraci, zatímco jeho potlačení významně inhibuje růst tumoru [42]. Význam monitorování hladin HE4 se zvyšuje při fertilitě zachovávající terapii EC. V prospektivní studii sérové hladiny HE4 nezávisle predikovaly selhání léčby progestinem ve studii 76 žen s EC nebo atypickou hyperplazií endometria (adjustovaný HR 0,97; p = 0,008) [43]. V jiné multicentrické randomizované studii na 153 ženách s hyperplazií endometria změny v expresi HE4 významně korelovaly s odpovědí na terapii progestiny (p < 0,001), i když nepredikovaly riziko recidivy (p > 0,05) [42]. Biomarkery HE4 a CA125 tedy představují nástroje pro diagnostiku, prognózu a sledování průběhu léčby EC, vč. fertility zachovávajících postupů, ale jejich role je doplňková a měly by být interpretovány v kontextu dalších klinických parametrů.
TROP2
Trophoblast cell surface antigen 2 (TROP2) je transmembránový glykoprotein typu I kódovaný genem TACSTD2. TROP2 se za fyziologických podmínek vyskytuje pouze v malé míře ve vybraných epitelech (původně identifikován v lidských trofoblastech), avšak je nadměrně exprimován v mnoha typech solidních malignit včetně EC. Hraje určitou roli v proliferaci, obnově a migraci buněk, a tím ovlivňuje karcinogenezi [44]. Vysoká exprese TROP2 je spojena s agresivními EC (převážně serózní karcinom, karcinosarkom) a také s rezistencí k chemoterapii [45,46]. Tento biomarker by mohl sloužit jako potenciální prognostický faktor a hlavně jako perspektivní terapeutický cíl a prediktor odpovědi na cílenou léčbu. Pacientky s exprimovaným TROP2 mohou profitovat z léčby pomocí specifických protilátek nebo terapie ADC (antibody-drug conjugate, léčivo konjugované s protilátkou). ADC sacituzumab govitecan (např. Trodelvy®) byl již schválen pro léčbu metastatického karcinomu prsu a uroteliálního karcinomu a intenzivně se studuje jeho použití i u jiných malignit včetně EC. Integrace TROP2 do klinické praxe představuje slibný krok směrem k personalizované onkologické péči [44,46].
ctDNA
Cirkulující nádorová DNA (ctDNA – circulating tumor DNA) je tvořena malými fragmenty DNA uvolněnými z nádorových buněk. Pokrok v oblasti sekvenčních technologií umožnil detekci již minimálních množství volné DNA cirkulující v séru a analýza těchto fragmentů byla schopna identifikovat různé genetické mutace nádoru. Vysoké hladiny ctDNA jsou asociovány s vyšší agresivitou tumoru, pokročilým stadiem onemocnění a zvýšeným rizikem recidivy [47,48]. Negativita ctDNA byla u pacientek s EC identifikována jako nezávislý prognostický faktor pro DFS (HR 3,864) spolu s grade 1 (HR 1,976) a pooperační hladinou CA125 < 19 U/ml (HR 3,740) [49]. A naopak nedetekovatelná hladina ctDNA byla po adjuvantní terapii signifikantně asociována s delším PFS (p = 0,0011) a OS (p = 0,0194) v retrospektivní studii na 44 pacientkách [50]. Slibný biomarker ctDNA nabízí určitý potenciál pro diagnostiku, odhad prognózy i sledování odpovědi na léčbu u některých pacientek s EC. Jeho přesný význam a implementaci do klinické praxe je ale potřeba verifikovat dalšími prospektivními studiemi.
circRNAs
Kruhové RNAs (circular RNAs, circRNAs) představují transkripty či segmenty nekódujících RNA, které regulují široké spektrum biologických procesů v buňce. CircRNAs ovlivňují proliferaci, migraci, angiogenezi i imunitní odpověď, čímž modifikují nádorové mikroprostředí a ovlivňují invazivní šíření malignit. Předpokládá se, že molekuly circRNAs hrají významnou roli také v patofyziologii EC, a to mimo jiné prostřednictvím regulace genové exprese a modulace signální dráhy PI3K/AKT/mTOR [8]. Např. bylo zjištěno, že u obézních pacientek s EC je exprese circRNAs v nádorové tkáni snížena přibližně o 40 % oproti zdravé tkáni [51] a rozdíl v expresi byl patrný obzvláště v nízce diferencovaných karcinomech [52]. Vzhledem ke své kovalentně uzavřené kruhové struktuře jsou circRNAs mimořádně stabilní v tělních tekutinách a uvolňují se do krevního oběhu zabalené v exozomech nebo mikrovezikulách. Tato stabilita z nich činí perspektivní neinvazivní diagnostické, prognostické a terapeutické biomarkery využitelné nejen u EC, ale i u dalších solidních nádorů (karcinom prsu, jater, žaludku) [8]. Nicméně jejich úloha v patogenezi EC zatím není plně objasněna, ale klinické využití circRNAs představuje u EC slibnou oblast výzkumu (např. klinické studie NCT04464122 a NCT05771337). Pozornost se rovněž soustředí na využití circRNAs v imunoterapii při tvorbě protinádorových vakcín, při podpoře účinnosti inhibitorů imunitních kontrolních bodů (ICI – immune checkpoint inhibitors, např. PD-1/PD-L1) či při terapiích založených na uměle vytvořených chimérických antigenních receptorech (CAR – chimeric antigen receptor). Tyto receptory umožňují imunitním buňkám, vč. T-lymfocytů, NK buněk či makrofágů, cíleně rozpoznat a eliminovat nádorové buňky [8].
TILs
Lymfocyty infiltrující nádor (TILs – tumor-infiltrating lymphocytes) představují imunitní buňky (zejména CD8+ T-lymfocyty), které migrují z okolní tkáně do nádorového parenchymu v rámci protinádorové imunitní odpovědi organizmu [53]. V posledních letech se ukazuje, že pouhá kvantifikace počtu imunitních buněk nepostačuje pro přesnou predikci odpovědi na imunoterapii – zásadní význam má prostorová distribuce imunitních buněk ve vztahu k nádorovým strukturám. Rozdílné prostorové uspořádání imunitních buněk by mohlo vysvětlit značnou heterogenitu EC v rámci jedné molekulární skupiny, a to včetně rozdílů v odpovědi na identickou léčbu.
Hattori et al. popsali tři základní imunofenotypy EC:
1. inflamed (zánětlivý) – s bohatou intratumorální infiltrací CD8+ T-buněk, typicky v POLEmut/MMRd, spojený s příznivější prognózou;
2. excluded (imunitně vyloučený, opuštěný) – CD8+ T-buňky přítomné pouze v peritumorálním stromatu, nikoli uvnitř nádorového parenchymu;
3. desert (desertní, imunitně pustý) – téměř úplná absence T-buněk, typická pro molekulární skupinu NSMP, predikuje horší prognózu [54].
Tyto imunofenotypy se jeví jako nezávislé prediktory také v kontextu léčby inhibitory imunitních kontrolních bodů ICI, jako jsou protilátky proti PD-1 a PD-L1. Pacientky s pokročilým endometriálním karcinomem by při určení správného fenotypu mohly profitovat z imunoterapie i v případě nevhodné molekulární skupiny, což naznačily výsledky studie NRG-GY018 s pembrolizumabem [55]. Další výzkumy v této oblasti by mohly vést k vývoji nových personalizovaných léčebných strategií u pacientek s pokročilým EC.
FRα
Folate receptor alfa (FRa) je membránově kotvený glykosylfosfatidylinositolový protein zajišťující transport folátu do buňky mechanizmem receptorově zprostředkované endocytózy. V normálních tkáních je jeho exprese omezená, avšak u některých solidních nádorů, včetně EC, dochází k její výrazné nadregulaci. U EC je nadměrná exprese zaznamenána přibližně ve 64 % případů, zejména u serózních a high grade endometrioidních histologických typů, často v souvislosti s molekulární skupinou p53abn [56]. Přítomnost FRa bývá asociována s nepříznivou prognózou, vyšší agresivitou nádoru a zvýšenou rezistencí k chemoterapii. Některé studie prokázaly souvislost mezi nadměrnou expresí FRa a kratším PFS i OS, a to nezávisle na jiných prognostických faktorech [57]. Stabilita exprese FRa v průběhu onemocnění podporuje jeho využití jako potenciálního prognostického biomarkeru, současně se jeví perspektivní jako selektivní biomarker pro cílenou terapii a v predikci odpovědi na tuto cílenou léčbu [56]. Klinické hodnocení léčiv cílených na FRa probíhá především u pacientek s pokročilým nebo recidivujícím onemocněním a s vysokou expresí tohoto receptoru. Nejvíce rozpracovanou terapeutickou strategií jsou některé ADC, zejména mirvetuximab soravtansin, který byl již schválen americkou Food and Drug Administration (FDA) pro léčbu ovariálního karcinomu [57]. Nově vyvíjený ADC proti FRa je luveltamab tazevibulin a počáteční data o jeho účinnosti prokázala u 16 pacientek s recidivujícím EC celkovou míru odpovědi (ORR – overall response rate) 37,5 % s přijatelným toxickým profilem [58]. Do vývoje dále vstupují i radioimunoterapeutické přístupy a folát-konjugovaná chemoterapie. Probíhá několik klinických studií, ve kterých jsou tyto přípravky obecně dobře tolerovány [56].
Diskuze
Nejdůležitějším prognostickým neanatomickým parametrem zůstává u EC histopatologický typ nádoru (tab. 1). Např. původní česká studie hodnotící před - a pooperační stratifikaci rizika pacientek s EC odhalila, že zatímco začlenění molekulární klasifikace změnilo rizikovou skupinu pouze ve 14 % případů, podrobné pooperační histopatologické vyšetření vedlo ke změně rizikové skupiny téměř 2krát častěji (u 26 % případů při srovnání s původní histologií založenou na biopsii) [59]. Nicméně původní binární systém histopatologického hodnocení (nízké vs. vysoké riziko) je nahrazován víceúrovňovým systémem, který umožňuje podrobnější stratifikaci rizika při hodnocení dalších biologických znaků (přítomnost LVSI, molekulární skupina, exprese L1CAM a HER2 apod.) [5,6,60]. Existuje ale mnoho dalších biomarkerů, u kterých se předpokládá velký potenciál pro využití u pacientek s EC. Rozsáhlá metaanalýza zaměřená na potenciální biomarkery u EC identifikovala 398 relevantních studií, které popsaly celkem 255 proteinů spojených s prognózou EC [26]. Tento systematický přehled zjistil, že nejvíce validovanými biomarkery pro zlepšení posouzení rizika a s tím související léčebná rozhodnutí jsou u pacientek s EC proteiny CA125, ER, PR, p53, HE4, proliferační markerový protein Ki-67, tyrosinkináza 2 receptoru Erb-B2 (ERBB2), imunoglobulin L1CAM, E-kadherin (CDH1), tumorový supresor PTEN a MMR proteiny (MSH2, MSH6, MHL1, PMS2) [26].
Výsledky studií jsou ale často protichůdné. Např. systematický přehled pěti studií prokázal, že exprese L1CAM je spojena se zhoršením OS (HR 3,62; p = 0,012) a DFS (HR 4,11; p = 0,047) u pacientek ve stadiu I (FIGO 2009) [31]. Naproti tomu význam L1CAM jako prognostického faktoru pro OS a DFS u pacientek ve stadiu I nepotvrdila jiná práce [61]. Nicméně metaanalýza zahrnující 17 starších studií s 7 146 pacientkami vypočítala, že exprese L1CAM je významně asociována s horším celkovým přežitím OS (HR 2,87; p < 0,001) a zhoršeným přežitím bez nemoci (DFS) (HR 3,32; p < 0,001) bez ohledu na stadium nemoci [32]. Jiným příkladem je prognostický význam specifické invaze nádoru do myometria MELF. Ve skupině 43 pacientek s MELF se středním a vyšším rizikem bylo podání adjuvantní chemoterapie statisticky významně spojeno s delším PFS oproti pacientkám bez chemoterapie (p = 0,047) [19]. Jiná studie zahrnující 172 pacientek s EC zjistila, že kombinace MELF vzorce s tumor buddingem představuje nezávislý prediktor nepříznivých výsledků [62]. Naopak v kohortě 979 pacientek s EC zařazených do studií PORTEC-1/-2 bylo riziko recidivy nižší u MELF pozitivních případů ve srovnání s MELF negativními (4,9 vs. 12,7 %; p = 0,026) [18].
Dalším příkladem je vypočítaný signifikantnější význam pro OS pacientek s EC pro sérový HE4 (HR 4,56; 95% CI 2,32–9,00) než pro biomarkery ER (HR 3,51; 95% CI 2,22–5,57) a TP53 (HR 2,80; 95% CI 2,00–3,92) v metaanalýze z roku 2022 [26]. Přitom s biomarkery TP53 a ER se na rozdíl od HE4 běžně pracuje při výpočtu rizika a zvažování adjuvantní terapie [5]. Na druhou stranu tato metaanalýza nenašla dostatek důkazů, které by potvrdily, že např. CA125 a PR jsou jednoznačně přínosné prognostické biomarkery EC [26]. A jiná recentní studie potvrdila nízkou expresi PR 0–10 % (vedle podstatné LVSI a p53abn) jako nezávislý negativní prognostický faktor pro kratší přežití (DSS) u pacientek s EC FIGO III–IV bez ohledu na molekulární skupinu [27].
Větší význam má při výpočtu rizika inkorporace více biomarkerů. Autoři z brněnského onkogynekologického centra do předoperační stratifikace 132 pacientek s EC zahrnuli mimo standardní kritéria (věk, stadium, histologický typ, grade, LVSI) také výsledek exprese některých biomarkerů (L1CAM, ER, PR a p53). Při inkorporaci všech těchto biomarkerů se významně zvýšila senzitivita pro stanovení skupiny s vysokým rizikem (48,4 vs. 75,8 %; p < 0,001) se statisticky nevýznamným poklesem specificity na 80 % (p = 0,238). Pozitivní prediktivní hodnota (PPV) byla pro obě metody podobná, zatímco negativní prediktivní hodnota (NPV), tj. pravděpodobnost extrémně nízkého rizika v negativních testovacích případech, se statisticky signifikantně zlepšila (66,0 vs. 78,9 %; p < 0,001) [63].
Podobně jiná studijní skupina na základě výsledků retrospektivní multicentrické analýzy 763 pacientek vyvinula model předoperační stratifikace rizika zahrnující grade nádoru, expresi ER a PR, p53, L1CAM, sérovou hladinu CA125, počet trombocytů, zhodnocení lymfadenopatie pomocí zobrazovacích metod a výsledek cervikální cytologie [64]. Tento nástroj odhadu předoperační rizika ENDORISK dokázal klasifikovat 55,8 % pacientek s < 5% rizikem postižení lymfatických uzlin, přičemž míra falešně negativních výsledků (false-negative rate) činila pouze 1,6 %. Autoři nicméně konstatují, že před potenciálním zavedením tohoto nástroje do klinické praxe je třeba výsledky ověřit prospektivní studií proveditelnosti [64].
Perspektivním směrem do budoucna je kombinovaný přístup, který integruje různé biomarkery s klinicko-patologickými charakteristikami s cílem stanovení přesnější prognózy a indikace individualizované adjuvantní terapie [26,36]. V systematickém přehledu 398 studí analyzovala jen polovina prací současně více než dva biomarkery a pouze 21 % studií hodnotilo proteiny v netkáňových vzorcích [26]. Dalším podstatným problémem je, že prognostický význam biomarkerů bývá často jen sekundárním cílem výzkumu. To vede k tvorbě vysoce heterogenních souborů pacientek a k riziku falešně pozitivních výsledků. V současnosti tedy neexistuje žádný biomarker schopný predikovat odpověď na konzervativní léčbu nad rámec standardního zobrazovacího a histopatologického vyšetření endometria [43].
Významnou přidanou hodnotu některých biomarkerů představuje možnost cílené léčby. Mezi těmito možnostmi v současnosti dominuje imunoterapie v léčbě pacientek s pokročilým nebo recidivujícím karcinomem endometria, u kterých byla prokázána mikrosatelitová nestabilita (MSI) nebo defekt mismatch repair systému (MMRd). V České republice zatím byly schváleny pro léčbu těchto pacientek dva preparáry: pembrolizumab (Keytruda) a dostarlimab (Jemperli). Další slibně se rozvíjející oblastí jsou léčiva konjugovaná s protilátkou (ADC – antibody-drug conjugates). Tyto přípravky se skládají z léčebného cytostatika, které je navázáno chemickým linkerem na vysoce selektivní monoklonální protilátku namířenou proti specifickému antigenu asociovanému se zhoubným nádorem. Cílem technologie ADC je zajistit silný efekt cytotoxické terapie při minimalizaci nežádoucích účinků na zdravé tkáně [65]. Řada ukončených i probíhajících klinických studií úspěšně zkoumala ADC cílené na HER2, FRa a TROP2, nyní se čeká na zavedení ADC do rutinní praxe [56].
Závěr
Karcinom endometria představuje skupinu vysoce heterogenních nádorů přesahující tradiční dualistický model histologického dělení. Intenzivní výzkum molekulárních, imunologických a cirkulujících biomarkerů umožnil stratifikaci karcinomu endometria do skupin s odlišnou prognózou a specifickými možnostmi terapie. Různé neanatomické charakteristiky nabízejí nové možnosti cílené léčby a predikce výsledků. Další prospektivní studie by měly být zaměřeny na lepší pochopení biologie EC včetně vzácných podtypů, jako je mesonefric-like karcinom nebo mucinózní karcinom s intestinální diferenciací a převážně biomarkerů souvisejících se specifickou cílenou terapií.
Zdroje
1. Sung H, Ferlay J, Siegel RL et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021; 71 (3): 209–249. doi: 10.3322/caac.21660.
2. Bray F, Laversanne M, Sung H et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2024; 74 (3): 229–263. doi: 10.3322/caac.21834.
3. Svod.cz. Český národní webový portál epidemiologie nádorů. Systém pro vizualizaci onkologických dat. Institut biostatistiky a analýz Lékařské a Přírodovědecké fakulty Masarykovy univerzity (IBA MU). 2026 [online]. Dostupné z: http: //www.svod.cz.
4. Concin N, Matias-Guiu X, Vergote I et al. ESGO/ESTRO/ESP guidelines for the management of patients with endometrial carcinoma. Radiother Oncol 2021; 154 : 327–353. doi: 10.1016/j.radonc.2020.11.018.
5. Concin N, Matias-Guiu X, Cibula D et al. ESGO--ESTRO-ESP guidelines for the management of patients with endometrial carcinoma: update 2025. Lancet Oncol 2025; 26 (8): e423–e435. doi: 10.1016/S1470-2045 (25) 00167-6.
6. Berek JS, Matias-Guiu X, Creutzberg C et al. FIGO staging of endometrial cancer: 2023. Int J Gynaecol Obstet 2023; 162 (2): 383–394. doi: 10.1002/ijgo.14923.
7. Hruda M, Sehnal B, Halaška MJ et al. Nový staging karcinomu endometria – FIGO 2023. Ceska Gynekol 2024; 89 (2): 120–127. doi: 10.48095/cccg2024120.
8. Włodarczyk K, Kuryło W, Pawłowska-Łachut A et al. circRNAs in endometrial cancer – a promising biomarker: state of the art. Int J Mol Sci 2024; 25 (12): 6387. doi: 10.3390/ijms25126387.
9. Bokhman JV. Two pathogenetic types of endometrial carcinoma. Gynecol Oncol 1983; 15 (1): 10–17. doi: 10.1016/0090-8258 (83) 90111-7.
10. How JA, Jazaeri AA, Westin SN et al. Translating biological insights into improved management of endometrial cancer. Nat Rev Clin Oncol 2024; 21 (11): 781–800. doi: 10.1038/s41 571-024-00934-7.
11. Makker V, MacKay H, Ray-Coquard I et al. Endometrial cancer. Nat Rev Dis Primer 2021; 7 (1): 88. doi: 10.1038/s41572-021-00324-8.
12. Ørtoft G, Lausten-Thomsen L, Høgdall C et al. Lymph-vascular space invasion (LVSI) as a strong and independent predictor for non-locoregional recurrences in endometrial cancer: a Danish Gynecological Cancer Group Study. J Gynecol Oncol 2019; 30 (5): e84. doi: 10.3802/jgo.2019.30.e84.
13. Tortorella L, Restaino S, Zannoni GF et al. Substantial lymph-vascular space invasion (LVSI) as predictor of distant relapse and poor prognosis in low-risk early-stage endometrial cancer. J Gynecol Oncol 2021; 32 (2): e11. doi: 10.3802/jgo.2021.32.e11.
14. Sehnal B, Hruda M, Matej R et al. New FIGO 2023 staging system of endometrial cancer: an updated review on a current hot topic. Geburtshilfe Frauenheilkd 2025; 85 (4): 405–416. doi: 10.1055/a-2494-8395.
15. Dagher C, Bjerre Trent P, Alwaqfi R et al. Oncologic outcomes based on lymphovascular space invasion in node-negative FIGO 2009 stage I endometrioid endometrial adenocarcinoma: a multicenter retrospective cohort study. Int J Gynecol Cancer 2024; 34 (10): 1485–1492. doi: 10.1136/ijgc-2024-005746.
16. Peters EE, León-Castillo A, Smit VT et al. Defining substantial lymphovascular space invasion in endometrial cancer. Int J Gynecol Pathol 2022; 41 (3): 220–226. doi: 10.1097/PGP.000000 0000000806.
17. Espinosa I, Serrat N, Zannoni GF et al. Endometrioid endometrial carcinomas with microcystic, elongated, and fragmented (MELF) type of myoinvasion: role of immunohistochemistry in the detection of occult lymph node metastases and their clinical significance. Hum Pathol 2017; 70 : 6–13. doi: 10.1016/ j.humpath.2017.05.026.
18. van den Heerik AS, Aiyer KT, Stelloo E et al. Microcystic elongated and fragmented (MELF) pattern of invasion: molecular features and prognostic significance in the PORTEC-1 and -2 trials. Gynecol Oncol 2022; 166 (3): 530–537. doi: 10.1016/j.ygyno.2022.06.027.
19. Jia P, Zhang Y. Molecular classification and adjuvant treatment in endometrioid endometrial cancer with microcystic elongated and fragmented (MELF) invasion pattern. BMC Womens Health 2024; 24 (1): 607. doi: 10.1186/s129 05-024-03449-6.
20. Okcu O, Askan G, Sen B et al. Prognositc significance of Microcystic Elongated and Fragmanted (MELF) myometrial invasion pattern: a retrospective study. Medeni Med J 2022; 37 (3): 212–219. doi: 10.4274/MMJ.galenos.2022.40336.
21. Presl J, Vaněček T, Michal M et al. Molekulární klasifikace endometriálních karcinomů převedená do praxe. Ceska Gynekol 2021; 86 (4): 258–262. doi: 10.48095/cccg2021258.
22. Dundr P, Cibula D, Doležel M et al. Molekulární testování u karcinomu endometria – společné doporučení ČOS, onkogynekologické sekce ČGPS, SROBF a SČP ČLS JEP. Ceska Gynekol 2021; 86 (4): 264–272. doi: 10.48095/cccg2021264.
23. León-Castillo A, de Boer SM, Powell ME et al. Molecular classification of the PORTEC-3 trial for high-risk endometrial cancer: impact on prognosis and benefit from adjuvant therapy. J Clin Oncol 2020; 38 (29): 3388–3397. doi: 10.1200/JCO.20.00549.
24. Michalová K, Presl J, Straková-Peteříková A et al. Výhody sekvenování nové generace (NGS) v molekulární klasifikaci endometriálních karcinomů – naše zkušenosti s 270 případy. Ceska Gynekol 2024; 89 (5): 349–359. doi: 10.48095/cccg2024349.
25. Ballová Z, Gašparová P, Sitáš M et al. Pohľad na klasifikáciu a manažment endometriálneho karcinómu v kontexte molekulárnych subtypov. Ceska Gynekol 2024; 89 (2): 128–132. doi: 10.48095/cccg2024128.
26. Coll-de la Rubia E, Martinez-Garcia E, Dittmar G et al. Prognostic biomarkers in endometrial cancer: a systematic review and meta-analysis. J Clin Med 2020; 9 (6): 1900. doi: 10.3390/jcm9061900.
27. Vrede SW, Van Weelden WJ, Bulten J et al. Hormonal biomarkers remain prognostically relevant within the molecular subgroups in endometrial cancer. Gynecol Oncol 2024; 192 : 15–23. doi: 10.1016/j.ygyno.2024.10.028.
28. Przewoźny S, Rogaliński J, de Mezer M et al. Estrogen Receptor (ER) and Progesterone Receptor (PgR) expression in endometrial cancer – an immunohistochemical assessment. Diagnostics (Basel) 2024; 14 (3): 322. doi: 10.3390/diagnostics14030322.
29. Jamieson A, Huvila J, Chiu D et al. Grade and estrogen receptor expression identify a subset of no specific molecular profile endometrial carcinomas at a very low risk of disease-specific death. Mod Pathol 2023; 36 (4): 100085. doi: 10.1016/j.modpat.2022.100085.
30. Vermij L, Jobsen JJ, León-Castillo A et al. Prognostic refinement of NSMP high-risk endometrial cancers using oestrogen receptor immunohistochemistry. Br J Cancer 2023; 128 (7): 1360–1368. doi: 10.1038/s41416-023-02141-0.
31. Giannini A, D’Oria O, Corrado G et al. The role of L1CAM as predictor of poor prognosis in stage I endometrial cancer: a systematic review and meta-analysis. Arch Gynecol Obstet 2024; 309 (3): 789–799. doi: 10.1007/s00404-023-07149-8.
32. Guo M, Gong H, Nie D, et al. High L1CAM expression predicts poor prognosis of patients with endometrial cancer: a systematic review and meta-analysis. Medicine (Baltimore) 2021; 100 (13): e25330. doi: 10.1097/MD.0000000000025330.
33. Zeimet AG, Reimer D, Huszar M et al. L1CAM in early-stage type I endometrial cancer: results of a large multicenter evaluation. J Natl Cancer Inst 2013; 105 (15): 1142–1150. doi: 10.1093/jnci/djt144.
34. Abada E, Kim S, Jang H et al. Human epidermal growth factor receptor-2 (HER2) expression in FIGO3 high-grade endometrial endometrioid carcinoma: clinicopathologic characteristics and future directions. Gynecol Oncol 2024; 185 : 25–32. doi: 10.1016/j.ygyno.2024.01.048.
35. Shawn LyBarger K, Miller HA, Frieboes HB. CA125 as a predictor of endometrial cancer lymphovascular space invasion and lymph node metastasis for risk stratification in the preoperative setting. Sci Rep 2022; 12 (1): 19783. doi: 10.1038/s41598-022-22026-1.
36. Yu Z, Sun Y, Guo C. Evaluating pretreatment serum CA-125 levels as prognostic biomarkers in endometrial cancer: a comprehensive meta-analysis. Front Oncol 2024; 14 : 1442814. doi: 10.3389/fonc.2024.1442814.
37. Presl J, Novotny Z, Topolcan O et al. CA125 and HE4 levels in a Czech female population diagnosed with endometrial cancer in preoperative management. Anticancer Res 2014; 34 (1): 327–331.
38. Jiang T, Huang L, Zhang S. Preoperative serum CA125: a useful marker for surgical management of endometrial cancer. BMC Cancer 2015; 15 : 396. doi: 10.1186/s12885-015-1260-7.
39. Li J, Wang X, Qu W et al. Comparison of serum human epididymis protein 4 and CA125 on endometrial cancer detection: a meta-analysis. Clin Chim Acta Int J Clin Chem 2019; 488 : 215–220. doi: 10.1016/j.cca.2018.11.011.
40. Brennan DJ, Hackethal A, Metcalf AM et al. Serum HE4 as a prognostic marker in endometrial cancer – a population based study. Gynecol Oncol 2014; 132 (1): 159–165. doi: 10.1016/j.ygyno.2013.10.036.
41. Wang Y, Han C, Teng F et al. Predictive value of serum HE4 and CA125 concentrations for lymphatic metastasis of endometrial cancer. Int J Gynaecol Obstet 2017; 136 (1): 58–63. doi: 10.1002/ijgo.12010.
42. Ørbo A, Arnes M, Lyså LM et al. HE4 is a novel tissue marker for therapy response and progestin resistance in medium - and low-risk endometrial hyperplasia. Br J Cancer 2016; 115 (6): 725–730. doi: 10.1038/bjc.2016.247.
43. Barr CE, Sergeant JC, Agnew HJ et al. Serum HE4 predicts progestin treatment response in endometrial cancer and atypical hyperplasia: a prognostic study. BJOG 2023; 130 (8): 941–948. doi: 10.1111/1471-0528.17417.
44. Liu X, Li J, Deng J et al. Targeting Trop2 in solid tumors: a look into structures and novel epitopes. Front Immunol 2023; 14 : 1332489. doi: 10.3389/fimmu.2023.1332489.
45. Moufarrij S, Dopeso H, Brown DN et al. TROP2 expression and therapeutic targeting in uterine carcinosarcoma. Gynecol Oncol 2025; 197 : 129–138. doi: 10.1016/j.ygyno.2025.04.590.
46. Wen Y, Ouyang D, Zou Q et al. A literature review of the promising future of TROP2: a potential drug therapy target. Ann Transl Med 2022; 10 (24): 1403. doi: 10.21037/atm-22-5976.
47. Bellone S, McNamara B, Mutlu L et al. Monitoring treatment response, early recurrence, and survival in uterine serous carcinoma and carcinosarcoma patients using personalized circulating tumor DNA biomarkers. Int J Mol Sci 2023; 24 (10): 8873. doi: 10.3390/ijms24108873.
48. Moss EL, Gorsia DN, Collins A et al. Utility of circulating tumor DNA for detection and monitoring of endometrial cancer recurrence and progression. Cancers (Basel) 2020; 12 (8): 2231. doi: 10.3390/cancers12082231.
49. Liu Y, Lu XN, Guo HM et al. Development and validation of a circulating tumor DNA-based optimization-prediction model for short-term postoperative recurrence of endometrial cancer. World J Clin Cases 2024; 12 (18): 3385–3394. doi: 10.12998/wjcc.v12.i18.3385.
50. Pereira E, Camacho-Vanegas O, Anand S et al. Personalized circulating tumor DNA biomarkers dynamically predict rreatment response and survival in gynecologic cancers. PLoS One 2015; 10 (12): e0145754. doi: 10.1371/journal.pone.0145754.
51. Takenaka K, Olzomer EM, Hoehn KL et al. Investigation of circular RNA transcriptome in obesity-related endometrial cancer. Gene 2023; 855 : 147125. doi: 10.1016/j.gene.2022.147125.
52. Ye F, Tang QL, Ma F et al. Analysis of the circular RNA transcriptome in the grade 3 endometrial cancer. Cancer Manag Res 2019; 11 : 6215–6227. doi: 10.2147/CMAR.S197343.
53. Guo F, Dong Y, Tan Q et al. Tissue infiltrating immune cells as prognostic biomarkers in endometrial cancer: a meta-analysis. Dis Markers 2020; 2020 : 1805764. doi: 10.1155/2020/1805764.
54. Hattori S, Yoshikawa N, Liu W et al. Understanding the impact of spatial immunophenotypes on the survival of endometrial cancer patients through the ProMisE classification. Cancer Immunol Immunother 2025; 74 (2): 70. doi: 10.1007/s00262-024-03919-8.
55. Eskander RN, Sill MW, Beffa L et al. Pembrolizumab plus chemotherapy in advanced or recurrent endometrial cancer: overall survival and exploratory analyses of the NRG GY018 phase 3 randomized trial. Nat Med 2025; 31 (5): 1539–1546. doi: 10.1038/s41591-025-03566-1.
56. Matoba Y, Devins KM, Milane L et al. High--grade endometrial cancer: molecular subtypes, current challenges, and treatment options. Reprod Sci 2024; 31 (9): 2541–2559. doi: 10.1007/s43032-024-01.
57. Matulonis UA, Lorusso D, Oaknin A et al. Efficacy and safety of mirvetuximab soravtansine in patients with platinum-resistant ovarian cancer with high folate receptor alpha expression: results from the SORAYA study. J Clin Oncol 2023; 41 (13): 2436–2445. doi: 10.1200/JCO.22.01900.
58. Soberanis Pina P, Lheureux S. Novel molecular targets in endometrial cancer: mechanisms and perspectives for therapy. Biologics 2024; 18 : 79–93. doi: 10.2147/BTT.S369783.
59. Bretová P, Ndukwe MI, Laco J et al. Preoperative risk stratification in endometrial cancer using ESGO/ESTRO/ESP 2021 guidelines: accuracy with and without molecular classification. BMC Cancer 2025; 25 (1): 1302. doi: 10.1186/s12885-025-14741-5.
60. Soslow RA, Tornos C, Park KJ et al. Endometrial carcinoma diagnosis: use of FIGO grading and genomic subcategories in clinical practice: recommendations of the International Society of Gynecological Pathologists. Int J Gynecol Pathol 2019; 38 (Suppl 1): S64–S74. doi: 10.1097/PGP.0000000000000518.
61. Klat J, Mladenka A, Dvorackova J et al. L1CAM as a negative prognostic factor in endometrioid endometrial adenocarcinoma FIGO stage IA–IB. Anticancer Res 2019; 39 (1): 421–424. doi: 10.21873/anticanres.13128.
62. Qi X, Zhu L, Zhang B. Clinicopathologic association and prognostic impact of microcystic, elongated and fragmented pattern invasion, combined with tumor budding in endometrioid endometrial cancer. J Obstet Gynaecol Res 2022; 48 (9): 2431–2441. doi: 10.1111/jog. 15335.
63. Weinberger V, Bednarikova M, Hausnerova J et al. A novel approach to preoperative risk stratification in endometrial cancer: the added value of immunohistochemical markers. Front Oncol 2019; 9 : 265. doi: 10.3389/fonc.2019. 00265.
64. Reijnen C, Gogou E, Visser NC et al. Preoperative risk stratification in endometrial cancer (ENDORISK) by a Bayesian network model: a development and validation study. PLoS Med 2020; 17 (5): e1003111. doi: 10.1371/journal.pmed.1003111.
65. Kuhn E, Gambini D, Runza L et al. Unsolved issues in the integrated histo-molecular classification of endometrial carcinoma and therapeutic implications. Cancers (Basel) 2024; 16 (13): 2458. doi: 10.3390/cancers16132458.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicínaČlánek vyšel v časopise
Česká gynekologie

2026 Číslo 2
-
Všechny články tohoto čísla
- vNOTES hysterektomie snižuje míru laparotomie u obezity III. stupně – retrospektivní srovnávací studie
- Perinatální výsledky u těžké preeklampsie s peritoneálním ascitem – zkušenosti z jednoho terciárního centra
- Epidemiologie obezity v těhotenství v České republice – demografické souvislosti a klinické dopady
- Endometriom Bartholinovy žlázy
- Vulvodynie a perzistentní vulvární bolest – diagnostika, terapie a role laserové vaporizace
- Klinicky významné histopatologické charakteristiky a biomarkery karcinomu endometria
- Limity skríningu a prevencie preeklampsie v populácii žien po metódach asistovanej reprodukcie
- Vliv vybraných rozměrů struktur pánevního dna na průběh porodu – přehled literatury
- Doporučení ESGO/ISUOG pro jehlové biopsie v onkogynekologii – upravená verze
- Zemřel doc. MUDr. Jaroslav Feyereisl, CSc. – bývalý ředitel Ústavu pro péči o matku a dítě
- Vliv angiogenních faktorů a mateřské endoteliální dysfunkce na výsledek těhotenství
- Kryokonzervace oocytů pro zachování ženské plodnosti
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Vliv angiogenních faktorů a mateřské endoteliální dysfunkce na výsledek těhotenství
- Vliv vybraných rozměrů struktur pánevního dna na průběh porodu – přehled literatury
- Kryokonzervace oocytů pro zachování ženské plodnosti
- Perinatální výsledky u těžké preeklampsie s peritoneálním ascitem – zkušenosti z jednoho terciárního centra