Gravidita v jizvě po císařském řezu
Cesarean scar pregnancy
Objective: To summarize the current knowledge on pregnancy in a cesarean scar. Methodology: A literature review on the topic using the PubMed database. Results: Gravidity in a cesarean scar is a relatively new type of ectopic pregnancy that will be an increasingly common problem in an era of increasing cesarean section rates. It is still a relatively rare event, occurring in about 6% of the population. Diagnosis is based primarily on ultrasound examination and is essential early on in pregnancy. The pathogenesis of the disease is due to a disorder of the basal layer of the endometrium and can lead to conditions that we refer to as placenta accreta spectrum. The management is completely individualized and depends on hCG values, ultrasound findings, fetal viability, the wishes of the pregnant woman and the experience of the gynecologist concerned. Conclusion: This is still a rare occurrence of ectopic pregnancy but with increasing potential. The solution is completely individualized based on a precise and early ultrasound diagnosis.
Keywords:
Methotrexate – cesarean scar pregnancy – ultrasound diagnosis – placenta accreta spectrum – vacumaspiration – uterine scar resuture
Autoři:
J. Hanáček 1,2
; Hynek Heřman 1,2
; P. Křepelka 1,2
; Lubomír Hašlík 1,2
; Brandejsová A. 1; Ladislav Krofta 1,2
Působiště autorů:
Ústav pro péči o matku a dítě, 3. LF UK, Praha
1; 3. LF UK a FNKV, Praha
2
Vyšlo v časopise:
Ceska Gynekol 2022; 87(3): 193-197
Kategorie:
Přehledový článek
doi:
https://doi.org/10.48095/cccg2022193
Souhrn
Cíl: Shrnout současné poznatky o graviditě v jizvě po císařském řezu. Metodika: Literární přehled k danému tématu s použitím databáze PubMed. Výsledky: Gravidita v jizvě po císařském řezu je relativně novým typem mimoděložní gravidity, která v době narůstajícího počtu císařských řezů bude stále častějším problémem. Stále se jedná o relativně raritní záležitost, která se vyskytuje asi v 6 % případů. Diagnostika je založena především na ultrazvukovém vyšetření a je podstatná v časné fázi těhotenství. Patogeneze onemocnění je dána poruchou základní vrstvy endometria a může vést ke stavům, které označujeme jako placenta accreta spektrum. Řešení je zcela individualizované a závislé na hodnotách hCG, ultrazvukovém nálezu, vitalitě plodu, přání těhotné a zkušenostech daného gynekologa. Závěr: Jedná se zatím o raritní výskyt mimoděložní gravidity, ale s narůstajícím potenciálem. Řešení je zcela individuální založené na kvalitní a především včasné ultrazvukové diagnostice.
Klíčová slova:
metotrexát – gravidita v jizvě po císařském řezu – ultrazvuková diagnostika – placenta accreta spektrum – vakuumaspirace – resutura jizvy děložní
Relativně novým typem mimoděložního těhotenství je gravidita v jizvě po císařském řezu (CSP – caesarean scar pregnancy). Jedná se o implantaci plodového vejce do oblasti jizvy po předchozím císařském řezu. Již dříve byla popsána obdobná ektopická gravidita, a to gravidita v jizvě po myomektomii. S tím, jak narůstá počet císařských řezů, narůstá i počet gravidit v jizvě po císařském řezu. V ČR bylo v roce 2000 provedeno 27 646 císařských řezů a v roce 2021 jich bylo 28 281. Předpokládá se, že CSP reprezentuje asi 6 % z celkového počtu ektopických gravidit u všech žen, které mají alespoň jeden císařský řez v anamnéze [1]. Odhaduje se incidence CSP okolo 1/ 1 688 všech těhotenství a přibližně 1/ 2 000 všech císařských řezů [2].
Patogeneze
V průběhu normálního těhotenství penetruje trofoblast do myometria a remodeluje cévy na nízkorezistentní a vysokoprůtokové. Tato fyziologická invaze je zastavena v Nitabuchově fibrinoidní vrstvě, což je vrstva, která se přirozeně vyskytuje na hranici mezi endometriem a cytotrofoblastem. Předchozí operace, která vede ke vzniku jizvy, a tím ke ztenčení nebo dokonce vymizení této vrstvy, je rizikovým faktorem, který vede k neoponované penetraci trofoblastu a ke vzniku placenta accreta. Tantbironj et al popisují vznik poruch placentace jako problém chybění decidui a ne jako samo o sobě invazivní prorůstání trofoblastu [3]. Obdobné poruchy můžeme vidět i po myomektomiích, kyretážích, resekcích septa, kde také dochází k vymizení bazální decidui, ale výskyt gravidit v těchto defektech je méně častý než v jizvě po císařském řezu. Timor-Tritsch et al předpokládají, že gravidita v jizvě a placenta accreta jsou stejná histologická onemocnění a že akretní placenta je progresí gravidity v jizvě. Ve své studii komparovali histologický materiál z oblasti jizvy a z endometria ze zadní stěny děložní. V oblasti jizvy nalezli méně leukocytů a nižší vaskularizaci a deklarovali, že se endometrium v jizvě výrazně liší od zbytku endometria dutiny děložní [4].
Jistě existuje vztah mezi kvalitou hojení jizvy po císařském řezu a jejími konsekvencemi. Roeder et al hodnotili histopatologické nálezy hojení jizvy a nalezli rozdílné tloušťky myometria v okolí jizvy s rozdílným poměrem svalových vláken a elastinu. Pravděpodobně porucha v hojení vede ke vzniku defektu stěny děložní [5]. Rizikové faktory, které vedou ke vzniku defektu přední stěny děložní v místě hysterotomie, jsou základní čtyři:
1. technika uzávěru hysterotomie;
2. lokalizace jizvy;
3. predispozice k hojení rány;
4. ostatní faktory.
Jsou zde tedy zahrnuty inadekvátní sutura hysterotomie, pooperační infekční komplikace, hematom, diabetes a choroby spojené s poruchami vaziva [6,7]. Také zhoršené prokrvení v místě hojící se hysterotomie nebo krátký interval mezi císařským řezem a následnou graviditou vedou k defektům stěny děložní a jsou častěji popsány i poruchy placentace.
Typy CSP
Rozlišujeme dva základní typy CSP, a to:
Typ 1 – endogenní, s progresí do cervikoistmického prostoru, jedná se vlastně o implantaci v místě hysterotomie. Myometrium nad gestačním váčkem by mělo být vyšší než 5 mm.
Typ 2 – exogenní, kde dochází k prorůstání do defektní jizvy směrem k měchýři a dutině břišní. Myometrium nad gestačním váčkem se popisuje menší než 2 mm.
Endogenní typ většinou rezultuje ve vitální graviditu s větší rizikem krvácení z placentární strany. Exogenní typ může být komplikován rupturou děložní a krvácením v časné fázi těhotenství [8–10].
Klinická prezentace
Většina symptomů CSP je nespecifických. V review na 751 případech byla více než třetina zcela asymptomatických, ve 39 % se objevilo nebolestivé krvácení, v 16 % bylo krvácení spojené s bolestí a v 9 % byla jediným symptomem bolest [11]. Gestační stáří bylo v rozmezí 5.–16. týdne gravidity s průměrem 7 ± 2,5 týdne.
Diagnostika
Ultrazvuk
Diagnóza gravidity v jizvě je postavena především na vaginálním ultrazvukovém vyšetření. Pacientka s pozitivním těhotenským testem a císařským řezem v anamnéze by měla být co nejdříve vyšetřena ultrazvukem se zaměřením na lokalizaci gravidity a její vztah k hysterotomii. Základními ultrazvukovými diagnostickými kritérii jsou [4,12–14]:
1. Prázdná dutina děložní, uzavřený a prázdný cervikální kanál.
2. Detekce gestačního váčku v oblasti istmu děložního v oblasti hysterotomie. Gestační váček může být s plodem s akcí srdeční, nebo bez ní. Před 7. gestačním týdnem se gestační váček tvaruje do podoby jizvy – tedy často trojúhelníkovitého vzhledu. Po 7. týdnu gestace dochází často k jeho vytažení se do dutiny děložní a v místě jizvy je patrná placentární tkáň.
3. Může být absentní nebo přítomná ztenčelá vrstva myometria mezi gestačním váčkem a stěnou močového měchýře.
4. Při použití dopplerovského mapování se zobrazuje okolo gestačního váčku zvýšený tok nízkoodporových cév. To nám slouží k diferenciální diagnostice u probíhajícího abortu, kde tyto zvýšené toky nejsou patrné (obr. 1, 2).
Fig. 1. Ultrasound finding of gestational week 7+1 pregnancy in a uterine scar.
Atypically low localized pregnancy. The empty upper half of the uterine cavity.
Thinned myometrium at the site of fetal egg nidation.

Fig. 2. Ultrasound finding of gestational week 6+2 pregnancy in a uterine scar.
Atypically low localized pregnancy. The empty upper half of the uterine cavity.
Thinned myometrium at the site of fetal egg nidation. Standard wall thickness is
1.7 cm, and thinned myometrium scar is 1.7 mm. Noticeable chorion frondosum
forming at the site of the scar.
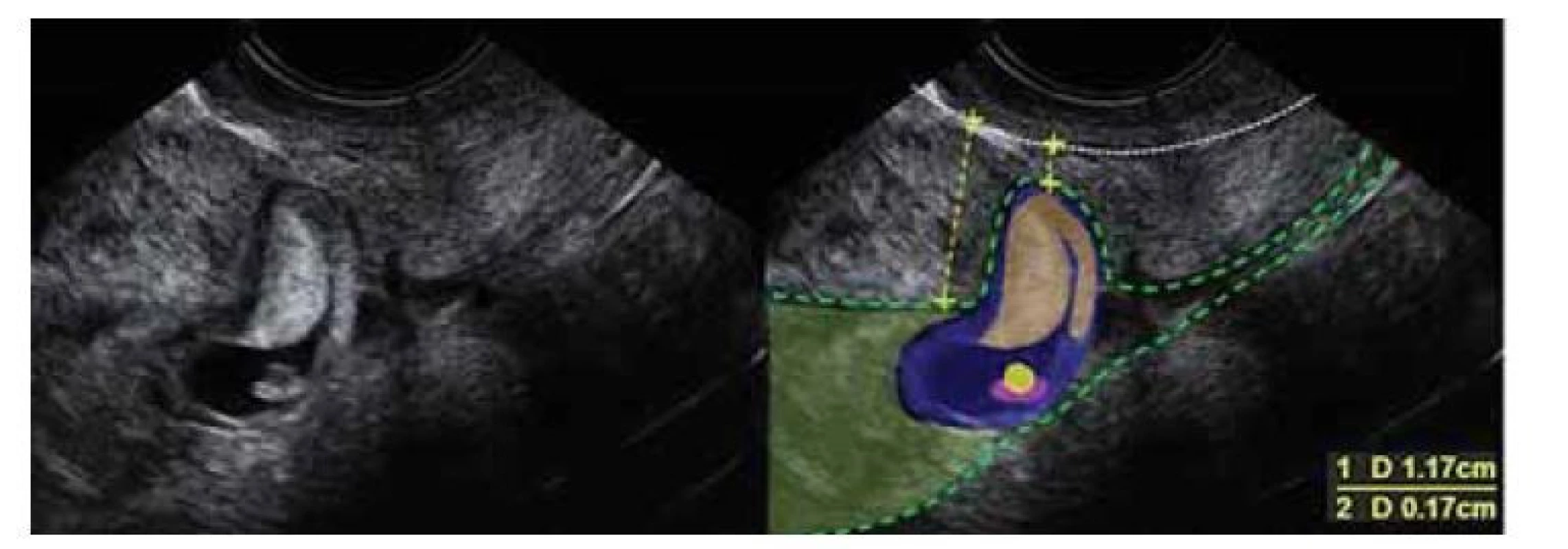
Magnetická rezonance
Magnetická rezonance může být doplňkovou metodou, pokud není ultrazvukové vyšetření validní. Lépe nám zobrazuje implantaci do jizvy. T2 vážené obrazy lépe zobrazují defektní jizvu, vrstvy trofoblastu a myometria [15].
Diferenciální diagnostika
V diferenciální diagnostice musíme myslet na intrauterinní graviditu, běžící abort, cervikální graviditu, placenta accreta spektrum a graviditu v jizvě po myomektomii.
Pomocným ultrazvukovým kritériem k diagnostice CSP a jejímu odlišení od intrauterinní gravidity je dle Timora-Tritsche metoda, kdy proložíme napříč polovinou dělohy přímku, potom pokud je centrum gestačního váčku pod touto přímkou, jedná se o graviditu v jizvě děložní, pokud bude plod nad přímkou, jedná se o intrauterinní graviditu. Toto kritérium je platné do 7.–8. týdne gravidity. K odlišení cervikální gravidity navrhuje obdobně proložit hrdlem v sagitální rovině úsečku a plod, který se vyskytuje výrazně v anteriorní straně, bude pravděpodobně CSP [12].
Pokud se jedná o běžící abort lokalizovaný v hrdle děložním nebo istmické části dělohy, nebude se u něj vyskytovat při dopplerovském zobrazení cirkulární zvýšená vaskularizace. Také při tlaku vaginální sondou dojde snadno ke slidingu neboli vysunutí plodu a jeho pohybu do dutiny děložní.
Přirozený vývoj CSP
Většina neřešených CSP gravidit končí těžkými komplikacemi (ruptura děložní, život ohrožující krvácení, hysterektomie v průběhu císařského řezu), ovšem jsou i gravidity, které končí úspěšně donošeným porodem císařským řezem, ovšem vždy s hysterektomií pro akrétní placentu [7]. Na otázku přirozeného vývoje CSP se snažila najít odpověď systematická review a metaanalýza Caliho et al [16]. Analyzovali 17 studií, kde bylo zahrnuto 273 žen a z nich 69 žen bylo řešeno pouze expektací ať už pro pozdní diagnostiku, neprovedenou diagnostiku, nebo na přání ženy. Rozdělili případy na CSP, kde byly embrya bez akce srdeční 24,6 % (17/ 69) a se srdeční akcí 75,4 % (52/ 69).
Embrya se srdeční akcí
Z 52 žen, u nichž byl CSP s akcí srdeční, došlo ve 13 % k vymizení akce srdeční a k nekomplikovanému abortu bez nutnosti intervence. Ve 20 % byla vyžadována akutní chirurgická intervence pro silné krvácení. Ruptura děložní se vyskytla v průběhu I. nebo II. trimestru v 9,9 %, a to průměrně v 18,1 týdnu gestace. Bylo nutné provést v 15,2 % hysterektomii ze všech případů. Zajímavé bylo, že 76,8 % gravidit pokračovalo do III. trimestru a téměř ve 30 % se u těchto žen objevilo silné krvácení. Z donošených gravidit byla v 75 % diagnostikována porucha placentace a z nich v 50 % se vyskytovala placenta percreta. Všechny byly diagnostikovány před porodem a proběhla hysterektomie v průběhu císařského řezu. Nedošlo k žádnému úmrtí ženy. Krevní ztráty se pohybovaly mezi 600 a 6 000 ml.
Embrya bez akce srdeční
U žen s CSP, kde nebyla akce srdeční, došlo v 70,6 % ke spontánnímu nekomplikovanému potratu a pouze u 29,4 % bylo nutné provést chirurgickou nebo medikamentózní terapii. Ke spontánní ruptuře děložní došlo v 5,98 % a nebylo třeba provést žádnou hysterektomii.
Zajímavá je i otázka rekurencí, heterotopických a vícečetných gravidit při CSP. Ben Nangi et al uvádějí 5% míru rekurence u 21 žen řešených konzervativně pro CSP [17]. Bennett et al uvádějí pacientku, která měla 5krát rekurentní graviditu do jizvy po císařském řezu [18]. Wang et al uvádějí dokonce 15,6% míru rekurence u 32 pacientek řešených konzervativně pro CSP [19].
Dokonce byly v literatuře uváděny i heterotopické gravidity s oběma vitálními plody řešené intragestačně aplikovaným chloridem draselným (KCl) do CSP plodu a následně úspěšně donošeným intrauterinním plodem [20].
Terapie
Terapie je závislá na včasné diagnostice, klinických symptomech, věku a přání gravidity pacientky, vitalitě plodu. Zatím nebyl stanoven jasný konsenzus terapie CSP. Je možné zvolit konzervativní postup, medikamentózní léčbu, lokální léčbu a chirurgický přístup. Je možné postupy i kombinovat. Snahou je zachovat fertilitu a preventivně se vyhnout život ohrožujícím komplikacím, jakými jsou masivní hemoragie a ruptura děložní [21].
Expektační postup
Z výše uvedeného vývoje CSP je patrné, že expektační postup je možný převážně u plodů bez akce srdeční. V ostatních případech je zde zvýšené riziko rozvoje poruch placentace, riziko ruptury děložní, masivního krvácení a následné hysterektomie.
Podání metotrexátu
Většina autorů udává v systémovém podání methotrexátu single dose s podáním 2. dávky o týden později, pokud je třeba. Zkušenosti jsou obdobné jako při léčbě molární gravidity. V systematické review bylo systémové podání metotrexátu efektivní při hodnotách hCG < 12 000 mIU/ ml, plod bez akce srdeční a při graviditě před 8. týdnem gestace [22]. Ve 25 % byla ovšem nutná ještě jiná terapie a ve 13 % se objevily závažné komplikace. Je možné, že fi brózní tkáň, která obklopuje trofoblast, znemožňuje průnik metotrexátu. Pro tyto komplikace a systémový vliv léčby je jednoznačně preferováno lokální podání metotrexátu.
Cok et al uvádějí ve své studii použití lokálního metotrexátu v dávce 50 mg/ m2 u 18 žen, kde došlo k úspěšnému ukončení gravidity v 61,1 %, ve 22,2 % bylo třeba aplikovat dodatečnou dávku a v 16,7 % bylo třeba provést chirurgický zákrok [23]. Předpokládá se dobrý efekt, pokud jsou hodnoty hCG < 20 000 mIU/ ml. K lokální léčbě je možné použít i jiné látky jako třeba KCl, hyperosmolární glukózu nebo etanol [24].
Embolizace uterinních arterií
Jedná se spíše o adjuvantní léčebnou modalitu, která se používá při aplikaci metotrexátu nebo před vakuumaspirací ke snížení krevní ztráty, obzvláště tam, kde je vyšší podezření na vrůstání trofoblastu do myometria [25]. Ze systematické review na 239 případech bylo použití uterinní embolizace a následně provedené revize dutiny děložní úspěšné v 99,16 % případů a komplikace se vyskytly pouze v 10,4 % [26]. Obdobně jako při použití embolizace uterinních arterií při léčbě myomatózy jsou i zde uvedeny komplikace jako snížená ovariální rezerva, intrauterinní růstová restrikce, předčasný porod, abrupce placenty a poruchy placentace.
Hysteroskopie
Jedná se o miniinvazivní výkon, kdy pod kontrolou zraku jsme schopni kličkou resektoskopu odstranit plodové vejce. Je možné použít s výhodou metodu hysteroskopického shaveru, který nám umožňuje lepší vizualizaci a nasátí plodových částí. Hysteroskopické řešení je nejjednodušší k provedení u typu 1 CSP. Ze systematické review u 95 žen došlo při použití této metody k závažné komplikace pouze u 3,2 % žen a v 17 % bylo třeba připojit ještě jinou další intervenci [27].
Vakuumaspirace
Pod ultrazvukovou kontrolou provedená vakuumaspirace je jednou ze základních metod k řešení CSP. Bývá často používána v kombinaci s ostatními metodami. Na našem pracovišti je asi nejpoužívanější především u plodu do 8. gestačního týdne. Riziko krvácivých komplikací narůstá po 10. týdnu gestace.
Laparoskopická nebo laparotomická resekce jizvy
Radikální řešení je doporučováno především u pacientek s projevy krvácení do dutiny břišní nebo u hemodynamicky nestabilních pacientek k zástavě krvácení nebo u větších týdnů gestace. Jedná se již o komplikovanější metodu, kdy musíme sesunout pliku močového měchýře, provést klínovitou resekci dolního děložního segmentu a následně jeho resuturu v jedné nebo ve dvou vrstvách. Ke snížení krevní ztráty je možné připojit ligaturu nebo alespoň dočasné zaklipování uterinních arterií (obr. 3, 4).
Fig. 3. Laparoscopic view of pregnancy
through a scar after caesarean section.
Gestational age – 11th week.
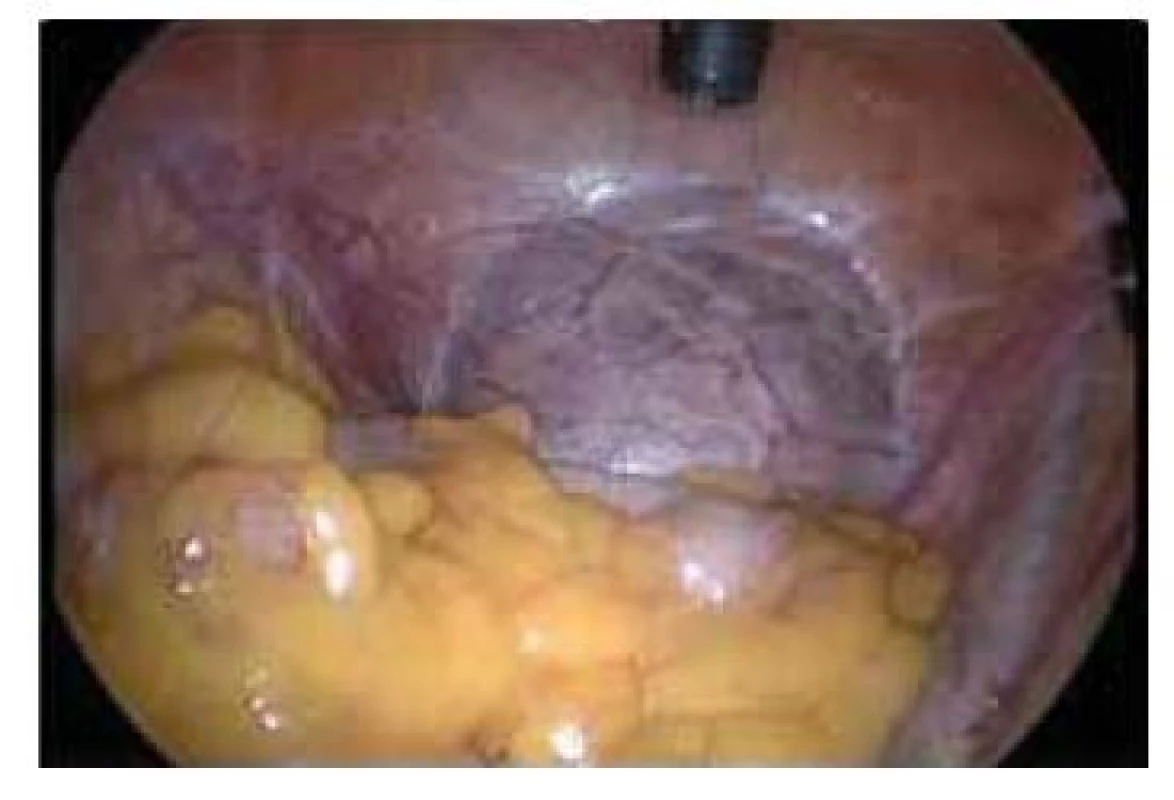
Fig. 4. Laparoscopic view of pregnancy
through a scar after caesarean section.
Gestational age – 11th week.
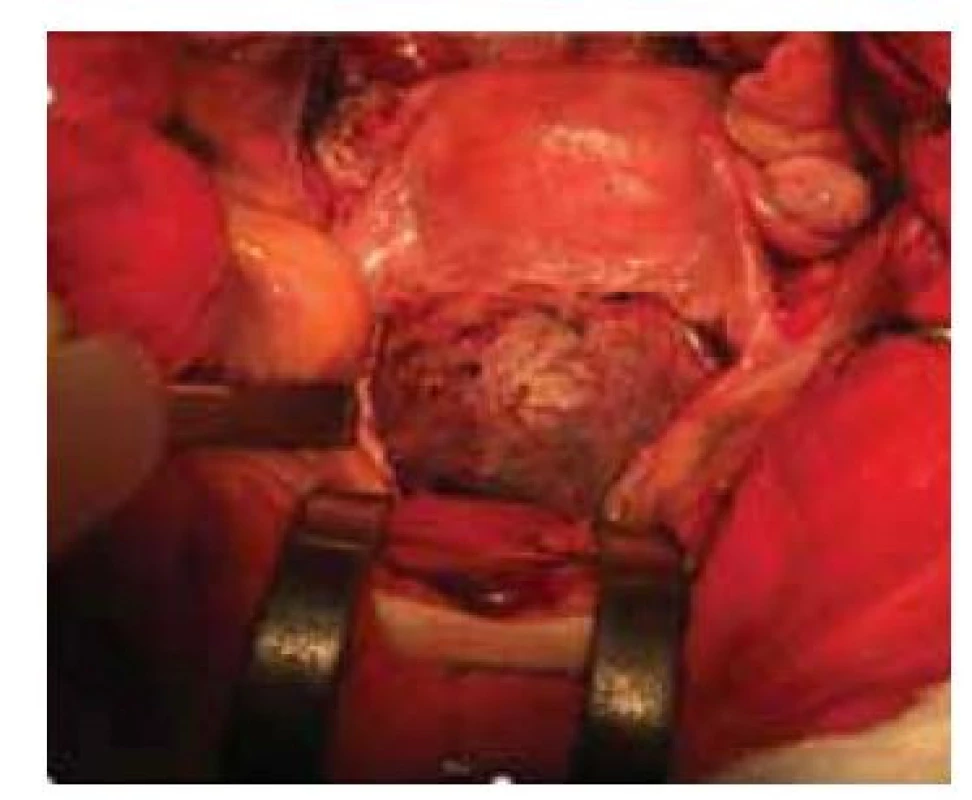
Náš postup
Je závislý na především na týdnu gestace a obtížích pacientky. Při CSP do 8.–10. týdne volíme nejčastěji vakuumaspiraci pod ultrazvukovou kontrolou nebo hysteroskopickou resekci. Při výkonu aplikujeme preventivně Mispregnol.
Při vyšších týdnech gestace provádíme preventivně nejčastěji laparoskopickou ligaci uterinních arterií a připojujeme vakuumaspiraci pod ultrazvukovou kontrolou. Aplikujeme preventivně Mispregnol. Při vyšším krvácení zavádíme foley katétr do dutiny děložní. V případě známek nitrobřišního krvácení volíme nejčastěji laparoskopickou nebo laparotomickou resuturu dolního děložního segmentu.
Všem pacientkám nabízíme s odstupem laparoskopickou resuturu dolního děložního segmentu.
Závěr
S rostoucím počtem císařských řezů dochází i k navyšování tohoto relativně nového typu ektopické gravidity. Právě pro možné krvácivé komplikace s rizikem hysterektomie a poruch placentace je podstatná časná ultrazvuková diagnostika i za použití Power Doppleru. U všech pacientek po císařském řezu je třeba myslet na tuto možnost a zaměřit se na oblast jizvy a vztahu k plodovému vejci a placentě. Terapie by měla být individuální a závislá na gestačním týdnu, hodnotách hCG, krvácivých komplikacích, přání pacientky, vitalitě plodu a dovednostech a možnostech operatéra.
ORCID autorů
J. Hanáček 0000-0002-7976-9079
H. Heřman 0000-0001-5732-3159
P. Křepelka 0000-0002-3663-1635
L. Hašlík 0000-0002-3416-8106
L. Krofta 0000-0001-7372-3953
Doručeno/ Submitted: 25. 3. 2022
Přijato/ Accepted: 31. 3. 2022
MUDr. Jiří Hanáček, Ph.D.
Ústav pro péči o matku a dítě
Podolské nábřeží 157
147 00 Praha 7-Podolí
Zdroje
1. Parker VL, Srinivas M. Non-tubal ectopic pregnancy. Arch Gynecol Obstet 2016; 294(1): 19–27. doi: 10.1007/ s00404-0116-4069-y.
2. Ouyang Y, Li X, Yi Y et al. First-trimester diagnosis and management of Cesarean scar pregnancies after in vitro fertilization – embryo transfer: a retrospective clinical analysis of 12 cases. Reprod Biol Endocrinol 2015; 13 : 126. doi: 10.1186/ s12958-015-0120-2.
3. Tantbirojn P, Crum CP, Parast MM. Pathophysiology of placenta creta: the role of decidua and extravillous trophoblast. Placenta 2008; 29(7): 639–645. doi: 10.1016/ j.placenta.2008. 04.008.
4. Timor-Tritsch IE, Monteaguo A, Cali G et al. Cesarean scar pregnancy and early placenta accreta share common histology. Ultrasound Obstet Gynecol 2014; 43(4): 383–395. doi: 10.1002/ uog.13282.
5. Ash A, Smith A, Maxwell D. Caesarean scar pregnancy. BJOG 2007; 114(3): 253–263. doi: 10.1111/ j.1471-0528.2006.01237.x.
6. Holland MG, Bienstock JL. Recurrent ectopic pregnancy in a cesarean scar. Obstet Gynecol 2008; 111(2 Pt 2): 541–545. doi: 10.1097/ 01. AOG.0000287295.39149.bd.
7. Timor-Tritsch IE, Monteagudo A, Cali G et al. Cesarean scar pregnancy is a precursor of morbidly adherent placenta. Ultrasound Obstet Gynecol 2014; 44(3): 346–353. doi:10.1002/ uog. 13426.
8. Ghezzi F, Laganà D, Franchi M et al. Conservative treatment by chemotherapy and uterine arteries embolization of a cesarean scar pregnancy. Eur J Obstet Gynecol Reprod Biol 2002; 103(1): 88–91. doi: 10.1016/ s0301-2115(02)00003-9.
9. Jurkovic D, Hillaby K, Woelfer B et al. First-trimester diagnosis and management of pregnancies implanted into the lower uterine segment Cesarean section scar. Ultrasound Obstet Gynecol 2003; 21(3): 220–227. doi: 10.1002/ uog.56.
10. Timor-Tritsch IE, Monteagudo A. Unforeseen consequences of the increasing rate of cesarean deliveries: early placenta accreta and cesarean scar pregnancy. A review. Am J Obstet Gynecol 2012; 207(1): 14–29. doi: 10.1016/ j. ajog.2012.03.007.
11. Ko JK, Li RH, Cheung VY. Caesarean scar pregnancy: a 10-year experience. Aust N Z J Obstet Gynaecol 2015; 55(1): 64–69. doi: 10.1111/ ajo.12273.
12. Timor-Tritsch IE, Haynes MC, Monteagudo A et al. Ultrasound diagnosis and management of acquired uterine enhanced myometrial vascularity/ arteriovenous malformations. Am J Obstet Gynecol 2016; 214(6): 731.e1–731.e10. doi: 10.1016/ j.ajog.2015.12.024.
13. Calì G, Timor-Trisch IE, Palacios-Jaraquemada J et al. Changes in ultrasonography indicators of abnormally invasive placenta during pregnancy. Int J Gynaecol Obstet 2018; 140(3): 319–325. doi: 10.1002/ ijgo.12413.
14. Calì G, Forlani F, Minneci G et al. First-trimester prediction of surgical outcome in abnormally invasive placenta using the cross-over sign. Ultrasound Obstet Gynecol 2018; 51(2): 184–188. doi: 10.1002/ uog.17440.
15. Zhang Y, Gu Y, Wang JM et al. Analysis of cases with cesarean scar pregnancy. J Obstet Gynaecol Res 2013; 39(1): 195–202. doi: 10.1111/ j.1447-0756.2012.01782.x.
16. Calì G, Timor-Trisch IE, Palacios-Jaraquemada J et al. Outcome of Cesarean scar pregnancy managed expectantly: systematic review and meta-analysis. Ultrasound Obstet Gynecol 2018; 51(2): 169–175. doi: 10.1002/ uog.17568.
17. Nagi JB, Ofi li-Yebovi D, Sawyer E et al. Successful treatment of a recurrent Cesarean scar ectopic pregnancy by surgical repair of the uterine defect. Ultrasound Obstet Gynecol 2006; 28(6): 855–856. doi: 10.1002/ uog.3843.
18. Bennett TA, Morgan J, Timor-Tritsch IE et al. Fifth recurrent Cesarean scar pregnancy: observations of a case and historical perspective. Ultrasound Obstet Gynecol 2017; 50(5): 658–660. doi: 10.1002/ uog.17461.
19. Wang Q, Peng HL, He L et al. Reproductive outcomes after previous cesarean scar pregnancy: follow up of 189 women. Taiwan J Obstet Gynecol 2015; 54(5): 551–553. doi: 10.1016/ j. tjog.2015.08.006.
20. Ugurlucan FG, Bastu E, Dogan M et al. Management of cesarean heterotopic pregnancy with transvaginal ultrasound-guided potassium chloride injection and gestational sac aspiration, and review of the literature. J Minim Invasive Gynecol 2012; 19(5): 671–673. doi: 10.1016/ j.jmig.2012.05.006.
21. Seow KM, Huang LW, Lin YH et al. Cesarean scar pregnancy: issues in management. Ultrasound Obstet Gynecol 2004; 23(3): 247–253. doi: 10.1002/ uog.974.
22. Petersen KB, Hoff mann E, Larsen CR et al. Cesarean scar pregnancy: a systematic review of treatment studies. Fertil Steril 2016; 105(4): 958–967. doi: 10.1016/ j.fertnstert.2015.12.130.
23. Cok T, Kalayci H, Ozdemir H et al. Transvaginal ultrasound-guided local methotrexate administration as the first-line treatment for cesarean scar pregnancy: follow-up of 18 cases. J Obstet Gynaecol Res 2015; 41(5): 803–808. doi: 10.1111/ jog.12627.
24. Shao MJ, Hu M, Hu MX. Conservative management of cesarean scar pregnancy by local injection of ethanol under hysteroscopic guidance. Int J Gynaecol Obstet 2013; 121(3): 281–282. doi: 10.1016/ j.ijgo.2013.01.012.
25. Vial Y, Petignat P, Hohlfeld P. Pregnancy in a cesarean scar. Ultrasound Obstet Gynecol 2000; 16(6): 592–593. doi: 10.1046/ j.1469-0705. 2000.00300-2.x.
26. Li Y, Gong L, Wu X et al. Randomized controlled trial of hysteroscopy or ultrasonography versus no guidance during D&C after uterine artery chemoembolization for cesarean scar pregnancy. Int J Gynaecol Obstet 2016; 135(2): 158–162. doi: 10.1016/ j.ijgo.2016.04.019.
27. Yang Q, Piao S, Wang G et al. Hysteroscopic surgery of ectopic pregnancy in the cesarean section scar. J Minim Invasive Gynecol 2009; 16(4): 432–436. doi: 10.1016/ j.jmig.2009.03. 015.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicínaČlánek vyšel v časopise
Česká gynekologie

2022 Číslo 3
-
Všechny články tohoto čísla
- Vztah změn mobility uretrovezikální junkce a pooperační progrese stresové inkontinence po sakrospinální fixaci – subanalýza multicentrické randomizované studie
- Screening vrozených vad a geneticky podmíněných onemocnění plodu ve Fakultní nemocnici Olomouc a odesílání/ hlášení do Národního registru reprodukčního zdraví v České republice
- Průběh porodu před císařským řezem a incidence avulze musculus levator ani při prvním následném vaginálním porodu – pilotní studie
- Akutní peripartální hysterektomie – naše 6letá zkušenost
- Syndrom úplné androgenní insenzitivity – raritní kazuistika malignizace dysgenetických gonád
- Hydronefróza jako příznak asymptomatické ureterální endometriózy
- Gravidita v jizvě po císařském řezu
- Systémový lupus erythematosus a sekundární antifosfolipidový syndrom u rodných sester se sníženou plodností
- Fertilitu zachovávající postupy u mladých žen s karcinomem endometria
- Balonková vaginoplastika jako miniinvazivní metoda při řešení vaginální aplazie
- Nádory ovaria a genetická dispozice
- Steroidní metabolom a vícečetné těhotenství
- Recenze knihy Pôrodníctvo
- Prof. MUDr. Alois Martan, DrSc. – 70letý
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
- Gravidita v jizvě po císařském řezu
- Hydronefróza jako příznak asymptomatické ureterální endometriózy
- Nádory ovaria a genetická dispozice
- Syndrom úplné androgenní insenzitivity – raritní kazuistika malignizace dysgenetických gonád
